Clor
Clorul este un element chimic cu numărul atomic 17 și cu simbolul Cl. Este al doilea cel mai ușor halogen, fiind în grupa acestora situat sub fluor și deasupra bromului, astfel încât proprietățile sale sunt oarecum intermediare celor două elemente. Clorul este un gaz de culoare galben-verzui în condiții normale de temperatură. Este un element extrem de reactiv și un agent oxidant puternic: în comparație cu celelalte elemente, are cea mai mare afinitate pentru electroni și a treia cea mai mare electronegativitate (singurii mai electronegativi fiind doar fluorul și oxigenul).
Cel mai răspândit compus al clorului, clorura de sodiu (denumită de obicei sare de bucătărie), a fost cunoscut încă din timpuri străvechi. În jurul anului 1630, clorul gazos a fost sintetizat în urma unei reacții chimice, dar la acel moment nu a fost recunoscut ca o substanță importantă la nivel fundamental. Carl Wilhelm Scheele a realizat o descriere a clorului gazos abia în 1774, crezând că este un oxid al unui nou element. În 1809, chimiștii au sugerat faptul că noul gaz ar putea fi un element pur, ceea ce a și fost confirmat de către Humphry Davy în 1810, care a denumit elementul după termenul din limba greacă veche χλωρός khlôros (verde-pal,) pe baza culorii sale.
Datorită reactivității sale foarte mari, toată cantitatea de clor din scoarța Pământului se află sub formă de compuși ai clorului, de obicei cloruri ionice, printre care se numără și sarea de bucătărie. Este al doilea cel mai răspândit halogen (după fluor) și al 21-lea cel mai răspândit element chimic din scoarța terestră. Pe de altă parte, cantitatea de săruri de clor din depozitele subterane sunt minore în comparație cu cantitatea imensă de clorură de sodiu dizolvată în apa de mare.
Clorul molecular este obținut la nivel industrial prin procedeul electrolizei saramurii. Potențialul mare de oxidare al clorului elementar a dus la dezvoltarea unor utilizări importante, precum producerea înălbitorilor, agenților dezinfectanți și a reactivilor folosiți pe larg în procedeele din industria chimică. Clorul este folosit pentru fabricarea unei game largi de produse uzuale și folositoare, aproximativ două treimi dintre aceștia fiind compuși organici precum policlorura de vinil, dar și mulți compuși intermediari pentru fabricarea materialelor plastice și dezinfecția piscinelor publice. Clorul elementar, la concentrații ridicate, este extrem de periculos și de toxic pentru toate organismele vii, și de aceea a fost folosit ca armă de război chimic în Primul Război Mondial, fiind primul compus gazos de acest gen.
Sub forma ionului, care este în alcătuirea sărurilor comune și a altor compuși, este abundent în natură și necesar multor forme de viață, inclusiv a omului. În starea sa elementară prezintă moleculă diatomică. Clorul este un agent oxidant puternic, fiind utilizat în procesele de albire și dezinfectare. În stratul superior al atmosferei, moleculele care conțin clor au fost implicate în distrugerea stratului de ozon.
Istoric[modificare | modificare sursă]
Clorul a fost produs pentru prima oară în 1774 de către Carl Wilhelm Scheele. Scheele a colectat gaz eliberat de reacția propulsiei cu dioxid de mangan[necesită citare]. Noul gaz a avut, în conformitate cu Scheele, un miros foarte perceptibil și în aer căpăta o culoare galben-verzuie. Scheele a remarcat de asemenea calitățile de albire ale noului gaz.
Carl Wilhelm Scheele a izolat clorul prin reacția piroluzitului (dioxid de mangan, MnO2) cu acidul clorhidric (HCl):[2]
- 4 HCl + MnO2 → MnCl2 + 2 H2O + Cl2
Structură atomică[modificare | modificare sursă]
Clorul face parte din familia halogenilor, grupa 17. Are 7 electroni de valență, 18 neutroni, 17 protoni și 17 electroni. Configurația electronică este: 1s2 2s2 2p6 3s2 3p5. Deoarece are 7 electroni pe ultimul strat, atomul de clor este instabil și caută un element cu care să se combine pentru a-și forma structura stabilă de 8 electroni.
Este situat în perioada a 3-a, grupa a VII-a principală. Valență: electrovalență -1, covalență – față de H:Cl (I) _ față de O:Cl(VII,V,III,I). Are caracter electrochimic electronegativ și caracter chimic nemetalic. Are molecula diatomică: Cl2.
Proprietăți[modificare | modificare sursă]
Proprietăți fizice[modificare | modificare sursă]
-Stare gazoasă;
-Culoare Galben verzui;
-Solubil în apă, formând o soluție numită APA DE CLOR;
-Densitate mai mare decât a aerului;
-Extrem de toxic;
-Acționează asupra căilor respiratorii.
Proprietăți chimice[modificare | modificare sursă]
-Reacționează cu substanțe simple
Cl2+H2=2HCl
Cl2+Mg=MgCl2
3Cl2+Fe3=2FeCl3
-Reacționează cu substanțe compuse
-Reacționează cu baze tari
Cl2+2NaOH=NaCl+NaClO+H2O
-Reacționează cu săruri
Cl2+2KBr=2KCl+Br2
-Din reacția clorului cu hidrogenul, in prezenta luminii, se
formeaza acidul clorhidric:
H2+Cl2=2HCl
Stări de oxidare[modificare | modificare sursă]
Clorul poate avea următoarele stări de oxidare:
- -1, în cloruri
- 0, în molecula biatomică de Cl2
- +1, în hipocloriți și acid hipocloros
- +3, în cloriți și acid cloros
- +5, în clorați și acid cloric
- +7, în perclorați și acid percloric
Compuși[modificare | modificare sursă]
Clorura de hidrogen și acidul clorhidric[modificare | modificare sursă]
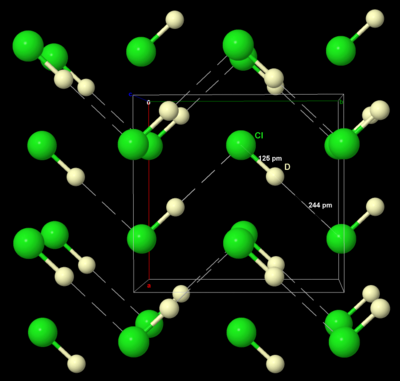
Cel mai simplu compus al clorului este clorura de hidrogen, cu formula HCl, o substanță deosebit de importantă, atât la nivel industrial, cât și în laborator. Compusul este întâlnit atât sub formă de gaz, cât și sub formă de soluție, dizolvat în apă, când se numește acid clorhidric. Se obține de obicei prin sinteza directă din elemente, prin arderea împreună a clorului și hidrogenului gazos, sau ca produs secundar al reacției de clorurare a hidrocarburilor. O altă metodă pune în valoare proprietatea acizilor tari de a scoate alți acizi din sărurile lor, astfel că se tratează clorura de sodiu cu acid sulfuric concentrat cu obținerea de acid clorhidric:[3]
- NaCl + H2SO4 NaHSO4 + HCl
- NaCl + NaHSO4 Na2SO4 + HCl
În laborator, clorura de hidrogen gazoasă se poate obține prin deshidratarea acidului clorhidric cu acid sulfuric concentrat. Clorura de deuteriu, DCl, poate fi obținută prin reacția clorurii de benzoil cu apa grea (D2O).[3]
La temperatura camerei, clorura de hidrogen este un gaz incolor, la fel ca și celelalte halogenuri de hidrogen (cu excepția fluorurii de hidrogen), din moment ce atomul de hidrogen nu formează legături de hidrogen puternice cu atomul de clor, mai mare și mai electronegativ; totuși, apar legături de hidrogen slabe în cadrul structurii cristaline a clorurii de hidrogen, la temperaturi scăzute, când compusul are o formă similară cu analogul de fluor.[3] Acidul clorhidric este un acid tare (pKa = −7) deoarece legăturile hidrogenului cu clorul sunt prea slabe pentru a putea disocia. În soluție apoasă, amestecul HCl/H2O poate fi întâlnit în diferite forme hidratate, mai exact HCl·nH2O, unde n = 1, 2, 3, 4 și 6. În cazul unui amestec de HCl și H2O, sistemul se împarte complet în două faze lichide separate. Acidul clorhidric formează un amestec azeotrop, a cărui punct de fierbere este 108,58 °C pentru o concentrație de 20,22 g HCl per 100 g de soluție; astfel, se consideră că acidul clorhidric nu poate fi concentrat peste acest punct.[4]
Spre deosebire de fluorura de hidrogen, clorura de hidrogen în stare lichidă și anhidră este mult mai greu de utilizat ca solvent, întrucât are un punct de fierbere foarte scăzut, punctul de topire destul de apropiat de acesta, are o constantă dielectrică mică și nu disociază bine în ioni H2Cl+ și HCl−
2 – cel din urmă, în orice caz, este mult mai puțin stabil decât ionii bifluorură sau dihidrogenofluorură (HF−
2), datorită legăturilor foarte slabe de hidrogen ce se formează între atomii de hidrogen și clor. Totuși, se pot izola unele săruri ale acestui ion cu unii cationi foarte slab polarizabili, precum Cs+ și NR+
4 (unde R = Me, Et, Bun). Clorura de hidrogen anhidră este un solvent slab, care are capacitatea de a dizolva compușii cu molecule mici, precum clorura de nitrozil (NOCl) sau fenolul, sau săruri cu energie reticulară mică, precum halogenurile de tetraalchilamoniu. Protonează cu ușurință electrofili ce conțin perechi de electroni neparticipanți sau legături π. Pentru soluțiile de clorură de hidrogen, sunt foarte caracteristice reacțiile de solvoliză, de înlocuire de ligand sau de oxidare:[5]
- Ph3SnCl + HCl → Ph2SnCl2 + PhH (solvoliză)
- Ph3COH + 3 HCl → Ph3C+HCl2- + H3O+Cl− (solvoliză)
- Me4N+HCl2- + BCl3 → Me4N+BCl4- + HCl (înlocuire de ligand)
- PCl3 + Cl2 + HCl → PCl4+HCl2- (oxidare)
Alte cloruri binare[modificare | modificare sursă]

Aproape toate elementele din sistemul periodic formează compuși binari cu clorul, compuși care sunt denumiți cloruri. Pentru puținele excepții, adică elementele care nu formează cloruri, se poate explica inexistența acestor compuși prin următoarele cauze: elementul ori este extrem de inert și de nereactiv pentru a participa la reacții chimice (gazele nobile, cu excepția xenonului, care formează clorurile XeCl2 și XeCl4), ori are un nucleu instabil și deci este susceptibil de dezintegrare radioactivă rapidă (majoritatea elementelor grele de după bismut), sau în cele din urmă are o electronegativitate mai mare decât clorul (oxigenul și fluorul), caz în care compușii binari rezultați în urma reacției chimice dintre clor și celălalt element vor fi oxizi de clor și respectiv fluoruri de clor, ci nu cloruri ale acestora.[6]
Prin clorurarea metalelor cu Cl2 se obțin de obicei compuși în care metalul are o stare de oxidare mai mare decât în cazul reacției de bromurare cu Br2, când se obțin stări de oxidare multiple. Un exemplu ar fi următoarele halogenuri de molibden: MoCl5 și MoBr3. Clorurile se pot obține prin reacția directă dintre un element, oxidul său, hidroxidul său sau carbonatul său cu acid clorhidric, iar apoi deshidratat la temperaturi ridicate, la presiune scăzută sau în atmosferă de clorură de hidrogen gazoasă. Această metodă este folositoare atunci când clorura care se obține este stabilă față de hidroliză. Alte metode includ: clorurarea oxidativă a elementului la temperaturi ridicate, reacție care se realizează cu clor sau clorură de hidrogen; clorurarea la temperaturi ridicate a unui oxid metalic sau a unei halogenuri cu clor, tetraclorură de carbon sau o clorură organică. De exemplu, dioxidul de zirconiu reacționează cu clorul în condiții standard cu obținerea de tetraclorură de zirconiu, iar trioxidul de uraniu reacționează cu hexacloropropena la încălzire cu obținere de tetraclorură de uraniu. Cea din urmă presupune și o reducere a numărului de oxidare, ceea ce se poate realiza și prin reducerea unei cloruri superioare, folosindu-se hidrogen sau un metal ca agent reducător. De asemenea, același rezultat se obține și prin reacția de descompunere termică sau reacția de disproporționare:[6]
- EuCl3 + 12 H2 → EuCl2 + HCl
- ReCl5 ReCl3 + Cl2
- AuCl3 AuCl + Cl2
Fluoruri de clor[modificare | modificare sursă]
Oxizi de clor[modificare | modificare sursă]
Oxoacizi și oxoanioni de clor[modificare | modificare sursă]
Compuși organici cu clor[modificare | modificare sursă]
Răspândire[modificare | modificare sursă]
Clorul se găsește în natură sub formă de cloruri. Clorurile alcătuiesc cea mai mare parte a sărurilor din apa oceanică - ionii de clorură reprezintă aproximativ 1,9% din masa oceanica - dar se întâlnesc și sub forma depozitelor solide în scoarța terestră.
În natură se găsesc doar izotopii 35 și 37, într-o proporție de aproximativ 3:1, ceea ce dă atomilor de clor o masă generală de 35,5.
Producere[modificare | modificare sursă]
Molecula diatomică de clor se poate obține din clorurile sale prin oxidare cu agenți oxidanți puternici sau electroliză, sau din compușii cu numere de oxidare superioare lui 0 prin reducere.
Industrial, se obține prin electroliza unei soluții de NaCl, după ecuația:
2NaCl + 2 H2O → Cl2 + H2 + 2 NaOH
Preparare în laborator[modificare | modificare sursă]
Producere la scară industrială[modificare | modificare sursă]

În industria chimică, clorul este, de obicei, produs prin electroliza clorurii de sodiu dizolvată în apă. Această metodă, industrializată în 1892, este folosită în prezent pentru a traduce tot clorul gazos industrial. Odată cu clorul, metoda produce hidrogen gazos și hidroxid de sodiu (hidroxidul de sodiu fiind, de fapt, cel mai important dintre cele trei produse industriale obținute). Procesul funcționează conform ecuației chimice următoare:[7]
2NaCl + 2H2O → Cl2 + H2 + 2NaOH
Electroliza soluțiilor de clorură are loc în conformitate cu următoarele ecuații:
Catod: 2H + (aq) + 2 e-→ H2 (g) Anod: 2Cl-(aq) → Cl2 (g) + 2 e-
Procesul global: 2NaCl (sau KCl) + 2H2O → Cl2 + H2 + 2NaOH (sau KOH)
În electroliza cu diafragmă, o diafragmă din azbest (sau fibră de polimer) separă un catod și un anod, prevenind formarea clorului la anod la reamestecare cu hidroxidul de sodiu și hidrogenul format la catod[8]. Soluția de sare (saramura) este continuu alimentată la compartimentul anodic și curge prin membrana la compartimentul catodic, unde se produce caustica alcalină și saramură sunt parțial epuizate. Metode de membrane produc diluat și ușor impurificată alcaline, dar ele nu sunt împovărate cu problema de a preveni descărcarea mercuruluui în mediu și sunt mai eficiente energetic. Electroliza membranei celulei angaja membrană permeabilă ca un schimbător de ioni. Sodiul saturat (sau de potasiu) soluția de clorură este trecută prin compartimentul anodic, lăsând la o concentrație mai mică[9]. Această metodă este mai eficientă decât cea cu diafragmă și produce un sodiu foarte pur (sau potasiu), hidroxidul de la concentrație este de aproximativ 32%, dar necesită saramură foarte curată.
Utilizare[modificare | modificare sursă]

Clorul este folosit în purificarea apei, dezinfectanți, înălbitori fiind un gaz asfixiant este folosit și la producerea gazului de luptă gazul de muștar.
Clorul se regăsește și în utilizările de zi cu zi:
- Sub formă de acid hipocloros(HClO), obținut prin hidroliza hipocloritului de sodiu(NaClO). Se utilizează pentru eliminarea bacteriilor și a altor microbi din apa de băut și piscine.
- Folosit în cantități mari în: produse de hârtie, produse antiseptice, coloranți, mâncare, insecticide, vopsele, produse petroliere, produse plastice, medicină, textile, solvenți, precum și multe alte produse de larg consum.
În chimia organică se folosesc proprietățile oxidante ale clorului pentru a substitui atomi de hidrogen din componența moleculelor, conferindu-le diferite proprietăți superioare(de exemplu în copolimerii din cauciucurile sintetice)
Soluțiile perfuzabile, denumite ser fiziologic sunt soluții de 0,9% NaCl.
Alte utilizări includ: producerea de clorați, cloroform, tetraclorură de carbon și extragerea bromului.
Rolul biologic[modificare | modificare sursă]
Rolul biologic al compușilor clorului este considerabil. Sarea de bucătărie NaCl este o necesitate vitală pentru om și animale. În Antichitate, din cauza sării NaCl se purtau războaie; sarea era prețuită mai mult decât aurul. Acidul clorhidric se conține in sucul gastric si contribuie la asimilarea hranei.
Siguranță[modificare | modificare sursă]
Clorul este mortal în cantități mari. Pentru că este mai greu decât aerul, el înlocuiește oxigenul din plămâni.
Referințe[modificare | modificare sursă]
- ^ Commission on Isotopic Abundances and Atomic Weights: Conventional Atomic Weights, 2013
- ^ en Greenwood, N., Earnshaw, A., Chemistry of the Elements (2nd ed.), Oxford: Butterworth-Heinemann, 1997, p. 790. ISBN 0-08-037941-9
- ^ a b c Greenwood and Earnshaw, pp. 809–812
- ^ Greenwood and Earnshaw, pp. 812–6
- ^ Greenwood and Earnshaw, pp. 818–9
- ^ a b Greenwood and Earnshaw, pp. 821–4
- ^ Wiberg 2001, p. 408.
- ^ „The diaphragm cell process”. Euro Chlor. Accesat în .
- ^ „The membrane cell process”. Euro Chlor. Accesat în .
Lectură suplimentară[modificare | modificare sursă]
- Raluca Ripan, I. Ceteanu, Manual de lucrări practice de chimie anorganică - vol I Metaloizi, Editura de stat didactică și pedagogică, București, 1961, p. 66-95
Legături externe[modificare | modificare sursă]
- ro Clorul pe sistemul-periodic.go.ro Arhivat în , la Wayback Machine.
- http://www.chemicool.com/elements/chlorine.html#discovery
- Clorul de la The Periodic Table of Videos (University of Nottingham)
- Agency for Toxic Substances and Disease Registry: Chlorul
- Producerea electrolitică
- Producerea și lichefierea clorului Arhivat în , la Wayback Machine.
- Chlorine Production Using Mercury, Environmental Considerations and Alternatives
- National Pollutant Inventory – Chlorine
- National Institute for Occupational Safety and Health – Chlorine Page
- Chlorine Institute Arhivat în , la Wayback Machine. – Trade association representing the chlorine industry
- Chlorine Online – the web portal of Eurochlor – the business association of the European chlor-alkali industry
 „Chlorine”. Encyclopædia Britannica. 6 (ed. 11). . pp. 254–256.
„Chlorine”. Encyclopædia Britannica. 6 (ed. 11). . pp. 254–256.
| |||||||||||||||||||||||||||||||||||||
| |||||||||||

