Moleculă
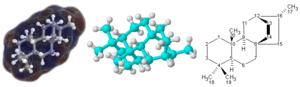
Molecula e cea mai mică parte dintr-o substanță care păstrează compoziția procentuală și toate proprietățile chimice ale acelei substanțe.[1] O moleculă este definită ca un grup electric neutru, destul de stabil, format din cel puțin doi atomi într-un anumit aranjament, legați împreună în conformitate cu legături chimice foarte puternice (covalente).
Caracteristici
[modificare | modificare sursă]Moleculele au dimensiuni foarte mici în comparație cu distanțele dintre ele. Există spații intermoleculare foarte mari, în comparație cu dimensiunile moleculelor. Între molecule există forțe de coeziune care sunt mai mici pentru gaze și mai mari pentru lichide sau solide. Moleculele sunt stabile și neutre din punct de vedere electric.
O altă caracteristică este imobilitatea acestora. Datorită imobilității, se difuzează unele printre celelalte sau prezintă fenomenul de dizolvare pentru lichide sau solide.
Moleculele se află într-o continuă mișcare.
Alcătuire
[modificare | modificare sursă]După natura atomilor componenți, pot fi molecule formate din atomi identici (H2, O2, Cl2) sau formate din atomi diferiți (HCl, H2O, NH3, CH4).
În funcție de numărul de atomi prezenți într-o moleculă, aceasta poate fi:
- diatomică: O2, N2, Cl2, I2, H2, Br2
- triatomică: O3
- tetraatomică: C4
- pentaatomică: P5
- octoatomică: S8
Descoperire
[modificare | modificare sursă]În anul 2019 a fost descoperită prima moleculă formată în univers la cca 300.000 ani după Big Bang, hidrura de heliu (HeH+). Este o combinație între un atom de heliu și un proton (fără electroni) de hidrogen. Descoperirea s-a făcut cu ajutorul observatoriului astronomic SOFIA (Stratospheric Observatory for Infrared Astronomy, plasat în stratosferă, o cooperare germano-americană) în nebuloasa planetară NGC 7027.
Vezi și
[modificare | modificare sursă]- Atom
- Moleculă Van der Waals
- Moleculă diatomică
- Polaritate chimică
- Geometrie moleculară
- Legătură covalentă
Referințe
[modificare | modificare sursă]Legături externe
[modificare | modificare sursă]- en Molecule of the Month – School of Chemistry, University of Bristol

