Clorură de mercur (I)
| Clorură de mercur (I) | |
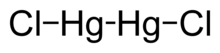 | |
 | |
| Identificare | |
|---|---|
| Număr CAS | 10112-91-1 |
| PubChem CID | 24956 |
| Formulă chimică | Cl₂Hg₂[1] |
| Masă molară | 472 u.a.m.[2] |
| Punct de topire | 543 °C[3] |
| Structură cristalină | Sistem cristalin tetragonal |
| Sunt folosite unitățile SI și condițiile de temperatură și presiune normale dacă nu s-a specificat altfel. | |
| Modifică date / text | |
Clorură de mercur (I), denumită și clorură mercuroasă sau calomel (ca atare, cât și sub forma mineralului cu același nume)[4] este un compus anorganic, o sare a acidului clorhidric cu mercurul, cu formula chimică Hg2Cl2. Este un compus alb sau alb-gălbui, inodor și solid. Este un component al electrozilor de referință utilizați în electrochimie.[5][6]
Obținere[modificare | modificare sursă]
Clorura mercuroasă se obține în urma reacției dintre mercurul metalic și clorura mercurică:
Mai poate fi preparată în urma unor reacții de metateză ce au loc între diverse surse de ion clorură (clorură de sodiu, acid clorhidric, etc) și o soluție apoasă de azotat de mercur (I):
Proprietăți chimice[modificare | modificare sursă]
Amoniacul induce disproporționarea Hg2Cl2:[7]
Note[modificare | modificare sursă]
- ^ a b „Clorură de mercur (I)”, Mercurous chloride (în engleză), PubChem, accesat în
- ^ „Clorură de mercur (I)”, Mercurous chloride (în engleză), PubChem, accesat în
- ^ Basic laboratory and industrial chemicals: A CRC quick reference handbook[*] Verificați valoarea
|titlelink=(ajutor) - ^
 Chisholm, Hugh, ed. (). „Calomel”. Encyclopædia Britannica (ed. 11). Cambridge University Press.
Chisholm, Hugh, ed. (). „Calomel”. Encyclopædia Britannica (ed. 11). Cambridge University Press.
- ^ Housecroft, C. E.; Sharpe, A. G. (2004). Inorganic Chemistry (ed. 2). Prentice Hall. pp. 696–697. ISBN 978-0-13-039913-7.
- ^ Skoog, Douglas A.; Holler, F. James; Nieman, Timothy A. (). Principles of Instrumental Analysis (ed. 5). Saunders College Pub. pp. 253–271. ISBN 978-0-03-002078-0.
- ^ „Characteristic Reactions of Mercury Ions (Hg²⁺ and Hg₂²⁺)”, Chemistry LibreTexts, , accesat în
Vezi și[modificare | modificare sursă]
| |||||||||||



