Glucoză
| Glucoză | |
 | |
 | |
| Identificare | |
|---|---|
| Număr CAS | 50-99-7 |
| Formulă chimică | C₆H₁₂O₆[1] |
| Sunt folosite unitățile SI și condițiile de temperatură și presiune normale dacă nu s-a specificat altfel. | |
| Modifică date / text | |

|
| Glucoză dextrogir |

|
| Glucoză levogir |
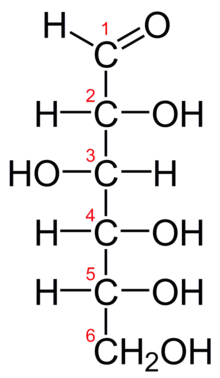
Glucoza este compusul organic, aparținând clasei zaharidelor, care are formula chimică C6H12O6. Deși are aceeași formulă chimică, fructoza este diferită față de glucoză prin modul de legare a atomilor. Astfel, glucoza are o singură grupare de alcool primar (în imagine, la carbonul cu numărul 6), pe când fructoza are două grupări de alcool primar.
Structură[modificare | modificare sursă]
Glucoza conține șase atomi de carbon și o grupă carbonil (specifică aldehidelor) și este numită uneori aldohexoză. În natură, în unele plante, glucoza există sub formă de structură aciclică; în altele, ea poate fi găsită sub formă ciclică. Teoretic, structura ciclică a glucozei apare în urma interacțiunii dintre grupa carbonil și grupele hidroxil de la carbonii cu cifrele 4 și 5. Aceste interacțiuni sunt reacții de adiție a grupelor hidroxil amintite la grupa carbonil. În soluție apoasă, cele două forme se află în echilibru, și la un pH 7, forma ciclică este predominantă.
La formarea structurii ciclice a glucozei, apare la fosta grupă carbonil o nouă grupare hidroxil, care se numește hidroxil glicozidic și care are o reactivitate mai mare decât celelalte grupe hidroxil din moleculă. În acest caz, numerotarea carbonilor începe de la primul carbon de după oxigenul din ciclu, în sens orar.
Izomeri[modificare | modificare sursă]
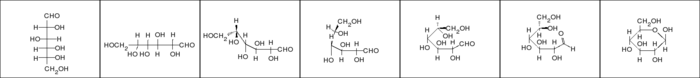
Glucoza are patru centre optice, deci teoretic glucoza poate avea 16 stereoizomeri optici. Doar șapte dintre aceștia sunt găsiți în natură, iar dintre ei, cei mai importanți sunt galactoza (Gal) și manoza (Man). Acești opt izomeri (incluzând și glucoza) sunt toți diastereoizomeri unul față de celălalt și aparțin seriei-D.
În cazul glucozei (dar și al fructozei, în mod echivalent), un alt centru asimetric la carbonul 1 (numit carbonul anomeric) este creat când glucoza trece în forma ciclică și se formează două structuri inelare, numite anomeri (un caz particular de izomeri) — α-glucoza și β-glucoza. α-glucoza este acea structură a glucozei în care grupele hidroxil de la carbonii cu numerele 1 și 4 se află de aceeași parte a planului ciclului hexagonal, iar β-glucoza este structura în care cei doi hidroxili se află de părți diferite ale planului. Formele α și β pot trece dintr-una în alta în soluție apoasă pe o perioadă de câteva ore, stabilizându-se la un raport α:β 36:64.
Proprietăți fizice[modificare | modificare sursă]
Glucoza este o substanță solidă, cristalizată, albă și solubilă în apă. Are un gust dulce. Punctul său de topire este foarte ridicat, deoarece între numeroasele sale grupări hidroxil (-OH) se formează multe legături de hidrogen. Când sunt încălzite, toate monozaharidele (nu numai glucoza) se descompun înainte de a se topi, în carbon și apă, reacție numită carbonizare. Glucoza are 75% din puterea de îndulcire a fructozei (care este luată ca unitate).
Proprietăți chimice[modificare | modificare sursă]
Reacții la grupa carbonil[modificare | modificare sursă]
Reacții comune aldehidelor și cetonelor[modificare | modificare sursă]
În această reacție, se adiționează o moleculă de hidrogen diatomică la o moleculă de glucoză, adiția având loc la dubla legătură dintre oxigen și carbon. Legătura dintre cei doi atomi se rupe, iar câte un atom de hidrogen se leagă la fiecare dintre ei și astfel se produce hexitolul (sorbitol).
Reacții caracteristice aldehidelor[modificare | modificare sursă]
Reacții la grupa hidroxil[modificare | modificare sursă]
Reacția de esterificare[modificare | modificare sursă]
Glucoza, în reacție cu clorura acidului acetic, produce esterul pentacilat al glucozei și acid clorhidric.
Reacția de eterificare[modificare | modificare sursă]
Reacția de esterificare are loc doar cu un ester anorganic, precum sulfatul acid de metil.
Reacția de fermentație[modificare | modificare sursă]
Această reacție are loc în prezență de enzime, care au rol de biocatalizator. Astfel, din glucoză rezultă alcool etilic și dioxid de carbon.
Obținere[modificare | modificare sursă]
Naturală[modificare | modificare sursă]
- Glucoza este unul dintre produșii de fotosinteză a plantelor și a unor procariote. Se găsește îndeosebi în sucul fructelor dulci ale plantelor.
- La animale și ciuperci, glucoza este rezultatul descompunerii glicogenului, proces numit glicogenoliză. La plante, se descompune amidonul.
- La animale, glucoza este sintetizată în ficat și rinichi din intermediari care nu sunt carbohidrați, precum piruvat și glicerol, proces numit gluconeogeneză.
Industrială[modificare | modificare sursă]
La scară industrială, glucoza se obține prin hidroliza amidonului în mediu acid.
O altă metodă este hidroliza enzimatică a amidonului. Multe culturi pot fi folosite ca sursă pentru amidon: porumbul, orezul, grâul, cartofii sunt utilizați la scară largă în toată lumea.
Procesul enzimatic are două etape. Pe durata a 1-2 ore, la aproximativ 100 °C, enzimele descompun amidonul în carbohidrați mai mici, cu o moleculă formată din 5-10 unități de glucoză. Unele variațiuni ale acestui proces încălzesc amidonul la aproximativ 130 °C sau mai mult de câteva ori. Astfel se îmbunătățește solubilitatea amidonului în apă, dar se dezactivează enzimele, așa că enzime noi trebuie adăugate în amestec după fiecare încălzire.
În a doua etapă, numită zaharificare, amidonul parțial hidrolizat este hidrolizat complet până la glucoză folosind enzima glucoamilază provenită de la ciuperca Aspergillus niger. Condițiile de reacție specifice sunt la un pH de 4,0–4,5, o temperatură de 60 °C și o cantitate de carbohidrați de 30–35%. În aceste condiții, amidonul poate fi convertit în glucoză în proporție de 96% după 1–4 zile. Totuși, se pot obține reacții cu randamente mai mari folosind soluții mai diluate, dar în acest fel sunt necesare reactoare mai mari și cantități mai mari de apă, și de aceea această modalitate nu este considerată economică. Soluția de glucoză rezultată este apoi purificată prin filtrare și concentrată prin evaporarea apei. D-glucoza solidă este produsă apoi prin cristalizări repetate.
Rol biologic[modificare | modificare sursă]

Se poate specula asupra cărui fapt se datorează răspândirea atât de mare a glucozei, și nu a altor monozaharide, precum fructoza. Glucoza se poate forma din formaldehidă în condiții abiotice, deci se poate ca ea să fie fost disponibilă pentru sistemele biochimice primitive. Glucoza este foarte răspândită în regnul animal și vegetal, și este principala oză din organismul uman.
Sursă de energie[modificare | modificare sursă]
Glucoza este un combustibil esențial în biologie. Carbohidrații reprezintă sursa principală de energie pentru corpul uman, producând 4 kilocalorii (17 kilojouli) pe gram. Descompunerea carbohidraților (amidonul, de exemplu) produce mono și dizaharide, iar o mare parte dintre produși este glucoză. Prin glicoliză și prin reacțiile ciclului acidului citric, glucoza este oxidată pentru a forma dioxid de carbon și apă, rezultând și energie, în principal sub formă de ATP.
Este distribuită în toate celulele și fluidele organismului, cu excepția urinei. În ser, concentrația de glucoză (glicemie) normală este de 80–110 mg/dl. Menținerea glicemiei în limite constante este asigurată prin acțiunea antagonistă a doi hormoni ai pancreasului endocrin: insulină (hipoglicemiant) și glucagon (hiperglicemiant). Creșterea cantității de glucoză în sânge este specifică diabetului zaharat, iar în urină (glicozurie) apare numai când glicemia depășește 160–180 mg/dl. Măsurarea concentrației sanguine se poate realiza cu glucometrul.
Precursor[modificare | modificare sursă]
Glucoza este esențială în producerea proteinelor și în metabolismul lipidelor. De asemenea, la cele mai multe plante și animale, este un precursor pentru vitamina C (acid ascorbic).
Glucoza este folosită ca precursor la sinteza unor substanțe importante. Amidonul, celuloza și glicogenul sunt polimeri (polizaharide) comuni ai săi. Lactoza - zahărul din lapte, este o dizaharidă compusă din glucoză și galactoză. În zaharoză, o altă dizaharidă importantă, glucoza este legată de fructoză.
Glucoza intră în structura diglucidelor și poliglucidelor. Prin oxidare în ficat se transformă în acid glucuronic, care are un rol important în glucuronoconjugare.
Utilizare[modificare | modificare sursă]

Există mai multe forme de comercializare și folosire a glucozei, dintre care cele mai importante sunt:
- sirop de glucoză - conține glucoză în concentrație de 32,40%;
- glucoza tehnică - cu o concentrație de 75%;
- glucoza cristalizată (tablete) - concentrație de 99%.
În medicină este folosită mai ales sub formă de soluții apoase perfuzabile. În funcție de concentrațiile lor, acestea au acțiuni și indicații diferite. Soluțiile sub 5 % sunt utilizate pentru diluarea unor medicamente, pentru hidratare sau ca substituent energetic. Soluția de glucoză 5 % este izotonă și are aceleași utilizări, fiind folosită cel mai adesea. Soluțiile de concentrații mai mari de 5 % (10, 20, 33, 40 %) sunt hipertonice și își găsesc utilitatea ca diuretice osmotice (realizează deshidratare tisulară, foarte utilă în edeme). Pentru a evita efectele nefaste ale hiperglicemiei, de obicei oricărei perfuzii cu glucoză i se adaugă insulină.
Vezi și[modificare | modificare sursă]
Bibliografie[modificare | modificare sursă]
S. Ifrim Chimia zahararurilor, 2009
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||



![{\displaystyle +[O]\rightarrow }](https://wikimedia.org/api/rest_v1/media/math/render/svg/10591a44832b58f0ee2fedb7d911d81a26e41c31)




