Oxid
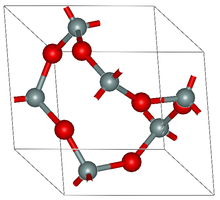
Oxidul (grec. oxys=ascuțit, usturător, acru) se formează printr-o legătură dintre un element chimic cu oxigenul, proces chimic numit reacție de oxidare. După modul în care reacționează cu apa, oxizii sunt de două tipuri: oxizi acizi și oxizi bazici. Oxizii sunt compuși binari ai oxigenului în reacție cu metale sau nemetale.
Proprietăți fizice[modificare | modificare sursă]
Ionul de oxigen O2-- nu poate fi găsit în stare liberă în natură, ci numai sub formă de combinații cu cationii din săruri.
Gruparea hidroxilică -OH este o grupare care determină caracterul bazic puternic al unor alcali ca NaOH, acceptori de sarcini pozitive (protoni).
Oxigenul se combină cu majoritatea elementelor chimice, formând oxizi, cu excepția unor elemente ca gazele: heliu, neon, argon, kripton și fluor.
Fluorul este un caz aparte deoarece se formează legături între oxigen și acest element sub forma OF2, O2F2 și O4F2, însă datorită caracterului electronegativ accentuat al fluorului, aceste combinații nu sunt numiți oxizi ci fluoruri.
Cea mai mare parte a scoarței pământului, (vezi straturile pământului) este formată din oxizi. În această categorie, o pondare de agregare solidă, restul oxizilor de nemetal au stare gazoasă.Oxizii de metal prezintă culori diferite, pe când oxizii de nemetal sunt incolori.
Proprietăți chimice[modificare | modificare sursă]
- Oxizii bazici formează în reacție cu apa baze:
- CaO + H2O = Ca(OH)2
- Oxizii acizi formează în reacție cu apa acizi:
- CO2 + H2O = H2CO3
- Oxizii metalici reacționează cu acizii formând o sare și apă (H2O)
- 2HNO3 + CaO = Ca(NO3)2 + H2O
- Oxizii acizi neutralizează bazele formând o sare și apă (H2O)
- 2NaOH + CO2 = Na2CO3 + H2O
