Hipotalamus
| Hipotalamusul | |
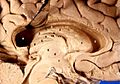
 Localizarea hipotalamusului uman | |
 Localizarea hipotalamusului în raport cu glanda hipofiză și restul creierului (colorat în albastru) | |
| Detalii | |
|---|---|
| Latină | hypothalamus |
| Parte din | creier |
| Sistem | sistemul nervos |
| Resurse externe | |
| Gray's | p.812 |
| TA | A14.1.08.401 A14.1.08.901 |
| FMA | 62008 |
| Terminologie anatomică | |
Hipotalamusul (din greaca veche ὑπό, „sub”, și θάλαμος, „cameră”) este o porțiune a creierului care conține un număr de nuclei mici cu o varietate de funcții. Una dintre cele mai importante funcții ale hipotalamusului este legarea sistemului nervos de sistemul endocrin prin intermediul glandei pituitare.Hipotalamusul este situat sub talamus și face parte din sistemul limbic. [1] În terminologia neuroanatomică, formează partea ventrală a diencefalului. Toate creierele vertebratelor conțin un hipotalamus. La om, este de mărimea unei migdale.
Hipotalamusul este responsabil pentru reglarea anumitor procese metabolice și a altor activități ale sistemului nervos autonom. Acesta sintetizează și secretă anumiți neurohormoni, numiți hormoni de eliberare sau hormoni hipotalamici, care la rândul lor stimulează sau inhibă secreția de hormoni din glanda pituitară. Hipotalamusul controlează temperatura corpului, foamea, aspectele importante ale comportamentelor parentale și de atașament, sete, [2] oboseală, somn și ritmuri circadiene . [3]
Anatomie[modificare | modificare sursă]

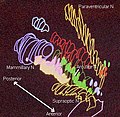
Hipotalamusul este împărțit în 3 regiuni (supraoptică, tuberală, mamilară) într-un plan parasagital, indicând localizarea anterior-posterioară; și 3 zone (periventriculară, medială, laterală) în planul coronal, indicând locația medial-laterală. Nucleii hipotalamici sunt localizați în aceste regiuni și zone specifice. [4] Se găsește în toate sistemele nervoase ale vertebratelor. La mamifere, celulele neurosecretorii magnocelulare din nucleul paraventricular și nucleul supraoptic al hipotalamusului produc hormonii neurohipofiziari, oxitocină și vasopresină. Acești hormoni sunt eliberați în sânge în hipofiza posterioară. [5] Celulele nevrosecretorii parvocelulare mult mai mici, neuronii nucleului paraventricular, eliberează hormonul care eliberează corticotropina și alți hormoni în sistemul portal hipofizar, unde acești hormoni se difuzează către hipofiza anterioară.
Nucleii[modificare | modificare sursă]
Nucleii hipotalamici includ următoarele: [6] [7] [8]
| Regiune | Zonă | Nucleu | Funcție [9] |
| Anterior (supraoptic) | Preoptic | Nucleul preoptic | |
| Medial | Nucleul preoptic medial |
| |
| Nucleul supraoptic |
| ||
| Nucleul paraventricular |
| ||
| Nucleul hipotalamic anterior |
| ||
| Nucleul suprachiasmatic | |||
| Lateral | |||
| Nucleul lateral | Vezi Lateral hypothalamus § Function - sursa primara de neuroni orexin care se proiecteaza in tot creierul si maduva spinarii | ||
| Mijlociu (tuberal) | Medial | Nucleul hipotalamic dorsomedial |
|
| Nucleul ventromedial |
| ||
| Nucleul arcuit |
| ||
| Lateral | Nucleul lateral | Vezi Lateral hypothalamus § Function - sursa primara de neuroni orexin care se proiecteaza in tot creierul si maduva spinarii | |
| Nucleii tuberali laterali | |||
| Posterior (mamilar) | Medial | Nucleii mamilari (parte a corpurilor mamilare ) | |
| Nucleul posterior |
| ||
| Lateral | Nucleul lateral | Vezi Lateral hypothalamus § Function - sursa primara de neuroni orexin care se proiecteaza in tot creierul si maduva spinarii | |
| Nucleul tuberomamilar [11] |
|
- Vezi și
- nucleul preoptic ventrolateral
- nucleul periventricular
-
Secțiunea transversală a hipotalamusului maimuței afișează două dintre nucleele majore hipotalamice de ambele părți ale celui de-al treilea ventricul plin de lichid.
-
Nucleii hipotalamici
-
Nucleii hipotalamici pe o parte a hipotalamusului, arătați într-o reconstrucție computerizată 3-D
Conexiuni[modificare | modificare sursă]
Hipotalamusul este puternic interconectat cu alte părți ale sistemului nervos central, în special trunchiul cerebral și formațiunea reticulară. Ca parte a sistemului limbic, are conexiuni cu alte structuri limbice, inclusiv amigdala și septumul, și este, de asemenea, conectat cu zone ale sistemului nervos autonom.
Hipotalamusul primește multe intrări din trunchiul cerebral, cele mai notabile din nucleul tractului solitar, locus coeruleus și medulla ventrolaterală.
Majoritatea fibrelor nervoase din hipotalamus au traseu în două moduri (bidirecționale):
- Proiecțiile către zonele caudale către hipotalamus trec prin planșeul median al creierului anterior, tractul mamilotegmental și fasciculul longitudinal dorsal.
- Proiecțiile către zonele rostrale către hipotalamus sunt efectuate de tractul mamilotalamic, fornix și stria terminală.
- Proiecțiile către zonele sistemului motor simpatic ( segmentele coloanei vertebrale laterale T1-L2 / L3) sunt purtate de tractul hipotalamospinal și activează calea motorie simpatică.
Dimorfism sexual[modificare | modificare sursă]
Mai mulți nuclei hipotalamici sunt dimorfici sexual; adică, există diferențe clare atât în structură, cât și în funcție între bărbați și femei. [12] Unele diferențe sunt evidente chiar și în neuroanatomia grosieră: cea mai notabilă este nucleul dimorf sexual din zona preoptică [12] în care diferențele sunt modificări subtile ale conectivității și sensibilității chimice a anumitor seturi de neuroni. Importanța acestor schimbări poate fi recunoscută prin diferențe funcționale între bărbați și femei. De exemplu, bărbații din majoritatea speciilor preferă mirosul și aspectul femelelor în locul bărbaților, care este esențial în stimularea comportamentului sexual masculin. Dacă nucleul dimorf sexual este lezat, această preferință pentru femei de către bărbați se diminuează. De asemenea, modelul de secreție a hormonului de creștere este dimorf sexual; [13] Acesta este motivul pentru care în multe specii, masculii adulți se disting vizibil de femele.
Sensibilitate la steroizii ovarieni[modificare | modificare sursă]
Alte dimorfisme funcționale izbitoare sunt în răspunsurile comportamentale la steroizii ovarieni ai adultului. Bărbații și femeile răspund la steroizi ovarieni în moduri diferite, parțial deoarece expresia neuronilor sensibili la estrogeni din hipotalamus este dimorfă sexual; adică, receptorii de estrogen sunt exprimați în diferite seturi de neuroni.
Estrogenul și progesteronul pot influența expresia genelor în special neuroni sau pot induce modificări ale potențialului membranei celulare și activării kinazei, ducând la diverse funcții celulare non-genomice. Estrogenul și progesteronul se leagă de receptorii lor de hormoni nucleari înrudiți, care se translocează în nucleul celular și interacționează cu regiuni ale ADN-ului cunoscute sub numele de elemente de răspuns hormonal (ERH) sau se leagă de locul de legare al unui alt factor de transcripție. S-a demonstrat că receptorul de estrogen (RE) transactivează alți factori de transcripție în acest mod, în ciuda absenței unui element de răspuns estrogen (ERE) în regiunea promotoră proximală a genei. În general, RE și receptorii de progesteron (RP) sunt activatori genetici, cu mARN crescut și sinteza proteinelor ulterioară după expunerea la hormoni.
Creierul masculin și cel feminin diferă în ceea ce privește distribuția receptorilor de estrogen și această diferență este o consecință ireversibilă a expunerii la steroizi neonatali. Receptorii de estrogen (și receptorii de progesteron) se găsesc în principal în neuronii din hipotalamusul anterior și mediubasal, în special:
- zona preoptică (unde sunt localizați neuronii LHRH, reglând răspunsurile dopaminei și comportamentul matern; [14]
- nucleul periventricular unde sunt localizați neuronii somatostatici, reglând nivelurile de stres; [15]
- hipotalamusul ventromedial care reglează foamea și excitația sexuală.
Dezvoltare[modificare | modificare sursă]
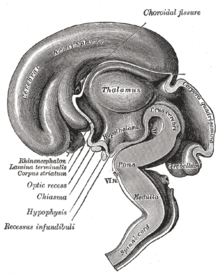
În viața neonatală, steroizii gonadici influențează dezvoltarea hipotalamusului neuroendocrin. De exemplu, ele determină capacitatea femelelor de a prezenta un ciclu reproductiv normal, iar a bărbaților și femelelor de a prezenta comportamente reproductive adecvate în viața adultă.
- Dacă un șobolan de sex feminin este injectat o dată cu testosteron în primele câteva zile de viață postnatală (în „perioada critică” de influență a steroizilor sexuali), hipotalamusul este ireversibil masculinizat; șobolanul adult va fi incapabil să genereze o creștere a LH ca răspuns la estrogen (o caracteristică a femelelor), dar va fi capabil să prezinte comportamente sexuale masculine (montând o femeie receptivă sexual). [16]
- Prin contrast, un șobolan mascul castrat chiar după naștere va fi feminizat, iar adultul va prezenta comportament sexual feminin ca răspuns la estrogen (receptivitate sexuală, comportament lordoză ). [16]
La primate, influența de dezvoltare a androgenilor este mai puțin clară, iar consecințele sunt mai puțin înțelese. În creier, testosteronul este aromatizat (până la estradiol ), care este principalul hormon activ pentru influențele de dezvoltare. Testiculul uman secretă niveluri ridicate de testosteron de la aproximativ săptămâna 8 a vieții fetale până la 5-6 luni de la naștere (o creștere similară a testosteronului perinatal se observă la multe specii), proces care pare să stea la baza fenotipului masculin. Estrogenul din circulația maternă este relativ ineficient, parțial din cauza nivelurilor circulante ridicate de proteine care leagă steroizii în timpul sarcinii. [16]
Steroizii sexuali nu sunt singurele influențe importante asupra dezvoltării hipotalamice; în special, stresul pre-pubertar la începutul vieții (al șobolanilor) determină capacitatea hipotalamusului adult de a răspunde la un factor de stres acut. [17] Spre deosebire de receptorii gonadici ai steroizilor, receptorii glucocorticoizi sunt foarte răspândiți în tot creierul; în nucleul paraventricular, ele mediază controlul feedback-ului negativ al sintezei și secreției CRF, dar în altă parte rolul lor nu este bine înțeles.
Funcție[modificare | modificare sursă]
Eliberarea hormonului[modificare | modificare sursă]
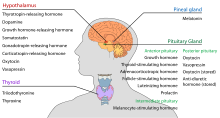
Hipotalamusul are o funcție neuroendocrină centrală, mai ales prin controlul său asupra hipofizei anterioare, care la rândul său reglează diferite glande și organe endocrine. Hormonii de eliberare (numiți și factori de eliberare) sunt produși în nuclei hipotalamici, apoi transportați de-a lungul axonilor fie la eminența mediană, fie la hipofiza posterioară, unde sunt depozitați și eliberați după cum este necesar. [18]
- Hipofiza anterioară
În axa hipotalamică-adenohipofizară, hormonii eliberatori, cunoscuți și sub denumirea de hormoni hipofiziotropi sau hipotalamici, sunt eliberați din eminența mediană, o prelungire a hipotalamusului, în sistemul portal hipofizar, care îi poartă către hipofiza anterioară, unde își exercită funcțiile de reglare. asupra secreției de hormoni adenohipofizari. [19] Acești hormoni hipofiziotropi sunt stimulați de celulele nevrosecretorii parvocelulare situate în zona periventriculară a hipotalamusului. După eliberarea lor în capilarele celui de-al treilea ventricul, hormonii hipofiziotropi călătoresc prin ceea ce este cunoscut sub numele de circulația portalului hipotalamo-hipofizar. Odată ce ajung la destinație în hipofiza anterioară, acești hormoni se leagă de receptori specifici localizați pe suprafața celulelor hipofizei. În funcție de celulele care sunt activate prin această legare, hipofiza fie va începe să secrete, fie va înceta să secrete hormoni în restul fluxului sanguin. [20]
| Hormonul secretat | Abreviere | Produs de | Efect |
|---|---|---|---|
| Hormon care eliberează tirotropina </br> (Hormonul care eliberează prolactina) |
TRH, TRF sau PRH | Celule neurosecretorii parvocelulare ale nucleului paraventricular | Stimulați eliberarea hormonului stimulator tiroidian (TSH) din hipofiza anterioară (în principal) </br> Stimulați eliberarea prolactinei din hipofiza anterioară |
| Hormonul care eliberează corticotropina | CRH sau CRF | Celule neurosecretorii parvocelulare ale nucleului paraventricular | Stimulați eliberarea hormonului adrenocorticotrop (ACTH) din hipofiza anterioară |
| Dopamina </br> (Hormonul inhibitor al prolactinei) |
DA sau PIH | Neuronii dopaminici ai nucleului arcuat | Inhibă eliberarea prolactinei din hipofiza anterioară |
| Hormon care eliberează hormonul de creștere | GHRH | Neuroni neuroendocrini ai nucleului Arcuate | Stimulați eliberarea hormonului de creștere (GH) din hipofiza anterioară |
| Hormonul care eliberează gonadotropina | GnRH sau LHRH | Celulele neuroendocrine din zona preoptică | Stimulați eliberarea hormonului foliculostimulant (FSH) din hipofiza anterioară </br> Stimulați eliberarea hormonului luteinizant (LH) din hipofiza anterioară |
| Somatostatină [21] </br> (hormon inhibitor al hormonului de creștere) |
SS, GHIH sau SRIF | Celulele neuroendocrine ale nucleului periventricular | Inhibați eliberarea hormonului de creștere (GH) din hipofiza anterioară </br> Inhibați (moderat) eliberarea hormonului stimulator tiroidian (TSH) din hipofiza anterioară |
Alți hormoni secretați din eminența mediană includ vasopresina, oxitocina și neurotensina . [22] [23] [24] [25]
- Hipofiza posterioară
În axul hipotalamic-neurohipofizar, hormonii neurohipofiziali sunt eliberați din hipofiza posterioară, care este de fapt o prelungire a hipotalamusului, în circulație.
| Hormonul secretat | Abreviere | Produs de | Efect |
|---|---|---|---|
| Oxitocina | OXY sau OXT | Celule neurosecretorii magnocelulare ale nucleului paraventricular și ale nucleului supraoptic | Contracția uterină </br> Alăptare (reflex de decădere) |
| Vasopresina </br> (hormon antidiuretic) |
ADH sau AVP | Celule neurosecretorii magnocelulare și parvocelulare ale nucleului paraventricular, celule magnocelulare din nucleul supraoptic | Creșterea permeabilității la apă a celulelor tubului distal și a canalului de colectare în rinichi și astfel permite reabsorbția apei și excreția de urină concentrată |
Se știe, de asemenea, că hormonii axei hipotalamo-hipofizo-suprarenale (HPA) sunt legați de anumite boli ale pielii și de homeostazia pielii. Există dovezi care leagă hiperactivitatea hormonilor HPA de bolile de piele legate de stres și tumorile pielii. [26]
Stimulare[modificare | modificare sursă]
Hipotalamusul coordonează multe ritmuri circadiene hormonale și comportamentale, modele complexe de ieșiri neuroendocrine , mecanisme homeostatice complexe și comportamente importante. Prin urmare, hipotalamusul trebuie să răspundă la multe semnale diferite, dintre care unele sunt generate extern și altele intern. Semnalizarea undei Delta care apare fie în talamus, fie în cortex influențează secreția de hormoni eliberatori; GHRH și prolactina sunt stimulate în timp ce TRH este inhibat.
Hipotalamusul răspunde la:
- Lumina: lungimea zilei și fotoperioada pentru reglarea ritmurilor circadiene și sezoniere
- Stimuli olfactivi, inclusiv feromoni
- Steroizi, inclusiv steroizi gonadici și corticosteroizi
- Informații transmise neuronal care apar în special din inimă, sistemul nervos enteric (al tractului gastrointestinal ), [27] și tractul reproductiv.
- Intrări autonome
- Stimuli transmisibili de sânge, inclusiv leptină, grelină, angiotensină, insulină, hormoni hipofizari, citokine, concentrații plasmatice de glucoză și osmolaritate etc.
- Stres
- Invadarea microorganismelor prin creșterea temperaturii corpului, resetarea termostatului corpului în sus.
Stimuli olfactivi[modificare | modificare sursă]
Stimulii olfactivi sunt importanți pentru reproducerea sexuală și funcția neuroendocrină la multe specii. De exemplu, dacă un șoarece însărcinat este expus la urina unui bărbat „ciudat” într-o perioadă critică după coit, atunci sarcina eșuează ( efectul Bruce ). Astfel, în timpul coitusului, o femelă de șoarece formează o „memorie olfactivă” precisă a partenerului ei care persistă câteva zile. Indicii feromonali ajută la sincronizarea estrului la multe specii; la femei, menstruația sincronizată poate apărea și din indicii feromonali, deși rolul feromonilor la om este contestat.
Stimuli transmisibili de sânge[modificare | modificare sursă]
Hormonii peptidici au influențe importante asupra hipotalamusului și, pentru a face acest lucru, trebuie să treacă prin bariera hematoencefalică . Hipotalamusul este delimitat parțial de regiuni specializate ale creierului care nu au o barieră hematoencefalică eficientă; endoteliul capilar din aceste locuri este fenestrat pentru a permite trecerea liberă chiar și a proteinelor mari și a altor molecule. Unele dintre aceste situri sunt siturile neurosecreției - neurohipofiza și eminența mediană . Cu toate acestea, altele sunt locuri în care creierul probează compoziția sângelui. Două dintre aceste situri, SFO ( organ subfornical ) și OVLT ( organum vasculosum al laminei terminale ) sunt așa-numitele organe circumventriculare, unde neuronii sunt în contact intim atât cu sângele, cât și cu LCR . Aceste structuri sunt dens vascularizate și conțin neuroni osmoreceptivi și receptivi la sodiu care controlează consumul de alcool, eliberarea de vasopresină, excreția de sodiu și pofta de sodiu. De asemenea, conțin neuroni cu receptori pentru angiotensină, factor natriuretic atrial, endotelină și relaxină, fiecare dintre aceștia fiind important în reglarea echilibrului fluidelor și electroliților. Neuronii din OVLT și SFO se proiectează către nucleul supraoptic și nucleul paraventricular și, de asemenea, către zonele hipotalamice preoptice. Organele circumventriculare pot fi, de asemenea, locul de acțiune al interleukinelor pentru a provoca atât febra, cât și secreția de ACTH, prin efecte asupra neuronilor paraventriculari.
Nu este clar cum toate peptidele care influențează activitatea hipotalamică câștigă accesul necesar. În cazul prolactinei și leptinei, există dovezi ale absorbției active a plexului coroid din sânge în lichidul cefalorahidian (LCR). Unii hormoni hipofizari au o influență de feedback negativ asupra secreției hipotalamice; de exemplu, hormonul de creștere se alimentează din nou cu hipotalamusul, dar modul în care acesta intră în creier nu este clar. Există, de asemenea, dovezi ale acțiunilor centrale ale prolactinei .
Rezultatele au sugerat că hormonul tiroidian (T4) este preluat de celulele gliale hipotalamice din nucleul infundibular / eminența mediană și că este convertit aici în T3 de deiodinaza de tip 2 (D2). Ulterior, T3 este transportat în neuronii producători de hormoni care eliberează tirotropina ( TRH ) din nucleul paraventricular . Receptorii hormonilor tiroidieni au fost găsiți în acești neuroni, indicând faptul că sunt într-adevăr sensibili la stimulii T3. În plus, acești neuroni au exprimat MCT8, un transportor de hormoni tiroidieni, susținând teoria că T3 este transportat în ei. T3 se poate lega apoi de receptorul hormonului tiroidian din acești neuroni și poate afecta producția de hormon care eliberează tirotropina, reglând astfel producția de hormon tiroidian. [28]
Hipotalamusul funcționează ca un tip de termostat pentru organism. [29] Stabilește temperatura corporală dorită și stimulează fie producția de căldură și retenția pentru a ridica temperatura sângelui la o setare mai mare, fie transpirația și vasodilatația pentru a răci sângele la o temperatură mai scăzută. Toate febrile rezultă dintr-un cadru ridicat în hipotalamus; temperaturile ridicate ale corpului datorate oricărei alte cauze sunt clasificate ca hipertermie . [29] Rareori, deteriorarea directă a hipotalamusului, cum ar fi un accident vascular cerebral, va provoca febră; aceasta se numește uneori febră hipotalamică . Cu toate acestea, este mai frecvent ca astfel de daune să provoace temperaturi anormal de scăzute ale corpului. [29]
Steroizi[modificare | modificare sursă]
Hipotalamusul conține neuroni care reacționează puternic la steroizi și glucocorticoizi - (hormonii steroizi ai glandei suprarenale, eliberați ca răspuns la ACTH ). De asemenea, conține neuroni specializați sensibili la glucoză (în nucleul arcuat și hipotalamusul ventromedial ), care sunt importanți pentru apetit . Zona preoptică conține neuroni termosensibili; acestea sunt importante pentru secreția de TRH.
Neural[modificare | modificare sursă]
Secreția de oxitocină ca răspuns la alăptarea sau stimularea vagino-cervicală este mediată de unele dintre aceste căi; secreția de vasopresină ca răspuns la stimulii cardiovasculari care decurg din chemoreceptori din corpul carotid și arcada aortică și din receptorii de volum atrial cu presiune scăzută este mediată de alții. La șobolan, stimularea vaginului provoacă, de asemenea , secreția de prolactină, ceea ce duce la pseudo-sarcină după o împerechere infertilă. La iepure, coitul provoacă ovulație reflexă. La ovine, stimularea cervicală în prezența unor niveluri ridicate de estrogen poate induce un comportament matern la o oaie virgină. Aceste efecte sunt toate mediate de hipotalamus, iar informațiile sunt purtate în principal de căile spinale care se retrag în trunchiul cerebral. Stimularea mameloanelor stimulează eliberarea de oxitocină și prolactină și suprimă eliberarea de LH și FSH .
Stimulii cardiovasculari sunt transportați de nervul vag . Vagul transmite, de asemenea, o varietate de informații viscerale, inclusiv de exemplu semnale care decurg din distensie gastrică sau golire, pentru a suprima sau promova hrănirea, prin semnalarea eliberării de leptină sau, respectiv, gastrină. Din nou, aceste informații ajung la hipotalamus prin relee în trunchiul cerebral.
În plus, funcția hipotalamică răspunde - și este reglementată de - nivelurile tuturor celor trei neurotransmițători clasici de monoamină, noradrenalină, dopamină și serotonină (5-hidroxitriptamină), în acele căi din care primește inervație. De exemplu, intrările noradrenergice care decurg din locus coeruleus au efecte de reglare importante asupra nivelului hormonului de eliberare a corticotropinei (CRH).
Controlul consumului de alimente[modificare | modificare sursă]
| Peptide care cresc </br> comportamentul alimentar |
Peptide care scad </br> comportamentul alimentar |
|---|---|
| Grelina | Leptina |
| Neuropeptida Y | (α, β, γ) - Hormoni care stimulează melanocitele |
| Peptida legată de Agouti | Peptide cu transcripție reglementate de cocaină și amfetamină |
| Orexine (A, B) | Hormonul care eliberează corticotropina |
| Hormon concentrator de melanină | Colecistochinina |
| Galanin | Insulină |
| Peptida asemănătoare glucagonului 1 |
Partea laterală extremă a nucleului ventromedial al hipotalamusului este responsabilă pentru controlul aportului alimentar. Stimularea acestei zone determină un aport crescut de alimente. Leziunea bilaterală a acestei zone determină încetarea completă a aportului de alimente. Părțile mediale ale nucleului au un efect de control asupra părții laterale. Leziunea bilaterală a părții mediale a nucleului ventromedial provoacă hiperfagie și obezitate la animal. O leziune ulterioară a părții laterale a nucleului ventromedial la același animal produce încetarea completă a aportului alimentar.
Există diferite ipoteze legate de această reglementare: [31]
- Ipoteza Lipostatic: Această ipoteză susține că adipos țesut produce un umoral semnal, care este proporțională cu cantitatea de grăsime și acționează asupra hipotalamusului pentru a reduce aportul de alimente și de ieșire creștere a energiei. A fost evident că un hormon leptină acționează asupra hipotalamusului pentru a reduce consumul de alimente și a crește puterea de energie.
- Ipoteza gutpeptidelor: hormonii gastro-intestinali precum Grp, glucagoni, CCK și alții au pretins că inhibă consumul de alimente. Mâncarea care intră în tractul gastro-intestinal declanșează eliberarea acestor hormoni, care acționează asupra creierului pentru a produce sațietate. Creierul conține atât receptori CCK-A, cât și receptori CCK-B.
- Ipoteza glucostatică: activitatea centrului de sațietate din nucleii ventromediali este probabil guvernată de utilizarea glucozei în neuroni. S-a postulat că, atunci când utilizarea glucozei este scăzută și, în consecință, atunci când diferența de glucoză din sânge arteriovenoasă între ei este scăzută, activitatea asupra neuronilor scade. În aceste condiții, activitatea centrului de hrănire este necontrolată și individul îi este foame. Aportul alimentar este crescut rapid prin administrarea intraventriculară de 2-dezoxiglucoză, scăzând astfel utilizarea glucozei în celule.
- Ipoteză termostatică: Conform acestei ipoteze, o scădere a temperaturii corpului sub un anumit set-point stimulează apetitul, în timp ce o creștere peste set-point inhibă apetitul.
Procesarea fricii[modificare | modificare sursă]
Zona medială a hipotalamusului face parte dintr-un circuit care controlează comportamentele motivate, cum ar fi comportamentele defensive. [32] Analizele etichetării Fos au arătat că o serie de nuclee din „coloana de control comportamental” este importantă în reglarea expresiei comportamentelor defensive înnăscute și condiționate. [33]
- Comportamentul defensiv antipredator
Expunerea la un prădător (cum ar fi o pisică) provoacă comportamente defensive la rozătoarele de laborator, chiar și atunci când animalul nu a fost niciodată expus unei pisici. [34] În hipotalamus, această expunere determină o creștere a celulelor marcate cu Fos în nucleul hipotalamic anterior, partea dorsomedială a nucleului ventromedial și în partea ventrolaterală a nucleului premamiliar (PMDvl). [35] Nucleul premamilar are un rol important în exprimarea comportamentelor defensive față de un prădător, deoarece leziunile din acest nucleu abolesc comportamentele defensive, cum ar fi înghețul și zborul. [35] [36] PMD nu modulează comportamentul defensiv în alte situații, deoarece leziunile acestui nucleu au avut efecte minime asupra scorurilor de înghețare post-șoc. [36] PMD are legături importante cu griul periaqueductal dorsal, o structură importantă în exprimarea fricii. [37] [38] În plus, animalele prezintă comportamente de evaluare a riscului față de mediul asociat anterior cu pisica. Analiza celulară marcată cu Fos a arătat că PMDvl este cea mai activată structură din hipotalamus, iar inactivarea cu muscimol înainte de expunerea la context elimină comportamentul defensiv. [35] Prin urmare, hipotalamusul, în principal PMDvl, are un rol important în exprimarea comportamentelor defensive înnăscute și condiționate față de un prădător.
- Înfrângerea socială
La fel, hipotalamusul are un rol în înfrângerea socială : nucleele din zona medială sunt mobilizate și în timpul unei întâlniri cu un specific agresiv. Animalul învins are o creștere a nivelurilor de Fos în structurile dimorfice sexual, cum ar fi nucleul pre-optic medial, partea ventrolaterală a nucleului ventromedial și nucleul premamilar ventral. [39] Astfel de structuri sunt importante în alte comportamente sociale, cum ar fi comportamentele sexuale și agresive. Mai mult, este mobilizat și nucleul premamilar, partea dorsomedială, dar nu partea ventrolaterală. [39] Leziunile din acest nucleu abolesc comportamentul defensiv pasiv, cum ar fi înghețarea și postura „pe spate”. [39]
Imagini suplimentare[modificare | modificare sursă]
-
Human brain left dissected midsagittal view
-
Location of the hypothalamus
Vezi si[modificare | modificare sursă]
- Copeptina
- Axa hipotalamo-hipofizo-suprarenală (axa HPA)
- Axa hipotalamică-hipofizară-gonadală (axa HPG)
- Axa hipotalamică-hipofizară-tiroidiană (axa HPT)
- Calea incertohipotalamică
- Neuroendocrinologie
- Neuroștiința somnului
Referințe[modificare | modificare sursă]
- ^ Dr. Boeree, C. George. „The Emotional Nervous System”. The Limbic System. Accesat în .
- ^ „NCI Dictionary of Cancer Terms”. National Cancer Institute.
- ^ Saper, Clifford B.; Scammell, Thomas E.; Lu, Jun (). „Hypothalamic regulation of sleep and circadian rhythms”. Nature (în engleză). 437 (7063): 1257–1263. Bibcode:2005Natur.437.1257S. doi:10.1038/nature04284. ISSN 1476-4687. PMID 16251950.
- ^ Inderbir Singh (septembrie 2011). Textbook of Anatomy: Volume 3: Head and Neck, Central Nervous System. JP Medical Ltd. pp. 1101–. ISBN 978-93-5025-383-0.
- ^ Melmed, S; Polonsky, KS; Larsen, PR; Kronenberg, HM (). Williams Textbook of Endocrinology (ed. 12th). Saunders. p. 107. ISBN 978-1437703245.
- ^ „Enlarged view of the hypothalamus”. psycheducation.org. Jim Phelps. Arhivat din original la . Accesat în .
- ^ „Diagram of Nuclei”. universe-review.ca. Accesat în .
- ^ „Emotion and the limbic system”. utdallas.edu. Lucien T. "Tres" Thompson, The University of Texas at Dallas. Accesat în .
- ^ Hall, John E.; Guyton, Arthur C. (). Guyton and Hall Textbook of Medical Physiology (ed. 12th). Saunders/Elsevier. ISBN 978-1416045748.
- ^ „Parallel preoptic pathways for thermoregulation”. The Journal of Neuroscience. 29 (38): 11954–64. septembrie 2009. doi:10.1523/JNEUROSCI.2643-09.2009. PMC 2782675
 . PMID 19776281.
. PMID 19776281.
- ^ „Chapter 6: Widely Projecting Systems: Monoamines, Acetylcholine, and Orexin”. Molecular Neuropharmacology: A Foundation for Clinical Neuroscience (ed. 2nd). New York: McGraw-Hill Medical. . pp. 175–176. ISBN 9780071481274.
Within the brain, histamine is synthesized exclusively by neurons with their cell bodies in the tuberomammillary nucleus (TMN) that lies within the posterior hypothalamus. There are approximately 64000 histaminergic neurons per side in humans. These cells project throughout the brain and spinal cord. Areas that receive especially dense projections include the cerebral cortex, hippocampus, neostriatum, nucleus accumbens, amygdala, and hypothalamus. ... While the best characterized function of the histamine system in the brain is regulation of sleep and arousal, histamine is also involved in learning and memory ... It also appears that histamine is involved in the regulation of feeding and energy balance.
- ^ a b „The sexually dimorphic nucleus of the preoptic area in the human brain: a comparative morphometric study”. Journal of Anatomy. 164: 55–72. iunie 1989. PMC 1256598
 . PMID 2606795.
. PMID 2606795.
- ^ „Neural growth hormone: regional regulation by estradiol and/or sex chromosome complement in male and female mice”. Biology of Sex Differences. 6: 8. . doi:10.1186/s13293-015-0026-x. PMC 4434521
 . PMID 25987976.
. PMID 25987976.
- ^ „Luteinizing hormone-releasing hormone distribution in the anterior hypothalamus of the female rats”. ISRN Anatomy. 2013: 1–6. . doi:10.5402/2013/870721. PMC 4392965
 . PMID 25938107.
. PMID 25938107.
- ^ „Estrogen receptor beta in the paraventricular nucleus of hypothalamus regulates the neuroendocrine response to stress and is regulated by corticosterone”. Neuroscience. 121 (4): 837–45. . doi:10.1016/S0306-4522(03)00561-X. PMID 14580933.
- ^ a b c „Sex differences in the brain: the not so inconvenient truth”. The Journal of Neuroscience. 32 (7): 2241–7. februarie 2012. doi:10.1523/JNEUROSCI.5372-11.2012. PMC 3295598
 . PMID 22396398.
. PMID 22396398.
- ^ „Stress history and pubertal development interact to shape hypothalamic-pituitary-adrenal axis plasticity”. Endocrinology. 147 (4): 1664–74. aprilie 2006. doi:10.1210/en.2005-1432. PMID 16410296.
- ^ Bowen, R. „Overview of Hypothalamic and Pituitary Hormones”. Accesat în .
- ^ „Disorders of the anterior pituitary and hypothalamus”. Harrison's Principles of Internal Medicine (ed. 16th). New York, NY: McGraw-Hill. . pp. 2076–97. ISBN 978-0-07-139140-5.
- ^ „Hypothalamic Control of the Anterior Pituitary”. Neuroscience: Exploring the Brain (ed. 4th). Philadelphia: Wolters Kluwer. . p. 528. ISBN 978-0-7817-7817-6.
- ^ „Pituitary somatostatin receptor signaling”. Trends in Endocrinology and Metabolism. 21 (3): 123–33. martie 2010. doi:10.1016/j.tem.2009.12.003. PMC 2834886
 . PMID 20149677.
. PMID 20149677.
- ^ „Oxytocin and vasopressin in rat hypophysial portal blood: experimental studies in normal and Brattleboro rats”. The Journal of Endocrinology. 104 (2): 211–24. februarie 1985. doi:10.1677/joe.0.1040211. PMID 3968510.
- ^ „Distribution of orexin/hypocretin in the rat median eminence and pituitary”. Brain Research. Molecular Brain Research. 76 (1): 1–6. martie 2000. doi:10.1016/s0169-328x(99)00317-4. PMID 10719209.
- ^ „In vivo release of neurotensin from the median eminence of ovariectomized estrogen-primed rats as estimated by push-pull perfusion: correlation with luteinizing hormone and prolactin surges”. Neuroendocrinology. 57 (4): 760–4. aprilie 1993. doi:10.1159/000126434. PMID 8367038.
- ^ „Orexins in the regulation of the hypothalamic-pituitary-adrenal axis”. Pharmacological Reviews. 58 (1): 46–57. martie 2006. doi:10.1124/pr.58.1.4. PMID 16507882.
- ^ Jung Eun Kim; Baik Kee Cho; Dae Ho Cho; Hyun Jeong Park (). „Expression of Hypothalamic-Pituitary-Adrenal Axis in Common Skin Diseases: Evidence of its Association with Stress-related Disease Activity”. National Research Foundation of Korea. Accesat în .
- ^ „Gut feelings: the emerging biology of gut-brain communication”. Nature Reviews. Neuroscience. 12 (8): 453–66. iulie 2011. doi:10.1038/nrn3071. PMC 3845678
 . PMID 21750565.
. PMID 21750565.
- ^ „Functional neuroanatomy of thyroid hormone feedback in the human hypothalamus and pituitary gland”. Molecular and Cellular Endocrinology. 251 (1–2): 1–8. iunie 2006. doi:10.1016/j.mce.2006.03.042. PMID 16707210.
- ^ a b c Fauci, Anthony (). Harrison's Principles of Internal Medicine (ed. 17). McGraw-Hill Professional. pp. 117–121. ISBN 978-0-07-146633-2. Parametru necunoscut
|arată-autori=ignorat (ajutor) - ^ „Chapter 10: Neural and Neuroendocrine Control of the Internal Milieu – Table 10:3”. Molecular Neuropharmacology: A Foundation for Clinical Neuroscience (ed. 2nd). New York: McGraw-Hill Medical. . p. 263. ISBN 9780071481274.
- ^ „Anorexia-producing intermediary metabolites”. The American Journal of Clinical Nutrition. 29 (5): 552–8. mai 1976. doi:10.1093/ajcn/29.5.552. PMID 178168.
- ^ „Cerebral hemisphere regulation of motivated behavior”. Brain Research. 886 (1–2): 113–164. decembrie 2000. doi:10.1016/S0006-8993(00)02905-X. PMID 11119693.
- ^ Canteras, N.S. (). „The medial hypothalamic defensive system:Hodological organization and functional implications”. Pharmacology Biochemistry and Behavior. 71 (3): 481–491. doi:10.1016/S0091-3057(01)00685-2. PMID 11830182.
- ^ „An alternative experimental procedure for studying predator-related defensive responses”. Neuroscience and Biobehavioral Reviews. 29 (8): 1255–63. . doi:10.1016/j.neubiorev.2005.04.006. PMID 16120464.
- ^ a b c „Hypothalamic sites responding to predator threats--the role of the dorsal premammillary nucleus in unconditioned and conditioned antipredatory defensive behavior”. The European Journal of Neuroscience. 28 (5): 1003–15. septembrie 2008. doi:10.1111/j.1460-9568.2008.06392.x. PMID 18691328.
- ^ a b Blanchard, D.C. (). „Dorsal premammillary nucleus differentially modulates defensive behaviors induced by different threat stimuli in rats”. Neuroscience Letters. 345 (3): 145–148. doi:10.1016/S0304-3940(03)00415-4. PMID 12842277.
- ^ „The dorsal premammillary nucleus: an unusual component of the mammillary body”. Proceedings of the National Academy of Sciences of the United States of America. 89 (21): 10089–93. noiembrie 1992. Bibcode:1992PNAS...8910089C. doi:10.1073/pnas.89.21.10089. PMC 50283
 . PMID 1279669.
. PMID 1279669.
- ^ „Functional characteristics of the midbrain periaqueductal gray”. Progress in Neurobiology. 46 (6): 575–605. august 1995. doi:10.1016/0301-0082(95)00009-K. PMID 8545545.
- ^ a b c „Dissecting the brain's fear system reveals the hypothalamus is critical for responding in subordinate conspecific intruders”. Proceedings of the National Academy of Sciences of the United States of America. 106 (12): 4870–5. martie 2009. Bibcode:2009PNAS..106.4870M. doi:10.1073/pnas.0900939106. PMC 2660765
 . PMID 19273843.
. PMID 19273843.
Lecturi suplimentare[modificare | modificare sursă]
- „Sex differences in the brain: the relation between structure and function”. Hormones and Behavior. 55 (5): 589–96. mai 2009. doi:10.1016/j.yhbeh.2009.03.012. PMC 3932614
 . PMID 19446075.
. PMID 19446075.
Legături externe[modificare | modificare sursă]
- Stained brain slice images which include the "Hypothalamus"
- Hipotalamusul și hipofiza la endotexts.org
- Căutare NIF - Hipotalamus prin intermediul cadrului de informare a neuroștiințelor
- Diagramele de umplere a spațiului și secțiunile transversale ale nucleilor hipotalamici: hipotalamusul drept, anterior, tubular, posterior .
| |||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||