Dimorfism sexual

Dimorfismul sexual reprezintă diferența fenotipică între masculul și femela aceleiași specii. Diferențele pot fi morfologice, ornamentale sau comportamentale.
Exemple[modificare | modificare sursă]




Ornamentație / culori[modificare | modificare sursă]
O formă comună de dimorfism este ornamentația. Unul din sexe are culori mai saturate.[1] Trăsaturi exagerate sunt folosite în special în competiția pentru un partener.[2] Ornamentele sunt costisitoare ca producție și mantenanță.[3][4][5]. Un exemplu foarte bun este păunul, care dezvoltă un penaj foarte bogat pentru a atrage și curta femela, dar îngreunează zborul și limitează abilitatea acestuia de a scăpa de prădători. Fiind atât de puternic colorat, camuflarea este dificilă.
Alt exemplu de dicromatism sexual este vrabia albastră. Masculii sunt mai galbeni decât femelele, se pare ca efect a consumului unei larve lepidoptere care conține cantități mari de carotenoide și zeaxanthin.[6] Această dieta rezultă într-un penaj de o culoare albastră dintr-o zona invizibilă pentru ochiul uman a spectrului, dar vizibilă pentru femele.[7][8] În alte cuvinte, deși ne par galbene aceste vrăbii au un penaj albastru mai mult sau mai puțin intens, ca indicator a cantității de carotenoid consumate, și indirect a abilităților de a găsi mâncare.[1][9] Carotenoidele joaca un rol important în dezvoltare funcțiilor imune la mai multe specii animale.
În multe cazuri, femelele preferă caracteristici sexuale secundare exagerate când aleg un partener (Ryan and Rand, 1993),[2] discriminând masculii cu culori terne.[10] Există o teorie a ornamentației care definește că evoluția speciei se bazează în preferințele discriminatorii ale femelei în alegerea partenerului.
Specii cu femele mai mari decât masculii[modificare | modificare sursă]
În anumite specii de insecte, paianjeni, anumiți pești, păsări de pradă și anumite mamifere precum hiena sau balena albastră, femela este mai mare decât masculul.[11] În anumite specii femelele sunt sedentare și rar distribuite, iar masculuii au sarcina de a le găsi. Vollrath și Parker argumentează că această diferentă de comportament rezultă în diferențe de selecție între sexe, favorizănd evident masculii mai mici.[11]
Un exemplu de dimorfism sexual de mărime este liliacul Myotis nigricans. În această specie, femelele sunt mult mai mari decăt masculii, diferind în greutate corporală, dimensiuni craniale și lungimea antebrațelor.[12] Diferența de mărime se crede ca se datorează selecției naturale pe care o au femelele mai mare ca fecunditate. Femelele suportă costul energetic de a produce ouă care este mult mai mare decât costul energetic al mascului care produce sperma. Avantajul fecundității spune că o femelă mai mare poate produce mai mulți urmași și le poate oferi acestora condiții mai bune de supraviețuire. Acest fapt este valid pentru majoriatea ectotermelor. Alt motiv pentru care se crede ca femelele sunt mai mari este datorită faptului că acestea oferă îngrijire un timp urmașilor până aceștia se maturizează Timpul de gestație și lactație este foarte lung pentru M. nigricans, femelele alăptând progeniturile păna aproape la vârsta adultă.[13] Nu ar fi cababile sa zboare și să prinda prada daca nu ar compensa cpentru masa adițională a puilui. Ca adăugare la ipoteza care explica avantajele unei femele mari, există ipoteza paralelă ca un mascul de mici dimensiuni este o adaptare a masculilor care crește manevrabilitatea și agilitatea, în competiția contra femelelor pentru mâncare și alte resurse.

Anumite specii de pește pescar prezintă dimorfism sexual extrem. Femele au o aparență normală, dar masculii sunt creaturi rudimentare cu sisteme digestive minimale. Un mascul trebuie să găsească o femelă și să se unească cu ea, trăind parazitic, și fiind aproape doar un organism care produce spermă. O situație similară se întâlnește la gândacul de apă Zeus Phoreticovelia disparata, unde femela are o zonp galndulară pe spate prin care hrănește masculul care este agățat de ea. Masculii pot supraviețui și separați de femele, dar în general nu trăiesc singuri.[14]
Diferențe psihologice și de comportament[modificare | modificare sursă]
Diferențierea indusă de către cantitatea de hormoni sexuali a fost demostrată experimental pe mai multe animale. La anumite mamifere, comportamente adulte sexuale pot fi modificate prin suplimentarea sau depravarea de hormoni androgeni la nivel fetal sau în periada infantilă, chiar dacă nivelele la adult sunt normale.
Evoluția dimorfismului sexual[modificare | modificare sursă]
În 1871 Charles Darwin a emis teoria selecției sexuale, care conectează dimorfismul sexual selecția sexuală. În mai multe specii non monogame reprezintă un beneficiu pentru mascul în a se cupla cu cât mai multe femele, însă acest beneficiu este mic sau inexistent pentru femele.[15] Pentru aceste specii exită o presiune a selecției pentru orice trăsături care îl ajută pe mascul în a avea cât mai multe partenere, și ca urmare masculii se diferențiază de femele.

Aceste trăsături sunt cele care ii permit să câștige controlul asupra unui teritoriu sau asupra unui harem.[16][17][18]
Femelele pot alege masculi care dau impresia de puternici și sănătoși, având astfel gene bune și dând naștere unor progenituri sănătoase.[19] Cu toate acestea, în anumite specii femele nu aleg neapărat trăsături conectate cu rata de supraviețuire, precum coada păunului, care are un potențial de a reduce această rată.[18] Doua teorii pentru a explica acest fapt sunt ipoteza fiului frumos și principiul handicapului.
Ipoteza fiului frumos argumentează ca femelele aleg o anumită trăsătură datorită faptului că această trăsătura va incrementa șansele de succes ale progeniturilor, chiar dacă aceasta este detrimentală individual. Progeniturile care nu vor fi interesante pentru femele nu se vor reproduce.[20]
Principiul handicapului susține că dacă un mascul supraviețuiește având un handicap, în cazul păunului o coadă care îi împiedică fuga, dovedește că genele sale sunt „bune”. Dacă masculii cu gene „rele” nu ar supraviețuii handicapului, femelele ar evolua în a alege masculi cu acest tip de handicap, această trăsătură acționând ca un semnal de succes.[21]
Dimorfism sexual la mamifere și păsări[modificare | modificare sursă]
Creierul multor specii de păsări și mamifere, incluzând oamenii, este semnificativ diferit între mascul și femelă.[22] Atăt genele cât și hormonii afectează formarea creierului animal înainte de naștere sau de eclozare. Hormonii afectează semnificativ formarea creierului, precum și dezvoltarea acestui la pubertate. Un articol din 2004 Nature Reviews Neuroscience notează că „datorită faptului că este mai ușor să manipulezi nivelul de hormoni decăt valorile genelor și cromozomilor care influențează sexul, efectele hormonilor au fost studiate mai intensiv și sunt mai bine înțelese, decât acțiunea directă asupra creierului a genelor sexuale”. Articolul concluzionează că „în timp ce efectele diferențiate ale secrețiilor gonadelor pare a fi dominant, diferențele genelor care contribuie la diferențele sexuale în creier contribuie semnificativ”.[23]
Oameni[modificare | modificare sursă]
 | |
 |
 |
|
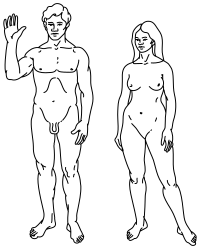
Top: Ilustrație stilizată reprezentănd dimorfismul sexual uman pe placa Pioneer.
| |
Dimorfismul sexual la oameni este un subiect controversat, în special când se trece de la diferențele fizice la abilități mentale sau la diferențe psihologice. (Pentru discuție vezi sex și psihologie, gen, și transgenic.) Diferențe evidente între bărbați și femei includ toate caracteristicile relaționate cu sistemul reproductiv, în special sistemul hormonal endocrin, încluzând efectele psihologice și de comportament. Diferențe sexuale nedisputate includ diferențierea gonadelor și a aparatului sexual intern și extern, diferențe ale pieptului, ale masei musculare, de înălțime și ale părului. În exterior, cel mai pronunțat dimorfism sexual este pieptul, partea inferioară a feței și zona dintre centură și genunchi.[24][25][26]
Rata metabolică basică este cu 6% mai mare la adolescenți bărbați decât la femei și crește la aproximativ 10% după pubertate. Femeile au tendința de a transforma o mai mare parte de hrană în grăsime, în timp ce bărbații transformă mai mult în mușchi și în rezerve circulatorii de energie. Femeile (în medie) sunt în proporție de 52% de puternice ca bărbații în partea superioară a corpului și, în jur de 66% în partea inferioară .[27] Bărbații în medie au oase mai dense și mai rezistente, la fel pentru tendoane și ligamente. Bărbații disipă căldură mai rapid decât femeile prin intermediul glandelor sudoripare[necesită citare]. Femeile au o protecție mai mare și rezerve mai mari de energie stocate în țesutului adipos subcutanat, absorbind mai puțină caldură exotermică, și reținând mai multă caldură endotermică.[necesită citare]
Bărbații au trahee și bronhii mai mari, până la 30% mai mult volum în plămâni raportat la masa corpului. Au o inimă mai mare, 10% mai multe celule roșii, un nivel mai ridicat de hemoglobină, și implicit o capacitate mai mare de asimilare a oxigenului. De asemenea au un număr mai mare de factori de coagulare, vitamina K, protrombină și trombocite. Aceste diferențe rezultă într-o capacitate mai mare de vindecare a rănilor și o toleranță mai mare la durere periferică.[28]
Femeile au mai multe celule albe (atât stocate cât și în circulație), mai multe granulocite și limfocite B și T. De asemenea ele produc mai mulți anticorpi și într-un ritm mai accelerat. Din această cauză dezvoltă mai puține boli și sucumbă acestora mai puțin timp.[28] Etologii argumentează că femelele, datorită faptului că interacționează cu alte femele și cu copii în grupuri sociale, au beneficiat de o selecție naturală.[29][30][31][32][33]
Anumiți biologi argumentează că gradul de dimorfism sexual al unei specii este invers proporțional cu gradul de grija maternală/paternală. Specii cu un grad ridicat de dimorfism, precum fazanul, tind să fie specii în care grija puilor este responsabilitatea exclusivă a mamei, cu foarte puțină participare a tatălui.[necesită citare].
Păsări[modificare | modificare sursă]

Dimorfismul sexual se poate manifesta la păsări în diferențe de mărime sau de penaj. Diferențele de mărime variază între specii, dar nu sunt regulă, în general păsările de pradă sau anumite specii de păsări nezburătoare nefiind diferențiate.[34] Diferențele de penaj, ca ornamentație sau culoare, de asemenea variază, dar în general masculii sunt mai ornamentați și prezintă culori mai vii.[35] Astfel de diferențe au fost atribuite contribuțiilor inegale din partea partenerilor sexuali.[36] În anumite specii, contribuția mascului se termină la sfârșitul copulării, în timp ce la alte specii mascului îngrijește urmașii. Diferitele forme de penaj au evoluat pentru a reflecta aceste diferențe și alte măsuri a valorii reproductive, cum ar fi condiția fizică[37] sau supravietuirea.[38] Fenotipul masculin trimite semnale femelei, care apoi alege cel mai „potrivit” mascul disponibil.
Dimorfismul sexual este un rezultat al selecției genetice, dar depinde și de mediul înconjurător. Un exemplu de polimorfism sexual determinat de mediu este Carpodacus mexicanus. Masculii acestei specii pot fi clasificați în trei categorii în timpul sezonului de împerechere: negrii, maron și sub-maron.[37] Aceste diferențe apar ca răspuns la starea de sănătate a păsării: dacă pasărea este sănătoasă va produce mai mulți hormoni androgeni devenind negre, în timp ce păsările mai puțin sănătoase produc mai puțini hormoni devenind maron.[37] Succesul reproductiv al masculilor este astfel determinat de nivelul de succes avut în afara sezonului de împerechere, variând anual în funcțiile de condițiile de mediu.
Dimorfismul sexual este controlat prin selecție naturală și selecție sexuală. De exemplu, dimorfismul sexual în culoare crește vulnerabilitatea în fața predatorilor.[39] De asemenea, energia necesară producerii de ornamente exagerate este un cost pentru masculi, regăsit în diminuarea imunității.[37] Atât timp cât beneficiile reproductive ale trăsături dimorfice este mai mare decât costul impus prin selecția naturală trasăturile se vor propaga în întreaga populație. Beneficiile reproductive se manifestă printr-un număr mare de urmași, iar selecția naturală impune costuri sub formă de supraviețuire redusă. Acest lucru înseamnă că dacă trasătura cauzează moartea prematură a masculilor aceasta este promovată atât timp căt trăsătura va produce mai mulți urmași decât numărul celor fără trăsătură. Adesea diferențele de formă sau de rol reproductiv cauzează diferențe de comportament. Masculii și femelele au roluri diferite în procesul reproductiv. Compartamentul de curtare și de reproducere al masculilor este regulat în mare măsură de hormoni.[40] Hormonii apar la pubertate și continuă să activeze anumite comportamente când este nevoie de-a lungul maturității, precum teritorialitatea în timpul sezonului de împerechere.[40] Hormoni organizaționali apar doar în timpul unei faze critice în dezvoltarea timpurie, chiar inainte sau imediat după eclozare, determinând modificări de comportament pe întreaga durată a vieții păsării.[40] Aceste diferențe de comportament pot cauza sensibilități disproporționate datorită presiunii antropogenice.[41] Femelele speciei Saxicola rubetra din Elveția se reproduc în zone cu ierburi.[41] Daca iarba este cosită la începutul sezonului de împerechere, acesta rezultă în mai multe morți de femele.[41] Populațiile multor specii de păsări sunt adeasea predominant mascului, iar dacă diferențele sexuale de comportament cresc această proporție populația generala suferă un declin rapid.[41]
În consecință, dimorfismul sexual are importanță în conservarea speciilor. Diferențele de formă și comportament pot rezulta în segregare sexuală.[42] Cele mai investigate cazuri de dimorfism sexual continuă să fie copitatele,[42] dar și liliecii,[43] canguri,[44] și păsările.[45] Planuri de conservare au fost create, specifice pentru speciile cu puternica segregare sexuală.[43]
Pești[modificare | modificare sursă]
Există cazuri în care masculii sunt mult mai mari decât femelele. Un exemplu este Lamprologus callipterus, o specie de ciclide în care masculul este de pâna la 60 de ori mai mare decat femela. Se crede că masculul este mai mare deoarece acesta are rolul de a găsi și a apăra cochilii de melci în care femela depune ouălele.[46] Masculii mari și puternici pot găsi si apăra cele mai mari cochilii, iar femelele rămân mici pentru a putea intra în cochilii pentru a depune icrele.[47] Așadar, creșterea în dimensiuni a femelei este limitată , femela reglăndu-și rata de creștere în funcție de dimensiunile cochiliei disponibile.[48]
Dimorfismul sexual apara și în cazul peștilor hermafrodiți. Aceste specii sunt cunoscute ca hermafrodite secvențiale.[49] În sistemele în care un mascul se împerecheaza cu mai multe femele, mărimea masculului joacă un rol important în succesul reproductiv.[50][51]
Vezi și[modificare | modificare sursă]
- Caracteristici sexuale primare
- Caracteristici sexuale secundare
- Principiul lui Bateman
- Proporția degetelor
- Diferențe de gen
- Intersex
- Diferențiere sexuală
- Reproducere sexuată
- Selecție sexuată
- Gene sexuale
Referințe[modificare | modificare sursă]
- ^ a b A. Johnsen, K. Delhey, S. Andersson & B. Kempenaers (). „Plumage colour in nestling blue tits: sexual dichromatism, condition dependence and genetic effects” (PDF). Proceedings of the Royal Society B. 270 (1521): 1263–1270. doi:10.1098/rspb.2003.2375. JSTOR 3558810. PMC 1691364
 . PMID 12816639.
. PMID 12816639.
- ^ a b Andersson 1994.
- ^ Amotz Zahavi (). „Mate selection – a selection for a handicap” (PDF). Journal of Theoretical Biology. 53 (1): 205–214. doi:10.1016/0022-5193(75)90111-3. PMID 1195756.
- ^ Andersson, 1986
- ^ Grafen, 1990
- ^ Slagsvold and Litfeld, 1985[necesită citare]
- ^ Andersson, 1998[necesită citare]
- ^ Hunt, 1998[necesită citare]
- ^ Senar, 2002[necesită citare]
- ^ S. A. Collins & S. T. Luddem (). „Degree of male ornamentation affects female preference for conspecific versus heterospecific males” (PDF). Proceedings of the Royal Society B. 269 (1487): 111–117. doi:10.1098/rspb.2001.1864. JSTOR 3067942. PMC 1690881
 . PMID 11798425.
. PMID 11798425.
- ^ a b Fritz Vollrath & Geoff A. Parker (). „Sexual dimorphism and distorted sex ratios in spiders”. Nature. 360 (6400): 156–159. Bibcode:1992Natur.360..156V. doi:10.1038/360156a0.
- ^ R. I. Bornholdt, L. R. Oliveira & M. E. Fabián (). „Sexual size dimorphism in Myotis nigricans (Schinz, 1821) (Chiroptera: Vespertilionidae) from south Brazil” (PDF). Brazilian Journal of Biology. 68 (4): 897–904. doi:10.1590/S1519-69842008000400028. PMID 19197511.
- ^ Virginia Hayssen & T. H. Kunz (). „Allometry of litter mass in bats: comparisons with maternal size, wing morphology, and phylogeny” (PDF). Journal of Mammalogy. 77 (2): 476–490. JSTOR 1382823.
- ^ Göran Arnqvist, Therésa M. Jones & Mark A. Elgar (). „Insect behaviour: reversal of sex roles in nuptial feeding” (PDF). Nature. 424 (6947): 387. Bibcode:2003Natur.424..387A. doi:10.1038/424387a. PMID 12879056. Arhivat din original (PDF) la . Accesat în .
- ^ Futuyma 2005, p. 330.
- ^ Futuyma 2005, p. 331.
- ^ Futuyma 2005, p. 332.
- ^ a b Ridley 2004, p. 328.
- ^ Futuyma 2005, p. 335.
- ^ Ridley 2004, p. 330.
- ^ Ridley 2004, p. 332.
- ^ Robert W. Goy and Bruce S. McEwen (). Sexual Differentiation of the Brain: Based on a Work Session of the Neurosciences Research Program. Boston: MIT Press. ISBN 978-0-262-57207-1. Arhivat din original la . Accesat în .
- ^ Arthur P. Arnold (). „Sex chromosomes and brain gender”. Nature Reviews Neuroscience. 5 (9): 701–708. doi:10.1038/nrn1494. PMID 15322528.
- ^ Gray 1918[necesită citare]
- ^ Nowell 1926[necesită citare]
- ^ Green 2000[necesită citare]
- ^ A. E. J. Miller, J. D. MacDougall, M. A. Tarnopolsky & D. G. Sale (). „Gender differences in strength and muscle fiber characteristics”. European Journal of Applied Physiology and Occupational Physiology. 66 (3): 254–262. doi:10.1007/BF00235103. PMID 8477683.
- ^ a b Alfred Glucksman (). Sexual Dimorphism in Human and Mammalian Biology and Pathology. Academic Press. pp. 66–75. ISBN 978-0-12-286960-0. OCLC 7831448.
- ^ Jo Durden-Smith & Diane deSimone (). Sex and the Brain. New York: Arbor House. ISBN 978-0-87795-484-2.
- ^ Eileen S. Gersh & Isidore Gersh (). Biology of Women. Baltimore: University Park Press. ISBN 978-0-8391-1622-6. LCCN 80-025534. OCLC 6914860.
- ^ Jay H. Stein (). Internal Medicine (ed. 2nd). Boston: Little, Brown. ISBN 978-0-316-81236-8.
- ^ M. McLaughlin & T. Shryer (). „Men vs women: the new debate over sex differences”. U.S. News & World Report: 50–58.
- ^ B. S. McEwen (). „Neural gonadal steroid actions”. Science. 211 (4488): 1303–1311. doi:10.1126/science.6259728. PMID 6259728.
- ^ Andersson 1994, p. 269.
- ^ K. J. McGraw, G. E. Hill, R. Stradi & R. S. Parker (). „The effect of dietary carotenoid access on sexual dichromatism and plumage pigment composition in the American goldfinch” (PDF). Comparative Biochemistry and Physiology Part B-Biochemistry and Molecular Biology. 131 (2): 261–269. doi:10.1016/S1096-4959(01)00500-0. Arhivat din original (PDF) la . Accesat în .
- ^ I. P. F. Owens & I. R. Hartley (). „Sexual dimorphism in birds: why are there so many different forms of dimorphism?”. Proceedings of the Royal Society B. 265 (1394): 397–407. doi:10.1098/rspb.1998.0308. JSTOR 50849. PMC 1688905
 .
.
- ^ a b c d Willow R. Lindsay, Michael S. Webster, Claire W. Varian & Hubert Schwabl (). „Plumage colour acquisition and behaviour are associated with androgens in a phenotypically plastic bird”. Animal Behaviour. 77 (6): 1525–1532. doi:10.1016/j.anbehav.2009.02.027.
- ^ Marion Petrie (). „Improved growth and survival of offspring of peacocks with more elaborate trains” (PDF). Nature. 371 (6498): 598–599. doi:10.1038/371598a0.
- ^ Anders Pape Møller & Jan Tøttrup Nielsen (). „Prey vulnerability in relation to sexual coloration of prey” (PDF). Behavioral Ecology and Sociobiology. 60 (2): 227–233. doi:10.1007/s00265-006-0160-x.[nefuncțională]
- ^ a b c Elizabeth Adkins-Regan (). „Hormones and the development of sex differences in behavior”. Journal of Ornithology. 148 (Supplement 1): S17–S26. doi:10.1007/s10336-007-0188-3.
- ^ a b c d Martin U. Grüebler, Heidi Schuler, Mathis Müller, Reto Spaar, Petra Horch & Beat Naef-Daenzer (). „Female biased mortality caused by anthropogenic nest loss contributes to population decline and adult sex ratio of a meadow bird”. Biological Conservation. 141 (12): 3040–3049. doi:10.1016/j.biocon.2008.09.008.
- ^ a b Martin B. Main (). „Reconciling competing ecological explanations for sexual segregation in ungulates”. Ecology. 89 (3): 693–704. doi:10.1890/07-0645.1. PMID 18459333.
- ^ a b Kamran Safi, Barbara König & Gerald Kerth (). „Sex differences in population genetics, home range size and habitat use of the parti-colored bat (Vespertilio murinus, Linnaeus 1758) in Switzerland and their consequences for conservation”. Biological Conservation. 137 (1): 28–36. doi:10.1016/j.biocon.2007.01.011.
- ^ G. Coulson, A. M. MacFarlane, S. E. Parsons & J. Cutter (). „Evolution of sexual segregation in mammalian herbivores: kangaroos as marsupial models” (PDF). Australian Journal of Zoology. 54 (3): 217–224. doi:10.1071/ZO05062.
- ^ Jacob González-Solís, John P. Croxall & Andy G. Wood (). „Sexual dimorphism and sexual segregation in foraging strategies of northern giant petrels, Macronectes halli, during incubation”. Oikos. 90 (2): 390–398. doi:10.1034/j.1600-0706.2000.900220.x.
- ^ Kazutaka Ota, Masanori Kohda & Tetsu Sato (). „Unusual allometry for sexual size dimorphism in a cichlid where males are extremely larger than females”. Journal of Biosciences. 35 (2): 257–265. doi:10.1007/s12038-010-0030-6.
- ^ Sato, 1994[necesită citare]
- ^ Dolores Schütz & Michael Taborsky (). „Mate choice and sexual conflict in the size dimorphic water spider Argyroneta aquatica (Araneae: Argyronetidae)” (PDF). Journal of Arachnology. 33 (3): 767–775. doi:10.1636/S03-56.1. Arhivat din original (PDF) la . Accesat în .
- ^ Mark I. McCormick, Christopher A. Ryen, Philip L. Munday, Stefan P. W. Walker (). „Differing mechanisms underlie sexual size-dimorphism in two populations of a sex-changing fish”. PLoS One. 5 (5): e10616. doi:10.1371/journal.pone.0010616. PMC 2868897
 . PMID 20485547.
. PMID 20485547.
- ^ Warner, 1988[necesită citare]
- ^ Adams and Williams, 2001[necesită citare]
Bibliografie[modificare | modificare sursă]
- Andersson, Malte B. (). Sexual Selection. Princeton University Press. ISBN 978-0-691-00057-2.
- Futuyma, D (). Evolution (ed. 1st). Sunderland, Massachusetts: Sinauer Associates. ISBN 978-0-87893-187-3.
- Ridley, M (). Evolution (ed. 3rd). Malden, Massachusetts: Blackwell Publishing. ISBN 978-1-4051-0345-9.
Lectură suplimentară[modificare | modificare sursă]
- Bonduriansky, Russell (). „The evolution of condition-dependent sexual dimorphism”. The American Naturalist. 169 (1): 9–19. doi:10.1086/510214. PMID 17206580.
- Figuerola, Jordi (). „A comparative study on the evolution of reversed size dimorphism in monogamous waders”. Biological Journal of the Linnean Society. 67 (1): 1–18. doi:10.1111/j.1095-8312.1999.tb01926.x.


