Acid formic
| Acid formic | |
 | |
 | |
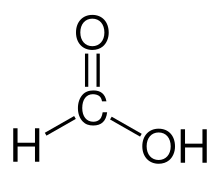
 Acid formic 85% | |
| Nume IUPAC | Acid formic |
|---|---|
| Alte denumiri | Acid metanoic |
| Identificare | |
| Număr CAS | 64-18-6 |
| ChEMBL | CHEMBL116736 |
| PubChem CID | 284 |
| Informații generale | |
| Formulă chimică | CH2O2 |
| Masă molară | 46,03 g/mol |
| Proprietăți | |
| Densitate | 1,22 g/cm3 |
| Starea de agregare | lichidă |
| Punct de topire | 8 °C |
| Punct de fierbere | 100,8 °C (se descompune) |
| Solubilitate | bună în apă, etanol și glicol |
| Presiune de vapori | 28 hPa |
| Indice de refracție(nD) | 1,3714 |
| Vâscozitate | dinamică 0,16 poiseuille |
| Sunt folosite unitățile SI și condițiile de temperatură și presiune normale dacă nu s-a specificat altfel. | |
| Modifică date / text | |
Acidul formic (nume sistematic: acid metanoic) este acidul carboxilic care are formula chimică H-COOH. Acidul formic se folosește ca solvent organic în industrie, la fabricarea insecticidelor și în industria tăbăcăriei. Sărurile sale se numesc formiați, un exemplu fiind formiatul de sodiu.
Obținere[modificare | modificare sursă]
Acidul formic se poate obține, în doi pași, prin reacția dintre hidroxid de sodiu și monoxid de carbon și acidulare cu acid sulfuric:
Se mai poate obține concomitent cu dioxid de carbon prin încălzirea rapidă a acidului oxalic la peste 200 °C[2]
Reacții[modificare | modificare sursă]
Acest acid este un compus agent reducător. Este oxidat de permanganat:
- ; în prezență de H2SO4;
Utilizare[modificare | modificare sursă]
Poate fi folosit în oxidare electrochimică în pile de combustie cu acid formic.
Note[modificare | modificare sursă]
- ^ „acid formic”, formic acid (în engleză), PubChem, accesat în
- ^ Nenițescu, ediția a VIII-a (1980), p. 758
Bibliografie[modificare | modificare sursă]
- C. D. Nenițescu, Chimie organică, ediția a VIII-a, vol I, Editura Didactică și Pedagogică, București, 1980
| ||||||||


![{\displaystyle HCOOH+[O]\longrightarrow CO_{2}+H_{2}O}](https://wikimedia.org/api/rest_v1/media/math/render/svg/0d0ca8dc35afe6838a0b593e211ef027dccbcbf8)

