Tuberculoză
| Tuberculoză | |
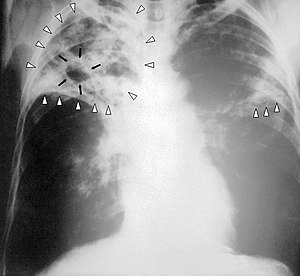 Radiografie pulmonară (examen cu Raze X) a unei persoane bolnave de tuberculoză în stadiu avansat. Săgețile albe indică infecția în ambii plămâni. Săgețile negre arată cavitatea care s-a format. | |
| Specialitate | boli infecțioase pneumologie |
|---|---|
| Simptome | tuse[1] hemoptizie slăbire[1] febră[1] transpirații nocturne[*][2] Durere toracică[1] fatigue[*][1] frisoane[*][1] |
| Cauze | Mycobacterium tuberculosis[3][4] |
| Metodă de diagnostic | radiografia toracelui[*][5] chest CT[*][6] Mantoux test[*][7] lung biopsy[*][8] Tuberculosis radiology[*][9] Abreugrafia[*][10] cultură spută[*][11] GeneXpert MTB/RIF[*][12] TB-LAM in the Diagnosis of TB[*][13][14] QuantiFERON[*][15] Colorația Ziehl-Neelsen[16] T-SPOT.TB[*][17] |
| Clasificare și resurse externe | |
| ICD-9 | 010–018 |
| ICD-10 | A15–A19 |
| ICD-11 | |
| OMIM | 607948 |
| DiseasesDB | 8515 |
| MedlinePlus | 000077 000624 |
| eMedicine | med/2324 emerg/618 radio/411 |
| Patient UK | Tuberculoză |
| MeSH ID | D014376 |
| Modifică date / text | |
Tuberculoza, sau TBC (abreviere pentru „bacilul de tubercul”) este o boală infecțioasă frecventă și, în cele mai multe cazuri, curabilă, provocată de diferite tipuri de micobacterii, de obicei de Mycobacterium tuberculosis.[18] Cel mai des, tuberculoza atacă plămânii, dar poate afecta și alte părți ale corpului (pleură, rinichi, peritoneu, piele, ochi, oase etc.). Tuberculoza se transmite prin aer, când persoanele care suferă de forme active de TBC tușesc, strănută sau elimină spută în aer (picăturile Flügge).[19] Cele mai contagioase forme sunt cele cavitare si cele extensive. Una din zece infecții latente progresează ulterior în boala activă. Lăsată netratată, tuberculoza omoară peste 50% din persoanele afectate.
Simptomele clasice ale tuberculozei active sunt tusea cronică, cu sângerări nazale, spută, febră, oboseală cronică, transpirația nocturnă și scăderea în greutate (TBC se numea în trecut „boala consumării”, din cauza scăderii în greutate a persoanelor infectate). Infectarea altor organe provoacă o varietate mare de simptome. Diagnosticul tuberculozei active se face prin radiologie, (cunoscută drept radiografie toracică) prin examinare microscopică și cultură microbiologică a fluidelor corporale. Diagnosticarea tuberculozei latente se face prin testul cutanat la tuberculină (TCT) și analize de sânge. Tratamentul presupune administrarea mai multor antibiotice pentru o perioadă îndelungată de timp (minimum 3 luni). De asemenea, contactele sociale ale persoanei infectate se examinează și tratează, dacă este necesar. Rezistența la antibiotice constituie o problemă în creștere în cazul tuberculozei rezistente la medicamente multiple (MDR-TB). Pentru a preveni TBC, oamenii trebuie examinați anual (radiografie pulmonară) pentru depistarea bolii și educați să aibă o viață echilibrată ca să nu le scadă imunitatea și să fie vulnerabili la infecție, copii mici trebuie vaccinați cu bacilul Calmette–Guérin pentru prevenirea îmbolnăvirilor cu forme grave care pot lăsa sechele majore (tuberculoza miliară, meningo-encefalita TBC).
Specialiștii cred că o treime din populația lumii este infectată cu M. tuberculosis,[20] și o nouă persoană se infectează în fiecare secundă.[20] În 2007, s-au estimat 13,7 milioane de cazuri cronice active la nivel mondial.[21] În 2010, s-au dezvoltat aproximativ 8,8 milioane de cazuri noi și s-au înregistrat 1,5 milioane de decese asociate tuberculozei, majoritatea în țările în curs de dezvoltare.[22] Numărul total de cazuri de tuberculoză este în scădere începând cu anul 2006, iar ce al cazurilor noi, din 2002.[22] Cazurile cu tuberculoză multidrog-rezistentă sunt în creștere, iar rezistența este din ce în ce mai extinsă, făcând din această formă de tuberculoză o amenințare mortală. Tuberculoza nu este uniform distribuită în lume. Aproximativ 80% din populația multor țări asiatice și africane dă rezultate pozitive la testul de tuberculină, în comparație cu doar 5-10% din populația Statelor Unite.[18] Mai multe persoane din țările în curs de dezvoltare contractează tuberculoza, din cauza imunității scăzute. De obicei, aceste persoane se îmbolnăvesc de tuberculoză deoarece sunt infectate cu HIV și dezvoltă SIDA.[23]
Semne și simptome[modificare | modificare sursă]
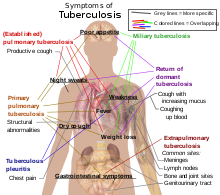
Aproximativ 5–10% din persoanele care nu au HIV, dar sunt infectate cu tuberculoză dezvoltă forma activă a bolii în timpul vieții.[25] În contrast, 30% din persoanele infectate cu HIV și tuberculoză dezvoltă forma activă a bolii.[25] Tuberculoza poate afecta orice parte a organismului, dar mai frecvent plămânii (cunoscută drept tuberculoză pulmonară).[26] TBC extrapulmonară este cea care se dezvoltă în afara plămânilor. TBC extrapulmonară poate coexista cu TBC pulmonară.[26] Semnele și simptomele generale includ febră, frisoane, transpirații în timpul somnului, pierderea poftei de mâncare, scăderea în greutate și letargie.[26] Mai poate fi observată și deformarea semnificativă a degetelor.[25]
Tuberculoza pulmonară[modificare | modificare sursă]
Dacă infecția cu tuberculoză devine activă, boala se dezvoltă în plămâni în aproximativ 90% din cazuri.[23][27] Simptomele pot include dureri în piept și tuse îndelungată, cu spută. Aproximativ 25% din persoane nu prezintă niciun simptom (sunt „asimptomatice”).[23] Uneori persoanele bolnave au tuse cu sânge în cantități mici. În cazuri rare, infecția poate eroda artera pulmonară, slăbind peretele acesteia și conducând la formarea unei dilatații sacciforme, numită anevrism Rasmussen. Dacă acesta se rupe, conduce la dezvoltarea unei hemoragii masive. Tuberculoza poate deveni o boală cronică și poate cauza leziuni extinse în lobii superiori ai plămânilor. Lobii superiori sunt afectați mai des.[26] Motivul nu este foarte clar.[18] Probabil că lobii superiori sunt afectați mai des datorită circulației mai bune a aerului[18] sau scurgerii mai lente a limfei în partea de sus a plămânilor.[26]
Tuberculoza extrapulmonară[modificare | modificare sursă]
În 15–20% din cazurile active, infecția se extinde în afara aparatului respirator, provocând alte tipuri de tuberculoză.[28] TBC dezvoltată în afara organelor respiratorii se numește „tuberculoză extrapulmonară”.[29] Tuberculoza extrapulmonară este mai frecventă în cazul persoanelor imunodeprimate și al copiilor mici. Tuberculoza extrapulmonară se dezvoltă la peste 50% din persoanele infectate cu HIV.[29] Cele mai frecvente locuri de dezvoltare a infecției extrapulmonare sunt pleura (pleurezie tuberculoasă), sistemul nervos central (meningită tuberculoasă) și sistemul limfatic (scrofuloză ganglionară). Tuberculoza extrapulmonară poate afecta, printre alte locuri de infectare posibile, și sistemul uro-genital (tuberculoză urogenitală), oasele și articulațiile (morbul lui Pott în cazul localizării la coloana vertebrală). Când se dezvoltă în oase, boala mai numește și „tuberculoză osoasă”,[30] o formă a osteomielitei.[18] Uneori, ruperea abcesului tubercular prin piele duce la tuberculoza ulcerată.[31] O formă a tuberculozei potențial mai gravă și mai răspândită se numește „tuberculoză diseminată”, cunoscută drept tuberculoză miliară.[26] Tuberculoza miliară constituie aproximativ 10% din cazurile extrapulmonare.[32]
Cauze[modificare | modificare sursă]
Micobacteriile[modificare | modificare sursă]

Cauza principală a tuberculozei este Mycobacterium tuberculosis, un bacil aerob, imobil.[26] Multe dintre caracteristicile clinice unice ale acestui agent patogen sunt cauzate de conținutul lipidic ridicat.[33] Bacilul se divide la fiecare 16 –20 de ore. Această rată de diviziune este lentă, în comparație cu alte bacterii care se divid în mai puțin de o oră.[34] Micobacteriile au membrana externă alcătuită dintr-un strat lipidic dublu.[35] La colorația Gram, MTB fie se colorează foarte slab (Gram pozitiv), fie nu reține culoarea, deoarece celula sa are un conținut lipidic și de acid micolic ridicat.[36] MTB rezistă dezinfectanților slabi și poate supraviețui în stare de endospor timp de mai multe săptămâni. În natură, bacteria se poate dezvolta doar în celulele unui organism gazdă, însă M. tuberculosis poate fi cultivat în laborator.[37]
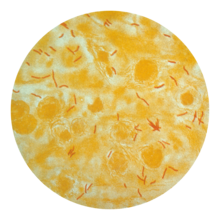
Aplicând coloranți histologici asupra mostrelor expectorate de flegmă, oamenii de știință pot identifica MTB cu un microscop obișnuit (flegma se mai numește „spută”). MTB reține anumiți coloranți, chiar și după tratarea cu soluții acide, de aceea se clasifică drept bacil acidorezistent (BAR).[18][36] Două tehnici cunoscute de colorare a bacteriilor acidorezistente sunt: colorația Ziehl-Neelsen, care colorează BAR în roșu aprins, evidențiat pe fundal albastru[38] și colorarea cu auramină-rodamină folosită în microscopia cu fluorescență.[39]
Complexul Mycobacterium tuberculosis (MTBC) include patru alte micobacterii care provoacă tuberculoza: Mycobacterium bovis, Mycobacterium africanum, Mycobacterium canetti și Mycobacterium microti[40] M. africanum nu este răspândită, dar constituie cauza principală a tuberculozei în anumite regiuni ale Africii.[41][42] M. bovis a fost în trecut o cauză obișnuită a tuberculozei, dar introducerea pasteurizării laptelui a exclus, în mare, această micobacterie din rândul factorilor de risc pentru sănătate în țările dezvoltate.[18][43] M. canetti nu este frecventă și pare a fi răspândită doar în Cornul Africii, deși unele cazuri au fost observate la emigranții africani.[44][45] Și M. microti este rară și apare mai des la persoanele imunodeficiente, dar este posibil ca acest agent patogen să fie mai frecvent decât se crede.[46]
Alte micobacterii patogene cunoscute sunt M. leprae, M. avium și M. kansasii. Ultimele două specii se clasifică drept „micobacterii non-tuberculoase” (MNT). MNT nu provoacă TBC sau lepră, dar provoacă alte afecțiuni pulmonare, similare tuberculozei.[47]
Factori de risc[modificare | modificare sursă]
Mai mulți factori îi fac pe oameni susceptibili la infecția tuberculoasă. Cel mai important factor de risc la nivel global este HIV; 13% dintre toate cazurile de tuberculoză prezintă infecție cu virusul HIV.[22] Această problemă este frecventă în Africa Subsahariană, unde ratele de îmbolnăvire cu HIV sunt ridicate.[48][49] Tuberculoza este strâns legată de suprapopulare și de nutriția deficitară. Această legătură face ca tuberculoza să fie una dintre principalele boli ale sărăciei.[23] Următoarele categorii de populație prezintă un risc mare de infectare cu tuberculoză: persoanele care își injectează substanțe interzise, locuitorii și angajații din locurile unde se strâng persoane vulnerabile (de exemplu, închisori și adăposturi pentru persoane fără locuință), persoanele sărace și care nu beneficiază de îngrijire medicală adecvată, minoritățile etnice cu risc mare, copiii în contact strâns cu persoane cu risc mare și furnizorii de îngrijire medicală care tratează aceste persoane.[50] Boala pulmonară cronică este un alt factor de risc important. Silicoza crește riscul de aproximativ 30 de ori.[51] Persoanele care fumează țigarete prezintă un risc de două ori mai mare decât nefumătorii.[52] Alte stări patologice pot crește, de asemenea, riscul de dezvoltare a tuberculozei, inclusiv alcoolismul[23] și diabetul zaharat (triplează riscul).[53] Unele medicamente, precum corticosteroizii și infliximab (un anticorp monoclonal anti-αTNF) sunt factori importanți de creștere a riscului, mai ales în țările dezvoltate.[23] De asemenea, există o predispoziție genetică,[54] dar oamenii de știință nu au stabilit ponderea acesteia.[23]
Mecanism[modificare | modificare sursă]

Transmitere[modificare | modificare sursă]
Când o persoană cu tuberculoză pulmonară activă tușește, strănută, vorbește, cântă sau scuipă, elimină picături infecțioase de aerosoli cu diametrul de 0,5 - 5 µm. Un singur strănut poate elibera până la 40.000 de picături.[55] Fiecare picătură poate transmite boala, deoarece doza infecțioasă a tuberculozei este foarte mică (o persoană poate fi infectată prin inhalarea a mai puțin de 10 bacterii).[56]
Persoanele cu contact prelungit, frecvent sau apropiat cu persoane cu tuberculoză au un risc mare de a se infecta, având o rată estimată de infecție de 22%.[57] O persoană cu tuberculoză activă dar netratată poate infecta 10–15 (sau mai mulți) alți oameni într-un an.[20] În mod normal, doar persoanele cu tuberculoză activă transmit boala. Persoanele cu infecție latentă nu sunt considerate contagioase.[18] Probabilitatea transmiterii de la o persoană la alta depinde de mai mulți factori. Acești factori includ numărul de picături infecțioase eliminate de purtător, eficiența ventilării mediului în care trăiesc persoanele, durata expunerii, virulența tulpinii de M. tuberculosis și nivelul de imunitate al persoanei neinfectate.[58] Pentru a preveni răspândirea în cascadă, de la o persoană la alta, persoanele cu tuberculoză activă („manifestă”) trebuiesc izolate și tratate cu medicamente împotriva tuberculozei. În general, după două săptămâni de tratament eficient, persoanele cu infecții active nerezistente nu mai sunt contagioase pentru ceilalți.[57] După infectare, în mod normal sunt necesare trei-patru săptămâni pentru ca persoana nou infectată să devină suficient de contagioasă pentru a transmite boala altor persoane.[59]
Patogeneză[modificare | modificare sursă]
Aproximativ 90% dintre persoanele infectate cu M. tuberculosis prezintă infecții asimptomatice latente (numite uneori LTBI).[60] La aceste persoane există o probabilitate de 10% ca, pe timpul vieții, infecția latentă să avanseze la stadiul de infecție tuberculoasă activă, manifestă.[61] Pentru persoanele cu HIV, riscul ca ele să dezvolte tuberculoză activă crește cu aproximativ 10% pe an.[61] Dacă nu se administrează un tratament eficient, rata deceselor la cazurile de tuberculoză activă este de 66%.[20]
Infecția tuberculoasă începe atunci când micobacteria ajunge la alveolele pulmonare, unde invadează și se multiplică în endozomii celulelor macrofage alveolare.[18][62] Localizarea principală a infecției plămânilor, numită și „focar Ghon”, este în partea de sus a lobului inferior sau în partea de jos a lobului superior.[18] De asemenea, tuberculoza pulmonară poate apărea prin infecția prin sânge, cunoscută drept focar Simon. În general, focarele Simon sunt localizate în partea de sus a plămânului.[63] Această transmitere hematogenă poate răspândi infecția și în locuri mai îndepărtate, cum ar fi ganglionii limfatici periferici, rinichii, creierul și sistemul osos.[18][64] Tuberculoza poate afecta toate organele, deși, fără motive cunoscute, afectează rareori inima, mușchii scheletici, pancreasul sau tiroida.[65]
Tuberculoza este clasificată în rândul bolilor inflamatorii granulomatoase. Celulele macrofage, limfocitele T, limfocitele B și fibroblastul se numără printre celulele care agregă pentru a forma granuloame. Limfocitele înconjoară celulele macrofage infectate. Granuloamele previn diseminarea micobacteriei și oferă un mediu local pentru interacțiunea celulelor cu sistemul imunitar. Bacteriile din interiorul granulomului pot deveni inactive, ceea ce determină o infecție latentă. O altă caracteristică a granuloamelor este dezvoltarea morții celulare anormale (necroză) în centrul tuberculilor. Observată cu ochiul liber, această necroză are textură brânzoasă, fiind albă și moale, și este numită necroză de cazeificare.[66]
Bacilii tuberculoși pot pătrunde în sânge dintr-un țesut deteriorat. Ei se pot răspândi în corp și pot forma mai multe focare de infecție, asemenea unor tuberculi albi, mici, fixați pe țesuturi.[67] Această formă severă de tuberculoză este numită tuberculoza miliară. Această formă de tuberculoză se întâlnește în general la copiii mici și la persoanele cu HIV.[68] Incidența deceselor este ridicată în rândul persoanelor care suferă de această tuberculoză diseminată, chiar dacă li se administrează tratament (aproximativ 30%).[32][69]
În cazul multor persoane afectate, infecția este inițial puternică și apoi scade în intensitate. Distrugerea și necrozarea țesutului sunt adesea balansate de vindecare și fibroză.[66] Țesutul afectat este înlocuit de cicatrici și cavități umplute cu material necrotic de cazeificare. Pe durata bolii, unele dintre aceste cavități sunt în contact cu căile respiratorii (bronhii) și acest material poate fi expulzat prin tuse. Acest material conține bacterii vii și poate răspândi infecția. Tratamentul cu antibioticele adecvate ucide bacteriile și permite vindecarea, zonele afectate fiind înlocuite cu țesut de cicatrizare.[66]
Diagnostic[modificare | modificare sursă]
Tuberculoza activă[modificare | modificare sursă]
Diagnosticul tuberculozei active numai pe baza semnelor și simptomelor clinice este dificil.[70] De asemenea, este dificilă diagnosticarea bolii la persoanele imunosupresate.[71] Cu toate acestea, persoanele care prezintă semne de boală pulmonară sau simptome constituționale care durează de mai mult de două săptămâni ar putea fi bolnave de tuberculoză.[71] Radiografia toracică și culturile de spută multiple pentru bacilii acid-rezistenți fac parte, în mod obișnuit, din evaluarea inițială.[71] Testul de eliberare de interferon gamma (testul IGRA) și testul cutanat la tuberculină nu sunt utile în țările în curs de dezvoltare.[72][73] Testele IGRA au limitări similare la persoanele cu HIV.[73][74]
Un diagnostic definitiv de tuberculoză este stabilit după identificarea M. tuberculosis într-o probă clinică (de exemplu, spută, puroi sau biopsia unui țesut). Cu toate acestea, procesul dificil de obținere a culturii pentru acest organism cu creștere lentă poate dura două până la șase săptămâni pentru culturile din sânge sau din spută.[75] Astfel, tratamentul este adesea început înainte de confirmarea culturilor.[76]
Testul de amplificare a acizilor nucleici și testul adenozin-dezaminazei pot diagnostica rapid tuberculoza.[70] Cu toate acestea, testele acestea nu sunt recomandate ca teste de rutină, deoarece rareori modifică modul de tratare a pacientului.[76] Testele de sânge pentru detectarea anticorpilor nu sunt specifice sau sensibile, prin urmare nu sunt recomandate.[77]
Tuberculoza latentă[modificare | modificare sursă]

Testul cutanat la tuberculină (testul Mantoux) este adesea utilizat pentru a identifica persoanele cu risc ridicat de tuberculoză.[71] Persoanele care au fost imunizate anterior pot avea o reacție fals pozitivă la acest test.[78] Testul poate fi fals negativ în cazul persoanelor care suferă de sarcoidoză, boala Hodgkin și malnutriție. Cel mai important, testul poate fi fals negativ în cazul persoanelor cu tuberculoză activă.[18] În cazul persoanelor cu reacție pozitivă la testul Mantoux se recomandă testul de eliberare de interferon gamma (IGRA) pe un eșantion de sânge.[76] Rezultatele testului IGRA nu sunt influențate de imunizare sau de majoritatea micobacteriilor din mediu, astfel încât sunt mai rar fals pozitive.[79] Totuși, rezultatele sunt influențate de M. szulgai, M. marinum și M. kansasii.[80] Sensibilitatea testului IGRA poate creste dacă este utilizat în combinație cu testul cutanat. Dacă însă este utilizat individual, sensibilitatea testului IGRA poate fi mai redusă decât cea a testului cutanat.[81]
Prevenire[modificare | modificare sursă]
Eforturile de prevenire și control al tuberculozei se bazează pe vaccinarea nou-născuților și pe detectarea și tratamentul adecvat al cazurilor active.[23] Organizația Mondială a Sănătății (OMS) a atins un anumit grad de reușită datorită unui regim de tratament îmbunătățit, observându-se o ușoară scădere a numărului de cazuri.[23]
Vaccinare[modificare | modificare sursă]
Începând din anul 1921, singurul vaccin disponibil este vaccinul BCG (vaccinul împotriva bacilului Calmette–Guérin). BCG este eficient împotriva răspândirii bolii în copilărie, însă conferă un grad de protecție variabil împotriva tuberculozei pulmonare.[82] Totuși, este vaccinul cu cea mai largă răspândire în lume, peste 90% dintre copii fiind vaccinați.[23] Imunitatea pe care o induce scade însă după aproximativ zece ani de la administrare.[23] Tuberculoza este o boală cu frecvență redusă în majoritatea provinciilor canadiene, în Marea Britanie și Statele Unite, vaccinul BCG fiind astfel administrat doar persoanelor cu risc crescut.[83][84][85] Unul dintre motivele pentru care nu se recomandă administrarea vaccinului este că acesta determină rezultate fals pozitive la testul cutanat la tuberculină, anulând eficacitatea acestuia în identificarea bolii.[85] În prezent, alte vaccinuri sunt în curs de dezvoltare.[23]
Sănătate publică[modificare | modificare sursă]
În anul 1993, Organizația Mondială a Sănătății a declarat tuberculoza o „problemă urgentă de sănătate globală”.[23] În 2006, parteneriatul pentru oprirea tuberculozei a întocmit Planul global de stopare a tuberculozei, al cărui obiectiv principal este să salveze 14 milioane de vieți până în 2015.[86] Nu toate obiectivele propuse vor fi atinse până în anul 2015, îndeosebi din cauza creșterii numărului de cazuri de tuberculoză asociată cu infecția HIV și apariția tuberculozei multidrog-rezistentă (MDR-TB).[23] În programele de sănătate publică se utilizează sistemul de clasificare a tuberculozei dezvoltat de Societatea Americană de Boli Toracice.[87]
Menținerea sub control a bolii[modificare | modificare sursă]
În tratamentul tuberculozei sunt prescrise antibiotice pentru exterminarea bacteriilor. Tratamentul poate fi uneori dificil din cauza structurii neobișnuite și compoziției chimice a peretelui celular micobacterian. Acesta blochează pătrunderea medicamentelor, anulând astfel eficiența unor antibiotice.[88] Cele două tipuri de antibiotice utilizate cel mai frecvent sunt izoniazida și rifampicina, tratamentele putând dura luni de zile.[58] În cazul tuberculozei latente, se administrează de regulă un singur tip de antibiotic.[89] În cazurile de tuberculoză activă cel mai eficiente sunt combinațiile de mai multe antibiotice pentru a reduce riscul ca bacteriile să dezvolte o rezistență la antibiotice.[23] De asemenea, pacienții cu infecție latentă sunt tratați pentru a preveni apariția ulterioară a tuberculozei active.[89] OMS recomandă terapia sub observare directă, prin care un cadru medical observă în mod direct luarea medicamentelor de către pacient. Obiectivul acestei terapii este de a reduce numărul persoanelor care nu urmează tratamentul în mod corespunzător.[90] Eficiența terapiei prin observare directă este aceeași cu a reamintirii importanței tratamentului.[91] Metodele de reamintire a importanței tratamentului sunt și ele eficiente.[92]
Instalarea bolii[modificare | modificare sursă]
Începând din anul 2010, tratamentul recomandat în cazul tuberculozei pulmonare în fază incipientă constă în administrarea unei combinații de antibiotice pe o durată de șase luni. În primele două luni se administrează rifampicină, izoniazidă, pirazinamidă și etambutol. În ultimele patru luni, se administrează numai rifampicină și izoniazidă.[23] În caz de rezistență crescută la izoniazidă, aceasta poate fi înlocuită cu etambutol în ultimele patru luni.[23]
Recurența bolii[modificare | modificare sursă]
În caz de recurență a bolii, înainte de a stabili tratamentul trebuiesc efectuate analize pentru a identifica antibioticele la care bacilul este sensibil.[23] În caz de tuberculoză multidrog-rezistentă (MDR-TB), se recomandă tratamentul cu cel puțin patru antibiotice eficiente pe o durată de 18–24 luni.[23]
Rezistența la medicamente[modificare | modificare sursă]
Rezistența primară apare în cazul în care o persoană este infectată cu o tulpină rezistentă. O persoană infectată poate dezvolta rezistență secundară (dobândită) la medicamente antituberculoase în timpul terapiei. Rezistența secundară poate apărea ca urmare a unui tratament inadecvat, datorită administrării incorecte a acestuia (nerespectarea tratamentului de către pacient), ori datorită utilizării de medicamente de proastă calitate.[93] Tuberculoza rezistentă la tratament constituie o problemă gravă de sănătate publică în multe țări în curs de dezvoltare. Tratamentul tuberculozei rezistente la tratament este mai îndelungat și necesită medicamente mai scumpe. MDR-TB se definește ca rezistența la cele două medicamente de linia întâi cu cea mai mare eficiență: rifampicină și izoniazidă. Tuberculoza cu rezistență extinsă la medicamentele antituberculoase este rezistentă la cel puțin trei dintre cele șase clase de medicamente de linia a doua.[94] Tuberculoza cu rezistență totală la medicamentele antituberculoase este rezistentă la toate medicamentele utilizate în prezent. Primul caz de tuberculoză cu rezistență totală la medicamentele antituberculoase a fost observat în Italia în anul 2003, dar nu și pe scară extinsă până în 2012.[95]
Prognostic[modificare | modificare sursă]

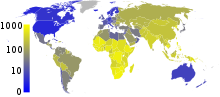
nu sunt date ≤10 ≥10–25 ≥25–50 ≥50–75 ≥75–100 ≥100–250 | ≥250–500 ≥500–750 ≥750–1000 ≥1000–2000 ≥2000–3000 ≥ 3000 |
Evoluția de la infecție la boală se produce în stadiul în care bacilii trec de barierele de protecție imunitară și încep să se multiplice. În cazul tuberculozei primare (aproximativ 1–5% din cazuri), această evoluție are loc imediat după infecția inițială.[18] Totuși, în majoritatea cazurilor, se produce infecția latentă, fără simptome evidente.[18] Acești bacili inactivi declanșează tuberculoza activă în 5–10% din cazurile latente, adesea după mai mulți ani de la infectare.[25]
Riscul de reactivare a bolii crește în caz de imunosupresie, produsă de exemplu de infectarea cu virusul HIV. În cazul persoanelor co-infectate cu „M. tuberculosis” și HIV, riscul de reactivare crește cu 10% pe an.[18] Studiile care utilizează amprente ADN ale tulpinilor „M. tuberculosis” demonstrează că reinfecția cauzează apariția tuberculozei recurente mai des decât se credea până acum.[97] Se consideră că reinfecția provoacă peste 50% din cazurile de tuberculoză reactivată în zonele cu răspândire mare a bolii.[98] Riscul de deces cauzat de tuberculoză a fost de 4% în anul 2008, în scădere de la cel de 8% înregistrat în 1995.[23]
Epidemiologie[modificare | modificare sursă]
Aproximativ o treime din populația lumii este infectată cu „M. tuberculosis”. În fiecare secundă, pe glob se produce o nouă infecție.[20] Totuși, majoritatea infecțiilor cu „M. tuberculosis” nu cauzează tuberculoza,[100] iar 90–95% dintre infecții nu prezintă simptome.[60] În 2007, existau aproximativ 13,7 milioane de cazuri de tuberculoză activă.[21] În 2010, numărul cazurilor nou diagnosticate a fost de 8,8 milioane, iar numărul de decese a fost de 1,45 milioane, majoritatea survenite în țările în curs de dezvoltare.[22] Dintre cele 1,45 milioane de decese, aproximativ 0,35 milioane s-au produs în rândul persoanelor co-infectate cu HIV.[101]
Tuberculoza reprezintă a doua cauză a mortalității ca urmare a unei boli infecțioase (principala cauză fiind HIV/SIDA).[26] Numărul total de cazuri de tuberculoză („prevalența”) este în scădere din anul 2005. Numărul de noi îmbolnăviri („incidența”) a scăzut din anul 2002.[22] Îndeosebi China a realizat o evoluție remarcabilă în acest sens. Între 1990 și 2010, China a redus rata mortalității cauzate de tuberculoză cu aproximativ 80%.[101] Tuberculoza este o boală mai frecvent întâlnită în țările în curs de dezvoltare. În aproximativ 80% din populația multor țări din Asia și Africa testul la tuberculină este pozitiv, în timp ce acest lucru este valabil doar în 5–10% din populația S.U.A.[18] Specialiștii au sperat ca tuberculoza să poată fi controlată complet. Totuși, controlul complet al maladiei este puțin probabil, datorită mai multor factori. Dezvoltarea unui vaccin eficient s-a dovedit dificilă. Costul este ridicat, iar diagnosticarea bolii necesită timp. Tratamentul durează mai multe luni. Un număr mai ridicat de persoane infectate cu HIV contractează tuberculoza. Tuberculoza rezistentă la medicamente a apărut în anii 1980.[23]
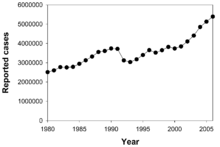
În anul 2007, țara cu cea mai ridicată rată de incidență estimată a fost Swaziland, cu 1.200 de cazuri la 100.000 de persoane. India a înregistrat cea mai ridicată incidență totală estimată a maladiei, cu 2 milioane de noi cazuri.[21] În țările dezvoltate, tuberculoza este o boală mai puțin obișnuită și este prezentă în special în zonele urbane. În 2010, ratele de TBC la 100.000 de persoane în diferite regiuni ale lumii au fost următoarele: pe glob 178, Africa 332, America de Nord și de Sud 36, Estul Mediteranei 173, Europa 63, Asia de Sud-Est 278 și Pacificul de Vest 139.[101] În Canada și Australia, tuberculoza este mult mai des întâlnită în rândul populațiilor aborigene, îndeosebi în zonele îndepărtate.[103][104] În Statele Unite, mortalitatea datorată tuberculozei în rândul populațiilor aborigene este de cinci ori mai ridicată.[105]
Incidența tuberculozei variază în funcție de vârstă. În Africa, maladia afectează în primul rând persoanele cu vârsta între 12 și 18 ani și adulții tineri.[106] Totuși, în țările în care ratele de incidență au scăzut considerabil (cum este cazul Statelor Unite), tuberculoza afectează îndeosebi persoanele în vârstă și persoanele cu un sistem imunitar deficitar.[18][107]
Tuberculoza în România[modificare | modificare sursă]
Tuberculoza este întâlnită în România mai frecvent decât în alte țări ale Uniunii Europene, se estimează că apar în medie 130 de cazuri la 100 000 de locuitori, față de media europeană de circa 30 bolnavi la suta de mii de locuitori.[108] Se estimează că în România sunt aproximativ 30 000 bolnavi în toată țara. În fiecare județ există cel puțin un spital și trei-patru dispensare de pneumoftiziologie.[108]
Istoric[modificare | modificare sursă]

Tuberculoza a apărut la oameni încă din antichitate.[23] Cea mai veche dovadă a bolii o constituie bacteria „M. tuberculosis” descoperită în fosilele unui bizon care a trăit în urmă cu aproape 17.000 ani.[109] Pe de altă parte, nu se știe cu exactitate dacă tuberculoza provine de la bovine, fiind transferată ulterior la om, sau dacă a apărut de la un strămoș comun.[110] A existat o perioadă în care oamenii de știință credeau că MTBC (complexul M. tuberculosis) a fost transmis de la animal la om în timpul domesticirii animalelor. Cu toate acestea, prin compararea genelor complexului „M. tuberculosis” (MTBC) de la oameni cu cele de la animale, s-a demonstrat că această teorie este falsă. Ambele tulpini bacteriene provin de la un strămoș comun, care ar fi putut provoca apariția infecției la oameni încă din perioada cunoscută sub numele de Revoluția neolitică.[111] Fragmentele de schelet găsite indică faptul că oamenii preistorici (4000 î.Hr.) sufereau de tuberculoză. Cercetătorii au putut constata o afectare tuberculoasă a coloanei vertebrale la mumiile egiptene din perioada 3000–2400 î.Hr.[112] „Ftizie” este termenul grecesc pentru „oftică,” vechea denumire a tuberculozei pulmonare.[113] În jurul anului 460 î.Hr., Hippocrate considera că ftizia era cea mai răspândită boală din acea vreme. Bolnavii de tuberculoză făceau febră și tușeau cu sânge. De cele mai multe ori, boala era fatală.[114] Studiile genetice indică faptul că tuberculoza există în America încă din jurul anului 100 d.Hr.[115]
Înainte de Revoluția industrială, în tradiția populară, tuberculoza era adesea asociată cu vampirii. Atunci când unul din membrii unei familii murea din cauza acestei boli, ceilalți membri ai familiei respective, care contractaseră și ei infecția, se îmbolnăveau și ei treptat. Se credea că cel care s-a îmbolnăvit primul secătuiește viața celorlalți membri ai familiei sale.[116]
Formațiunile pulmonare asemănătoare unor tuberculi au fost incluse printre simptomele bolii de către Dr. Richard Morton în 1689.[117][118] Cu toate acestea, tuberculoza poate prezenta o mare varietate de simptome, astfel că boala nu a putut fi identificată ca atare decât în jurul anului 1820. Numele de tuberculoză i-a fost dat de-abia în anul 1839 de către J. L. Schönlein.[119] Între 1838 și 1845, Dr. John Croghan, proprietarul Mammoth Cave, obișnuia să ducă bolnavii de tuberculoză în peșteră, în speranța că aceștia se vor însănătoși datorită temperaturii constante și aerului curat din interiorul acesteia: bolnavii respectivi au murit după mai puțin de un an.[120] Hermann Brehmer a deschis primul sanatoriu TBC în 1859, în Sokołowsko, Polonia.[121]

Bacilul care provoacă tuberculoza, „Mycobacterium tuberculosis”, a fost descoperit la 24 martie 1882 de Robert Koch. Pentru descoperirea sa, Koch a primit Premiul Nobel pentru Fiziologie sau Medicină în 1905.[122] Koch nu credea că există vreo legătură între tuberculoza la bovine (vite) și tuberculoza la oameni. Din acest motiv, destul de târziu s-a putut stabili că laptele infectat reprezintă o sursă de infecție. Ulterior, riscul transmiterii de la această sursă a fost redus în mod simțitor datorită introducerii procesului de pasteurizare. În 1890, Koch a susținut că un anumit extras de glicerină din bacilul tuberculozei constituie „leacul” împotriva tuberculozei. A numit acest extras „tuberculină”. Deși „tuberculina” s-a dovedit ineficientă, aceasta a fost adaptată ca test de screening pentru identificarea prezenței bolii în faza presimptomatică.[123]
Albert Calmette și Camille Guérin au înregistrat primul succes în imunizarea împotriva tuberculozei în anul 1906. Aceștia au folosit o tulpină atenuată a bacilului tuberculozei bovine pentru a crea un vaccin pe care l-au numit vaccinul BCG (bacilul lui Calmette și Guérin). Vaccinul BCG a fost folosit pentru prima dată la oameni în anul 1921 în Franța.[124] Pe de altă parte, vaccinul BCG a fost utilizat pe scară largă doar în SUA, Marea Britanie și Germania de-abia după cel de-al doilea război mondial.[125]
Tuberculoza a creat o profundă îngrijorare în secolul al XIX-lea și la începutul secolului al XX-lea, fiind considerată o boală endemică a populației urbane sărace. În 1815, în Anglia, unul din patru oameni murea de „oftică”. În 1918, în Franța, unul din șase oameni murea de tuberculoză. După ce oamenii de știință au stabilit, în jurul anului 1880, că boala este contagioasă, tuberculoza a fost inclusă într-o listă a bolilor cu declarare obligatorie în Marea Britanie. Au fost inițiate campanii care să îi convingă pe oameni să nu mai scuipe în locurile publice, iar persoanele sărace infectate erau „încurajate” să se interneze în sanatorii care semănau mai degrabă cu niște închisori. (Sanatoriile pentru clasele de mijloc și cele superioare ofereau servicii excelente de asistență medicală.)[121] Se presupunea că sanatoriile oferă avantajele unui mediu cu „aer curat”. Dar chiar și în cele mai bune condiții, 50% dintre cei internați mureau în următorii cinci ani („cca.” 1916).[121]
În Europa, rata îmbolnăvirilor de tuberculoză a început să crească la începutul anului 1600. Îmbolnăvirile de tuberculoză au atins un nivel de vârf în Europa în jurul anului 1800, constituind cauza a aproximativ 25% din totalul deceselor înregistrate.[126] Până în 1950, numărul deceselor scăzuse cu aproape 90%.[127] Schimbările întreprinse în sistemul de sănătate publică au redus în mod semnificativ incidența tuberculozei chiar înainte ca streptomicina și alte antibiotice să înceapă să fie utilizate. Chiar și în aceste condiții, boala a rămas o amenințare serioasă la adresa sănătății publice. La înființarea sa în 1913, Medical Research Council din Marea Britanie punea accent pe cercetarea în domeniul tuberculozei.[128]
În 1946, dezvoltarea antibioticului numit streptomicină a transformat în realitate tratarea eficientă și vindecarea bolnavilor de TBC. Înainte de introducerea acestui medicament, singurul tratament (cu excepția sanatoriilor) consta în intervenția chirurgicală. „Tehnica pneumotorax” comprima plămânul infectat pentru a-l „imobiliza”, permițând astfel leziunilor tuberculoase să se vindece.[129] Apariția MDR-TB a introdus din nou intervenția chirurgicală ca opțiune în cadrul standardelor de asistență medicală în tratamentul afecțiunilor pulmonare TBC. Intervențiile chirurgicale actuale implică îndepărtarea cavităților patologice din plămâni („bule”) pentru a reduce numărul bacteriilor existente și pentru a crește expunerea bacteriilor rămase la medicamentele din sânge. Prin intervenția chirurgicală se reduce numărul total al bacteriilor și se crește eficiența tratamentului sistemic cu antibiotice.[130] Deși specialiștii au sperat să elimine complet tuberculoza (vezi variola), apariția tulpinilor rezistente la medicamente, în jurul anului 1980, a făcut mai puțin probabilă eradicarea tuberculozei. Reapariția ulterioară a bolii a determinat OMS să declare tuberculoza o urgență mondială în anul 1993.[131]
Societate și cultură[modificare | modificare sursă]
Organizația Mondială a Sănătății și Fundația Bill și Melinda Gates finanțează un nou test de diagnostic rapid pentru țările cu venituri mici și mijlocii.[132][133] În 2011, foarte multe țări sărace aveau acces doar la diagnosticul prin microscopia sputei.[134]
În 2010, în India s-a înregistrat cel mai mare număr de cazuri de tuberculoză la nivel mondial. Una dintre cauze a fost gestionarea defectuoasă a bolii de către sectorul privat de sănătate. Programe precum Programul Național de Control al Tuberculozei contribuie la scăderea numărului de cazuri de TBC în rândul populației care beneficiază de serviciile sistemului public de sănătate.[135][136]
Cercetare[modificare | modificare sursă]
Vaccinul BCG are limitele sale, fapt pentru care, în prezent, se fac cercetări pentru a dezvolta noi vaccinuri anti-TBC.[137] Câteva dintre acestea se află deja în studii clinice de faza I și II.[137] Se încearcă eficientizarea vaccinurilor disponibile prin două metode. Una dintre aceste metode presupune adăugarea unei subunități de vaccin la BCG. Cea de-a doua metodă constă în încercarea de a dezvolta noi vaccinuri active, mai eficiente.[137]MVA85A constituie un exemplu de vaccin subunitar, aflat în faza de evaluare clinică în Africa de Sud. MVA85A are la bază un virus Vaccinia modificat genetic.[138] Se speră ca vaccinurile să joace un rol important în tratarea tuberculozei latente și active.[139]
Pentru a încuraja descoperirile ulterioare, cercetătorii și factorii de decizie promovează noi modele economice pentru dezvoltarea de vaccinuri, inclusiv premii, stimulente fiscale și angajamente prealabile de punere pe piață.[140][141] În activitatea de cercetare sunt implicate grupuri precum Stop TB Partnership,[142] SATVI (South African Tuberculosis Vaccine Initiative) și Aeras Global TB Vaccine Foundation.[143] Fundația Aeras a primit peste 280 milioane de dolari din partea Fundației Bill și Melinda Gates pentru a dezvolta și omologa o formă îmbunătățită a vaccinului anti-TBC, care să fie utilizată în țările cu o incidență ridicată a bolii.[144][145]
Sunt studiate o serie de medicamente pentru tuberculoza rezistentă la mai multe droguri, inclusiv: bedaquilina și delamanidul.[146] Bedaquilina este primită de Food and Drug Administration (FDA) din S.U.A. aprobată în 2012.[147] Siguranța acestui nou agent este încă necunoscută deoarece numărul de persoane cărora a fost administrat este mic.[146]
Tuberculoza la animale[modificare | modificare sursă]
Micobacteriile pot infecta foarte multe animale, inclusiv păsări,[148] rozătoare[149] și reptile.[150] Subspeciile „Mycobacterium tuberculosis” apar foarte rar la animalele sălbatice.[151] Efortul de eradicare a tuberculozei bovine cauzate de „Mycobacterium bovis” în rândul bovinelor, căprioarelor și cerbilor din Noua Zeelandă a fost relativ încununat de succes.[152] În Marea Britanie, eforturile în acest sens au avut mai puțin succes.[153][154]
Referințe[modificare | modificare sursă]
- ^ a b c d e f https://www.webmd.com/lung/understanding-tuberculosis-basics Lipsește sau este vid:
|title=(ajutor) - ^ https://www.sil.org/resources/archives/95641 Lipsește sau este vid:
|title=(ajutor) - ^ Centrul pentru Prevenirea și Controlul Bolilor
- ^ Disease Ontology
- ^ https://www.radiologymasterclass.co.uk/gallery/chest/pulmonary-disease/tuberculosis_tb Lipsește sau este vid:
|title=(ajutor) - ^ https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4531444/ Lipsește sau este vid:
|title=(ajutor) - ^ https://www.cdc.gov/tb/topic/testing/tbtesttypes.htm Lipsește sau este vid:
|title=(ajutor) - ^ https://www.nature.com/articles/s41598-023-43078-x#:~:text=Transbronchial%20lung%20biopsy%20(TBLB)%20is,subject%20of%20limited%20studies1. Lipsește sau este vid:
|title=(ajutor) - ^ https://emedicine.medscape.com/article/358610-overview Lipsește sau este vid:
|title=(ajutor) - ^ https://pubmed.ncbi.nlm.nih.gov/768593/ Lipsește sau este vid:
|title=(ajutor) - ^ https://www.healthlinkbc.ca/healthlinkbc-files/sputum-testing-tuberculosis-tb Lipsește sau este vid:
|title=(ajutor) - ^ https://www.cdc.gov/tb/publications/factsheets/testing/xpert_mtb-rif.htm Lipsește sau este vid:
|title=(ajutor) - ^ https://tbksp.org/en/node/1692 Lipsește sau este vid:
|title=(ajutor) - ^ https://bmcinfectdis.biomedcentral.com/articles/10.1186/1471-2334-13-407 Lipsește sau este vid:
|title=(ajutor) - ^ https://www.ouh.nhs.uk/immunology/diagnostic-tests/tests-catalogue/quantiferon-tb-gold.aspx#:~:text=Quantiferon%20is%20an%20ELISA%20based,plasma%20is%20measured%20by%20ELISA. Lipsește sau este vid:
|title=(ajutor) - ^ https://www.sciencedirect.com/topics/immunology-and-microbiology/ziehl-neelsen-stain#:~:text=Microscopic%20examination%20of%20clinical%20samples,%C3%97%20103%20organisms%2FmL. Lipsește sau este vid:
|title=(ajutor) - ^ https://www.ouh.nhs.uk/immunology/diagnostic-tests/tests-catalogue/t-spot-tb.aspx Lipsește sau este vid:
|title=(ajutor) - ^ a b c d e f g h i j k l m n o p q Kumar V, Abbas AK, Fausto N, Mitchell RN (). Robbins Basic Pathology (ed. 8th). Saunders Elsevier. pp. 516–522. ISBN 978-1-4160-2973-1.
- ^ Konstantinos A (). „Testing for tuberculosis”. Australian Prescriber. 33 (1): 12–18.
- ^ a b c d e „Tuberculosis Fact sheet N°104”. World Health Organization. noiembrie 2010. Accesat în .
- ^ a b c World Health Organization (). „Epidemiology” (PDF). Global tuberculosis control: epidemiology, strategy, financing. pp. 6–33. ISBN 978-92-4-156380-2. Accesat în .[nefuncțională]
- ^ a b c d e World Health Organization (). „The sixteenth global report on tuberculosis” (PDF).
- ^ a b c d e f g h i j k l m n o p q r s t u v Lawn, SD (). „Tuberculosis”. Lancet. 378 (9785): 57–72. doi:10.1016/S0140-6736(10)62173-3. PMID 21420161.
- ^ Schiffman G (). „Tuberculosis Symptoms”. eMedicineHealth.
- ^ a b c d al.], edited by Peter G. Gibson ; section editors, Michael Abramson ... [et (). Evidence-based respiratory medicine (ed. 1. publ.). Oxford: Blackwell. p. 321. ISBN 978-0-7279-1605-1.
- ^ a b c d e f g h Dolin, [edited by] Gerald L. Mandell, John E. Bennett, Raphael (). Mandell, Douglas, and Bennett's principles and practice of infectious diseases (ed. 7th). Philadelphia, PA: Churchill Livingstone/Elsevier. pp. Chapter 250. ISBN 978-0-443-06839-3.
- ^ Behera, D. (). Textbook of pulmonary medicine (ed. 2nd ed.). New Delhi: Jaypee Brothers Medical Pub. p. 457. ISBN 978-81-8448-749-7.
- ^ Jindal, editor-in-chief SK. Textbook of pulmonary and critical care medicine. New Delhi: Jaypee Brothers Medical Publishers. p. 549. ISBN 978-93-5025-073-0.
- ^ a b Golden MP, Vikram HR (). „Extrapulmonary tuberculosis: an overview”. American family physician. 72 (9): 1761–8. PMID 16300038.
- ^ Kabra, [edited by] Vimlesh Seth, S.K. (). Essentials of tuberculosis in children (ed. 3rd ed.). New Delhi: Jaypee Bros. Medical Publishers. p. 249. ISBN 978-81-8061-709-6.
- ^ Manual of Surgery. Kaplan Publishing. . p. 75. ISBN 9781427797995.
- ^ a b Ghosh, editors-in-chief, Thomas M. Habermann, Amit K. (). Mayo Clinic internal medicine : concise textbook. Rochester, MN: Mayo Clinic Scientific Press. p. 789. ISBN 978-1-4200-6749-1.
- ^ Southwick F (). „Chapter 4: Pulmonary Infections”. Infectious Diseases: A Clinical Short Course, 2nd ed. McGraw-Hill Medical Publishing Division. p. 104. ISBN 0-07-147722-5. Arhivat din originalul de la . Accesat în . Mai multe valori specificate pentru
|pages=și|page=(ajutor) - ^ Jindal, editor-in-chief SK. Textbook of pulmonary and critical care medicine. New Delhi: Jaypee Brothers Medical Publishers. p. 525. ISBN 978-93-5025-073-0.
- ^ Niederweis M, Danilchanka O, Huff J, Hoffmann C, Engelhardt H (). „Mycobacterial outer membranes: in search of proteins”. Trends in Microbiology. 18 (3): 109–16. doi:10.1016/j.tim.2009.12.005. PMC 2931330
 . PMID 20060722.
. PMID 20060722.
- ^ a b Madison B (). „Application of stains in clinical microbiology”. Biotech Histochem. 76 (3): 119–25. doi:10.1080/714028138. PMID 11475314.
- ^ Parish T, Stoker N (). „Mycobacteria: bugs and bugbears (two steps forward and one step back)”. Molecular Biotechnology. 13 (3): 191–200. doi:10.1385/MB:13:3:191. PMID 10934532.
- ^ Medical Laboratory Science: Theory and Practice. New Delhi: Tata McGraw-Hill. . p. 473. ISBN 0-07-463223-X.
- ^ Piot, editors, Richard D. Semba, Martin W. Bloem; foreword by Peter (). Nutrition and health in developing countries (ed. 2nd ed.). Totowa, NJ: Humana Press. p. 291. ISBN 978-1-934115-24-4.
- ^ van Soolingen D; et al. (). „A novel pathogenic taxon of the Mycobacterium tuberculosis complex, Canetti: characterization of an exceptional isolate from Africa”. International Journal of Systematic Bacteriology. 47 (4): 1236–45. doi:10.1099/00207713-47-4-1236. PMID 9336935.
- ^ Niemann S; et al. (). „Mycobacterium africanum Subtype II Is Associated with Two Distinct Genotypes and Is a Major Cause of Human Tuberculosis in Kampala, Uganda”. J. Clin. Microbiol. 40 (9): 3398–405. doi:10.1128/JCM.40.9.3398-3405.2002. PMC 130701
 . PMID 12202584.
. PMID 12202584.
- ^ Niobe-Eyangoh SN; et al. (). „Genetic Biodiversity of Mycobacterium tuberculosis Complex Strains from Patients with Pulmonary Tuberculosis in Cameroon”. J. Clin. Microbiol. 41 (6): 2547–53. doi:10.1128/JCM.41.6.2547-2553.2003. PMC 156567
 . PMID 12791879.
. PMID 12791879.
- ^ Thoen C, Lobue P, de Kantor I (). „The importance ofMycobacterium bovis as a zoonosis”. Vet. Microbiol. 112 (2–4): 339–45. doi:10.1016/j.vetmic.2005.11.047. PMID 16387455.
- ^ Acton, Q. Ashton (). Mycobacterium Infections: New Insights for the Healthcare Professional. ScholarlyEditions. p. 1968. ISBN 978-1-4649-0122-5.
- ^ Pfyffer, GE (1998 Oct-Dec). „Mycobacterium canettii, the smooth variant of M. tuberculosis, isolated from a Swiss patient exposed in Africa”. Emerging infectious diseases. 4 (4): 631–4. PMID 9866740. Verificați datele pentru:
|date=(ajutor) - ^ Panteix, G (2010 Aug). „Pulmonary tuberculosis due to Mycobacterium microti: a study of six recent cases in France”. Journal of medical microbiology. 59 (Pt 8): 984–9. PMID 20488936. Verificați datele pentru:
|date=(ajutor) - ^ American Thoracic Society (). „Diagnosis and treatment of disease caused by nontuberculous mycobacteria. Această afirmație oficială a Societății Toracice Americane a fost aprobată în martie 1997 de către Consiliul de administrație. Medical Section of the American Lung Association”. Am J Respir Crit Care Med. 156 (2 Pt 2): S1–25. PMID 9279284.
- ^ World Health Organization. „Global tuberculosis control–surveillance, planning, financing WHO Report 2006”. Accesat în .
- ^ Chaisson, RE (). „Tuberculosis in Africa--combating an HIV-driven crisis”. The New England Journal of Medicine. 358 (11): 1089–92. doi:10.1056/NEJMp0800809. PMID 18337598.
- ^ Griffith D, Kerr C (). „Tuberculosis: disease of the past, disease of the present”. J Perianesth Nurs. 11 (4): 240–5. doi:10.1016/S1089-9472(96)80023-2. PMID 8964016.
- ^ ATS/CDC Statement Committee on Latent Tuberculosis Infection (). „Targeted tuberculin testing and treatment of latent tuberculosis infection. American Thoracic Society”. MMWR Recomm Rep. 49 (RR–6): 1–51. PMID 10881762.
- ^ van Zyl Smit, RN (2010 Jan). „Global lung health: the colliding epidemics of tuberculosis, tobacco smoking, HIV and COPD”. The European respiratory journal : official journal of the European Society for Clinical Respiratory Physiology. 35 (1): 27–33. PMID 20044459.
Aceste analize arată că fumătorii au de o probabilitate de două ori mai mare de a contacta infecția tuberculoasă și de a trece la stadiul de boală activă (rată de risc de ∼1,5 pentru infecție latentă cu tuberculoză (LTBI) și rată de risc de ∼2,0 pentru boala tuberculoasă). De asemenea, fumătorii au o probabilitate de două ori mai mare să moară de tuberculoză (rată de risc de ∼2,0 de mortalitate din cauza tuberculozei), dar datele sunt dificil de interpretat din cauza eterogenității rezultatelor provenite din diferitele studii.
Verificați datele pentru:|date=(ajutor) - ^ Restrepo, BI (). „Convergence of the tuberculosis and diabetes epidemics: renewal of old acquaintances”. Clinical infectious diseases : an official publication of the Infectious Diseases Society of America. 45 (4): 436–8. doi:10.1086/519939. PMC 2900315
 . PMID 17638190.
. PMID 17638190.
- ^ Möller, M (2010 Mar). „Current findings, challenges and novel approaches in human genetic susceptibility to tuberculosis”. Tuberculosis (Edinburgh, Scotland). 90 (2): 71–83. doi:10.1016/j.tube.2010.02.002. PMID 20206579. Verificați datele pentru:
|date=(ajutor) - ^ Cole E, Cook C (). „Characterization of infectious aerosols in health care facilities: an aid to effective engineering controls and preventive strategies”. Am J Infect Control. 26 (4): 453–64. doi:10.1016/S0196-6553(98)70046-X. PMID 9721404.
- ^ Nicas M, Nazaroff WW, Hubbard A (). „Toward understanding the risk of secondary airborne infection: emission of respirable pathogens”. J Occup Environ Hyg. 2 (3): 143–54. doi:10.1080/15459620590918466. PMID 15764538.
- ^ a b Ahmed N, Hasnain S (). „Molecular epidemiology of tuberculosis in India: Moving forward with a systems biology approach”. Tuberculosis. 91 (5): 407–3. doi:10.1016/j.tube.2011.03.006. PMID 21514230.
- ^ a b „Core Curriculum on Tuberculosis: What the Clinician Should Know” (PDF) (ed. 5th). Centers for Disease Control and Prevention (CDC), Division of Tuberculosis Elimination. . Parametru necunoscut
|pg=ignorat (ajutor) - ^ „Causes of Tuberculosis”. Mayo Clinic. . Accesat în .
- ^ a b Skolnik, Richard (). Global health 101 (ed. 2nd ed.). Burlington, MA: Jones & Bartlett Learning. p. 253. ISBN 978-0-7637-9751-5.
- ^ a b editors, Arch G. Mainous III, Claire Pomeroy, (). Management of antimicrobials in infectious diseases : impact of antibiotic resistance (ed. 2nd rev. ed.). Totowa, N.J.: Humana. p. 74. ISBN 978-1-60327-238-4.
- ^ Houben E, Nguyen L, Pieters J (). „Interaction of pathogenic mycobacteria with the host immune system”. Curr Opin Microbiol. 9 (1): 76–85. doi:10.1016/j.mib.2005.12.014. PMID 16406837.
- ^ Khan (). Essence Of Paediatrics. Elsevier India. p. 401. ISBN 978-81-312-2804-3.
- ^ Herrmann J, Lagrange P (). „Dendritic cells and Mycobacterium tuberculosis: which is the Trojan horse?”. Pathol Biol (Paris). 53 (1): 35–40. doi:10.1016/j.patbio.2004.01.004. PMID 15620608.
- ^ Agarwal R, Malhotra P, Awasthi A, Kakkar N, Gupta D (). „Tuberculous dilated cardiomyopathy: an under-recognized entity?”. BMC Infect Dis. 5 (1): 29. doi:10.1186/1471-2334-5-29. PMC 1090580
 . PMID 15857515.
. PMID 15857515.
- ^ a b c Grosset J (). „Mycobacterium tuberculosis in the Extracellular Compartment: an Underestimated Adversary”. Antimicrob Agents Chemother. 47 (3): 833–6. doi:10.1128/AAC.47.3.833-836.2003. PMC 149338
 . PMID 12604509.
. PMID 12604509.
- ^ Crowley, Leonard V. (). An introduction to human disease : pathology and pathophysiology correlations (ed. 8th ed.). Sudbury, Mass.: Jones and Bartlett. p. 374. ISBN 978-0-7637-6591-0.
- ^ Anthony, Harries (). TB/HIV a Clinical Manual (ed. 2nd). Geneva: World Health Organization. p. 75. ISBN 978-92-4-154634-8.
- ^ Jacob, JT (2009 Jan). „Acute forms of tuberculosis in adults”. The American journal of medicine. 122 (1): 12–7. PMID 19114163. Verificați datele pentru:
|date=(ajutor) - ^ a b Bento, J (2011 Jan-Feb). „[Diagnostic tools in tuberculosis]”. Acta medica portuguesa. 24 (1): 145–54. PMID 21672452. Verificați datele pentru:
|date=(ajutor) - ^ a b c d Escalante, P (2009 Jun 2). „In the clinic. Tuberculosis”. Annals of internal medicine. 150 (11): ITC61–614; quiz ITV616. PMID 19487708. Verificați datele pentru:
|date=(ajutor) - ^ Metcalfe, JZ (2011 Nov 15). „Interferon-γ release assays for active pulmonary tuberculosis diagnosis in adults in low- and middle-income countries: systematic review and meta-analysis”. The Journal of infectious diseases. 204 Suppl 4: S1120–9. PMID 21996694. Verificați datele pentru:
|date=(ajutor) - ^ a b Sester, M (2011 Jan). „Interferon-γ release assays for the diagnosis of active tuberculosis: a systematic review and meta-analysis”. The European respiratory journal : official journal of the European Society for Clinical Respiratory Physiology. 37 (1): 100–11. PMID 20847080. Verificați datele pentru:
|date=(ajutor) - ^ Chen, J (). „Interferon-gamma release assays for the diagnosis of active tuberculosis in HIV-infected patients: a systematic review and meta-analysis”. PloS one. 6 (11): e26827. PMID 22069472.
- ^ Diseases, Special Programme for Research & Training in Tropical (). Diagnostics for tuberculosis : global demand and market potential. Geneva: World Health Organization on behalf of the Special Programme for Research and Training in Tropical Diseases. p. 36. ISBN 978-92-4-156330-7.
- ^ a b c Format:NICE
- ^ Steingart, KR (2011 Aug). „Commercial serological tests for the diagnosis of active pulmonary and extrapulmonary tuberculosis: an updated systematic review and meta-analysis”. PLoS medicine. 8 (8): e1001062. doi:10.1371/journal.pmed.1001062. PMC 3153457
 . PMID 21857806. Verificați datele pentru:
. PMID 21857806. Verificați datele pentru: |date=(ajutor) - ^ Rothel J, Andersen P (). „Diagnosis of latent Mycobacterium tuberculosis infection: is the demise of the Mantoux test imminent?”. Expert Rev Anti Infect Ther. 3 (6): 981–93. doi:10.1586/14787210.3.6.981. PMID 16307510.
- ^ Pai M, Zwerling A, Menzies D (). „Systematic Review: T-Cell–based Assays for the Diagnosis of Latent Tuberculosis Infection: An Update”. Ann. Intern. Med. 149 (3): 1–9. PMC 2951987
 . PMID 18593687.
. PMID 18593687.
- ^ Jindal, editor-in-chief SK. Textbook of pulmonary and critical care medicine. New Delhi: Jaypee Brothers Medical Publishers. p. 544. ISBN 978-93-5025-073-0.
- ^ Amicosante, M (2010 Apr). „Rational use of immunodiagnostic tools for tuberculosis infection: guidelines and cost effectiveness studies”. The new microbiologica. 33 (2): 93–107. PMID 20518271. Verificați datele pentru:
|date=(ajutor) - ^ McShane, H (). „Tuberculosis vaccines: beyond bacille Calmette–Guérin”. Philosophical transactions of the Royal Society of London. Series B, Biological sciences. 366 (1579): 2782–9. doi:10.1098/rstb.2011.0097. PMC 3146779
 . PMID 21893541.
. PMID 21893541.
- ^ „Vaccine and Immunizations: TB Vaccine (BCG)”. Centers for Disease Control and Prevention. . Accesat în .
- ^ „BCG Vaccine Usage in Canada -Current and Historical”. Public Health Agency of Canada. . Arhivat din original la . Accesat în .
- ^ a b Teo, SS (2006 Jun). „Does BCG have a role in tuberculosis control and prevention in the United Kingdom?”. Archives of Disease in Childhood. 91 (6): 529–31. doi:10.1136/adc.2005.085043. PMC 2082765
 . PMID 16714729. Verificați datele pentru:
. PMID 16714729. Verificați datele pentru: |date=(ajutor) - ^ „The Global Plan to Stop TB”. World Health Organization. . Accesat în .
- ^ Warrell, ed. by D. J. Weatherall ... [4. + 5. ed.] ed. by David A. (). Sections 1 - 10 (ed. 4. ed., paperback.). Oxford [u.a.]: Oxford Univ. Press. p. 560. ISBN 978-0-19-857014-1.
- ^ Brennan PJ, Nikaido H (). „The envelope of mycobacteria”. Annu. Rev. Biochem. 64: 29–63. doi:10.1146/annurev.bi.64.070195.000333. PMID 7574484.
- ^ a b Menzies, D (2011 Mar). „Recent developments in treatment of latent tuberculosis infection”. The Indian journal of medical research. 133: 257–66. PMID 21441678. Verificați datele pentru:
|date=(ajutor) - ^ Arch G., III Mainous (). Management of Antimicrobials in Infectious Diseases: Impact of Antibiotic Resistance. Humana Pr. p. 69. ISBN 1-60327-238-0.
- ^ Volmink J, Garner P (). „Directly observed therapy for treating tuberculosis”. Cochrane Database Syst Rev (4): CD003343. doi:10.1002/14651858.CD003343.pub3. PMID 17943789.
- ^ Liu, Q (2008 Oct 8). „Reminder systems and late patient tracers in the diagnosis and management of tuberculosis”. Cochrane database of systematic reviews (Online) (4): CD006594. PMID 18843723. Verificați datele pentru:
|date=(ajutor) - ^ O'Brien R (). „Drug-resistant tuberculosis: etiology, management and prevention”. Semin Respir Infect. 9 (2): 104–12. PMID 7973169.
- ^ Centers for Disease Control and Prevention (CDC) (). „Emergence of Mycobacterium tuberculosis with extensive resistance to second-line drugs—worldwide, 2000–2004”. MMWR Morb Mortal Wkly Rep. 55 (11): 301–5. PMID 16557213.
- ^ Maryn McKenna (). „Totally Resistant TB: Earliest Cases in Italy”. Wired. Accesat în .
- ^ „WHO Disease and injury country estimates”. World Health Organization. . Accesat în .
- ^ Lambert M; et al. (). „Recurrence in tuberculosis: relapse or reinfection?”. Lancet Infect Dis. 3 (5): 282. doi:10.1016/S1473-3099(03)00607-8. PMID 12726976. Mai multe valori specificate pentru
|pages=și|page=(ajutor) - ^ Wang, JY (). „Prediction of the tuberculosis reinfection proportion from the local incidence”. The Journal of infectious diseases. 196 (2): 281–8. doi:10.1086/518898. PMID 17570116.
- ^ World Health Organization (). „The Stop TB Strategy, case reports, treatment outcomes and estimates of TB burden”. Global tuberculosis control: epidemiology, strategy, financing. pp. 187–300. ISBN 978-92-4-156380-2. Accesat în .
- ^ „Fact Sheets: The Difference Between Latent TB Infection and Active TB Disease”. Centers for Disease Control. . Accesat în .
- ^ a b c „Global Tuberculosis Control 2011” (PDF). World Health Organization. Accesat în .
- ^ World Health Organization. „WHO report 2008: Global tuberculosis control”. Accesat în .
- ^ FitzGerald, JM (2000 Feb 8). „Tuberculosis: 13. Control of the disease among aboriginal people in Canada”. CMAJ : Canadian Medical Association journal = journal de l'Association medicale canadienne. 162 (3): 351–5. PMID 10693593. Verificați datele pentru:
|date=(ajutor) - ^ Quah, Stella R.; Carrin, Guy; Buse, Kent; Kristian Heggenhougen (). Health Systems Policy, Finance, and Organization. Boston: Academic Press. p. 424. ISBN 0-12-375087-3.
- ^ Anne-Emanuelle Birn (). Textbook of International Health: Global Health in a Dynamic World. p. 261. ISBN 9780199885213.
- ^ World Health Organization. „Global Tuberculosis Control Report, 2006 – Annex 1 Profiles of high-burden countries” (PDF). Accesat în .
- ^ Centers for Disease Control and Prevention (). „2005 Surveillance Slide Set”. Accesat în .
- ^ a b Dezbatere pe tema sănătății la cdep.ro
- ^ Rothschild BM; Martin LD; Lev G; et al. (). „Mycobacterium tuberculosis complex DNA from an extinct bison dated 17,000 years before the present”. Clin. Infect. Dis. 33 (3): 305–11. doi:10.1086/321886. PMID 11438894.
- ^ Pearce-Duvet J (). „The origin of human pathogens: evaluating the role of agriculture and domestic animals in the evolution of human disease”. Biol Rev Camb Philos Soc. 81 (3): 369–82. doi:10.1017/S1464793106007020. PMID 16672105.
- ^ Comas, I (2009 Oct). „The past and future of tuberculosis research”. PLoS pathogens. 5 (10): e1000600. PMID 19855821. Verificați datele pentru:
|date=(ajutor) - ^ Zink A, Sola C, Reischl U, Grabner W, Rastogi N, Wolf H, Nerlich A (). „Characterization of Mycobacterium tuberculosis Complex DNAs from Egyptian Mummies by Spoligotyping”. J Clin Microbiol. 41 (1): 359–67. doi:10.1128/JCM.41.1.359-367.2003. PMC 149558
 . PMID 12517873.
. PMID 12517873.
- ^ The Chambers Dictionary. New Delhi: Allied Chambers India Ltd. . p. 352. ISBN 978-81-86062-25-8.
- ^ Hippocrates.Aphorisms. Accessed 7 October 2006.
- ^ Konomi N, Lebwohl E, Mowbray K, Tattersall I, Zhang D (). „Detection of Mycobacterial DNA in Andean Mummies”. J Clin Microbiol. 40 (12): 4738–40. doi:10.1128/JCM.40.12.4738-4740.2002. PMC 154635
 . PMID 12454182.
. PMID 12454182.
- ^ Sledzik, Paul S. (). „Bioarcheological and biocultural evidence for the New England vampire folk belief” (PDF). American Journal of Physical Anthropology. 94 (2): 269–274. doi:10.1002/ajpa.1330940210. ISSN 0002-9483. PMID 8085617.
- ^ Format:WhoNamedIt
- ^ Trail RR (). „Richard Morton (1637-1698)”. Med Hist. 14 (2): 166–74. PMC 1034037
 . PMID 4914685.
. PMID 4914685.
- ^ Zur Pathogenie der Impetigines. Auszug aus einer brieflichen Mitteilung an den Herausgeber. [Müller’s] Archiv für Anatomie, Physiologie und wissenschaftliche Medicin. 1839, page 82.
- ^ Kentucky: Mammoth Cave long on history. Arhivat în , la Wayback Machine. CNN. 27 February 2004. Accessed 8 October 2006.
- ^ a b c McCarthy OR (). „The key to the sanatoria”. J R Soc Med. 94 (8): 413–7. PMC 1281640
 . PMID 11461990.
. PMID 11461990.
- ^ Nobel Foundation. The Nobel Prize in Physiology or Medicine 1905. Accessed 7 October 2006.
- ^ Waddington K (). „To stamp out "So Terrible a Malady": bovine tuberculosis and tuberculin testing in Britain, 1890–1939”. Med Hist. 48 (1): 29–48. PMC 546294
 . PMID 14968644.
. PMID 14968644.
- ^ Bonah C (). „The 'experimental stable' of the BCG vaccine: safety, efficacy, proof, and standards, 1921–1933”. Stud Hist Philos Biol Biomed Sci. 36 (4): 696–721. doi:10.1016/j.shpsc.2005.09.003. PMID 16337557.
- ^ Comstock G (). „The International Tuberculosis Campaign: a pioneering venture in mass vaccination and research”. Clin Infect Dis. 19 (3): 528–40. doi:10.1093/clinids/19.3.528. PMID 7811874.
- ^ Bloom, editor, Barry R. (). Tuberculosis : pathogenesis, protection, and control. Washington, D.C.: ASM Press. ISBN 978-1-55581-072-6.
- ^ Persson, Sheryl (). Smallpox, Syphilis and Salvation: Medical Breakthroughs That Changed the World. ReadHowYouWant.com. p. 141. ISBN 978-1-4587-6712-7.
- ^ editor, Caroline Hannaway, (). Biomedicine in the twentieth century: practices, policies, and politics. Amsterdam: IOS Press. p. 233. ISBN 978-1-58603-832-8.
- ^ Shields, Thomas (). General thoracic surgery (ed. 7th ed.). Philadelphia: Wolters Kluwer Health/Lippincott Williams & Wilkins. p. 792. ISBN 978-0-7817-7982-1.
- ^ Lalloo UG, Naidoo R, Ambaram A (). „Recent advances in the medical and surgical treatment of multi-drug resistant tuberculosis”. Curr Opin Pulm Med. 12 (3): 179–85. doi:10.1097/01.mcp.0000219266.27439.52. PMID 16582672. Arhivat din original la . Accesat în .
- ^ „Frequently asked questions about TB and HIV”. World Health Organization. Accesat în .
- ^ Lawn, SD (2011 Sep). „Xpert® MTB/RIF assay: development, evaluation and implementation of a new rapid molecular diagnostic for tuberculosis and rifampicin resistance”. Future microbiology. 6 (9): 1067–82. PMID 21958145. Verificați datele pentru:
|date=(ajutor) - ^ „WHO says Cepheid rapid test will transform TB care”. Reuters. .
- ^ Lienhardt, C (2011 Nov). „What research is needed to stop TB? Introducing the TB Research Movement”. PLoS medicine. 8 (11): e1001135. doi:10.1371/journal.pmed.1001135. PMC 3226454
 . PMID 22140369. Verificați datele pentru:
. PMID 22140369. Verificați datele pentru: |date=(ajutor) - ^ Anurag Bhargava, Lancelot Pinto, Madhukar Pai (). „Mismanagement of tuberculosis in India: Causes, consequences, and the way forward”. Hypothesis. 9 (1): e7. Arhivat din original la . Accesat în .
- ^ Amdekar, Y (2009 Jul). „Changes in the management of tuberculosis”. Indian journal of pediatrics. 76 (7): 739–42. PMID 19693453. Verificați datele pentru:
|date=(ajutor) - ^ a b c Martín Montañés, C (2011 Mar). „New tuberculosis vaccines”. Enfermedades infecciosas y microbiologia clinica. 29 Suppl 1: 57–62. doi:10.1016/S0213-005X(11)70019-2. PMID 21420568. Verificați datele pentru:
|date=(ajutor) - ^ Ibanga H, Brookes R, Hill P, Owiafe P, Fletcher H, Lienhardt C, Hill A, Adegbola R, McShane H (). „Early clinical trials with a new tuberculosis vaccine, MVA85A, in tuberculosis-endemic countries: issues in study design”. Lancet Infect Dis. 6 (8): 522–8. doi:10.1016/S1473-3099(06)70552-7. PMID 16870530.
- ^ Kaufmann SH (). „Future vaccination strategies against tuberculosis: Thinking outside the box”. Immunity. 33 (4): 567–77. doi:10.1016/j.immuni.2010.09.015. PMID 21029966.
- ^ Webber D, Kremer M (). „Stimulating Industrial R&D for Neglected Infectious Diseases: Economic Perspectives” (PDF). Bulletin of the World Health Organization. 79 (8): 693–801.
- ^ Barder O, Kremer M, Williams H (). „Advance Market Commitments: A Policy to Stimulate Investment in Vaccines for Neglected Diseases”. The Economists' Voice. 3 (3). doi:10.2202/1553-3832.1144.
- ^ Economic, Department of (). Achieving the global public health agenda : dialogues at the Economic and Social Council. New York: United Nations. p. 103. ISBN 978-92-1-104596-3.
- ^ Jong, [edited by] Jane N. Zuckerman, Elaine C. (). Travelers' vaccines (ed. 2nd ed.). Shelton, CT: People's Medical Pub. House. p. 319. ISBN 978-1-60795-045-5.
- ^ Bill and Melinda Gates Foundation Announcement (). „Gates Foundation Commits $82.9 Million to Develop New Tuberculosis Vaccines”. Arhivat din original la . Accesat în .
- ^ Nightingale, Katherine (). „Gates foundation gives US$280 million to fight TB”.
- ^ a b Zumla, A (2012 Mar 1). „Advancing the development of tuberculosis therapy”. Nature reviews. Drug discovery. 11 (3): 171–2. PMID 22378254. Verificați datele pentru:
|date=(ajutor) - ^ „J&J Sirturo Wins FDA Approval to Treat Drug-Resistant TB”. Bloombeg. Dec 31st,2012. Accesat în 1 January 2013. Verificați datele pentru:
|date=(ajutor) - ^ Shivaprasad, HL (2012 Jan). „Pathology of mycobacteriosis in birds”. The veterinary clinics of North America. Exotic animal practice. 15 (1): 41–55, v–vi. PMID 22244112. Verificați datele pentru:
|date=(ajutor) - ^ Reavill, DR (2012 Jan). „Mycobacterial lesions in fish, amphibians, reptiles, rodents, lagomorphs, and ferrets with reference to animal models”. The veterinary clinics of North America. Exotic animal practice. 15 (1): 25–40, v. PMID 22244111. Verificați datele pentru:
|date=(ajutor) - ^ Mitchell, MA (2012 Jan). „Mycobacterial infections in reptiles”. The veterinary clinics of North America. Exotic animal practice. 15 (1): 101–11, vii. PMID 22244116. Verificați datele pentru:
|date=(ajutor) - ^ Wobeser, Gary A. (). Essentials of disease in wild animals (ed. 1st ed.). Ames, Iowa [u.a.]: Blackwell Publ. p. 170. ISBN 978-0-8138-0589-4.
- ^ Ryan, TJ (2006 Feb 25). „Advances in understanding disease epidemiology and implications for control and eradication of tuberculosis in livestock: the experience from New Zealand”. Veterinary microbiology. 112 (2-4): 211–9. PMID 16330161. Verificați datele pentru:
|date=(ajutor) - ^ White, PC (2008 Sep). „Control of bovine tuberculosis in British livestock: there is no 'silver bullet'”. Trends in microbiology. 16 (9): 420–7. PMID 18706814. Verificați datele pentru:
|date=(ajutor) - ^ Ward, AI (2010 Jan 1). „Farm husbandry and badger behaviour: opportunities to manage badger to cattle transmission of Mycobacterium bovis?”. Preventive veterinary medicine. 93 (1): 2–10. PMID 19846226. Verificați datele pentru:
|date=(ajutor)
Vezi și[modificare | modificare sursă]
Legături externe[modificare | modificare sursă]
- Asociatia Romana a Bolnavilor de Tuberculoza - Pagina Facebook
- Asociatia Romana a Bolnavilor de Tuberculoza
- Știți cum să vă feriți? Azi: tuberculoza, 13 martie 2009, Amos News
