Cuban
| Cuban | |
 | |
 | |
| Identificare | |
|---|---|
| Număr CAS | 277-10-1 |
| PubChem CID | 136090 |
| Formulă chimică | C₈H₈[1] |
| Masă molară | 104,063 u.a.m.[1] |
| Punct de topire | 130 °C |
| Sunt folosite unitățile SI și condițiile de temperatură și presiune normale dacă nu s-a specificat altfel. | |
| Modifică date / text | |
Cubanul este un compus organic sintetic cu formula chimică C8H8. Este o hidrocarbură formată din opt atomi de carbon dispuși în colțurile unui cub, cu un atom de hidrogen atașat la fiecare atom de carbon. Este o substanță cristalină solidă. A fost sintetizat pentru prima dată în 1964 de Philip Eaton și Thomas Cole.[2] Înaintea acestei sinteze, Eaton a crezut că substanța nu poate fi sintetizată, din cauza unghiurilor de 90 grade din structura moleculară.[3][4]
Forma cubică moleculară face ca atomii de carbon să adopte un unghi de legătură neobișnuit, de 90°, care ar fi foarte tensionat în comparație cu unghiul de 109,45° al unui carbon tetraedric. Odată format, cubanul este destul de stabil din punct de vedere cinetic, din cauza lipsei unor metode de descompunere imediate. Astfel, este cea mai simplă hidrocarbură cu simetrie octaedrică.
Obținere
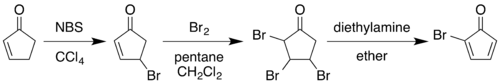
[modificare | modificare sursă]Sinteza clasică realizată în anul 1964 începe cu transformarea 2-ciclopentenonei la 2-bromociclopentadienonă:[2][5]
Prin bromurare alilică cu N-bromosuccinimidă în tetraclorură de carbon, urmată de adăugarea de brom molecular la alchenă, se obține o 2,3,4-tribromociclopentanonă. Tratarea acestui compus cu dietilamină în eter dietilic determină eliminarea a doi echivalenți de acid bromhidric pentru a obține produsul dienic:
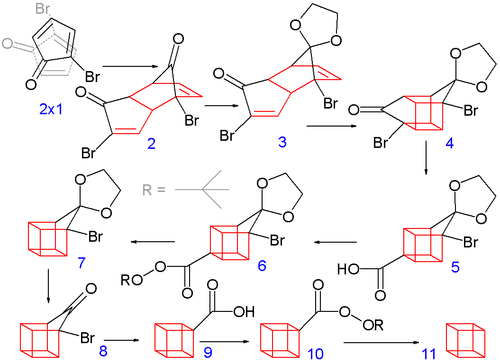
Construcția formei cubanului, cu structura formată din opt atomi de carbon, începe atunci când 2-bromociclopentadienona suferă o dimerizare spontană de tip Diels-Alder. Ulterior, un cetal al izomerului endo este deprotejat selectiv cu soluție de acid clorhidric (3).
În etapa următoare, izomerul endo 3 (cu ambele grupe alchene în imediata apropiere) formează izomerul 4, printr-o cicloadiție fotochimică [2+2]. Gruparea bromocetonă este transformată în acidul carboxilic cu 5 printr-o transpoziție Favorskii, în prezență de hidroxid de potasiu. În continuare, are loc decarboxilarea termică prin clorura de acid (cu clorură de tionil) și peresterul de terț-butil 6 (cu hidroperoxid de terț-butil și piridină) la compusul 7; după aceea, acetalul este din nou eliminat pentru a forma 8. O a doua transpoziție Favorskii dă compusul 9, iar în final o altă decarboxilare dă, prin intermediarul 10, cubanul (11).
Proprietăți
[modificare | modificare sursă]Cuneanul poate fi produs din cuban printr-o reacție de transpoziție σ catalizată de ioni metalici:[6] [7][7]
Cu un catalizator de rodiu, se formează mai întâi sin-triciclooctadiena, care se poate descompune termic în ciclooctatetraenă la 50-60 °C:[8]
Derivați
[modificare | modificare sursă]Datorită energiei potențiale ridicate și a stabilității cinetice, cubanul și compușii săi derivați sunt utili pentru stocarea controlată a energiei. De exemplu, octanitrocubanul și heptanitrocubanul au fost studiați ca explozibili de înaltă performanță.[9][10]
Note
[modificare | modificare sursă]- ^ a b c „Cuban”, Cubane (în engleză), PubChem, accesat în
- ^ a b Eaton, Philip E.; Cole, Thomas W. (). „Cubane”. J. Am. Chem. Soc. 86 (15): 3157–3158. doi:10.1021/ja01069a041.
- ^ Teachers, University of New South Wales Summer School for Chemistry (). Approach to Chemistry: Lectures and Workshop Reports of the ... Summer School for Chemistry Teachers (în engleză). The University. p. 98. "This compound was described only a few months ago and, curiously enough, it is quite easy to make, although only a year ago I would have predicted that it would be difficult, or even impossible , to synthesize."
- ^ Moore, John W.; Stanitski, Conrad L.; Jurs, Peter C. (). Chemistry: The Molecular Science (în engleză). Harcourt College Publishers. p. 372. ISBN 978-0-03-032011-8. "This sharp bond angle creates severe bond strain in cubane, a compound thought previously impossible to synthesize because of the required 90° bond angles."
- ^ Eaton, Philip E.; Cole, Thomas W. (). „The Cubane System”. J. Am. Chem. Soc. 86 (5): 962–964. doi:10.1021/ja01059a072.
- ^ Smith, Michael B.; March, Jerry (). March's Advanced Organic Chemistry
 (ed. 5th). John Wiley & Sons. p. 1459. ISBN 0-471-58589-0.
(ed. 5th). John Wiley & Sons. p. 1459. ISBN 0-471-58589-0.
- ^ a b Kindler, K.; Lührs, K. (). „Studien über den Mechanismus chemischer Reaktionen, XXIII. Hydrierungen von Nitrilen unter Verwendung von Terpenen als Wasserstoffdonatoren”. Chem. Ber. 99: 227–232. doi:10.1002/cber.19660990135.
- ^ Cassar, Luigi; Eaton, Philip E.; Halpern, Jack (). „Catalysis of symmetry-restricted reactions by transition metal compounds. Valence isomerization of cubane”. Journal of the American Chemical Society (în engleză). 92 (11): 3515–3518. doi:10.1021/ja00714a075. ISSN 0002-7863.
- ^ Zhang, Mao-Xi; Eaton, Philip E.; Gilardi, Richard (). „Hepta- and Octanitrocubanes”. Angewandte Chemie International Edition. 39 (2): 401–404. doi:10.1002/(SICI)1521-3773(20000117)39:2<401::AID-ANIE401>3.0.CO;2-P. PMID 10649425.
- ^ Eaton, Philip E.; Zhang, Mao-Xi; Gilardi, Richard; Gelber, Nat; Iyer, Sury; Surapaneni, Rao (). „Octanitrocubane: A New Nitrocarbon”. Propellants, Explosives, Pyrotechnics. 27 (1): 1–6. doi:10.1002/1521-4087(200203)27:1<1::AID-PREP1>3.0.CO;2-6.
Vezi și
[modificare | modificare sursă]
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||