Acetilenă
| Acetilenă | |
Formula structurală | |
 | |
 | |
| Denumiri | |
|---|---|
| Alte denumiri | Etină |
| Identificare | |
| Număr CAS | 74-86-2 |
| ChEMBL | CHEMBL116336 |
| PubChem CID | 6326 |
| Informații generale | |
| Formulă chimică | C2H2 |
| Aspect | gaz incolor |
| Masă molară | 26,04 g/mol |
| Proprietăți | |
| Densitate | 1,175 g/l |
| Starea de agregare | gazoasă |
| Punct de topire | −80,8 °C |
| Punct de fierbere | −84 °C (sublimă) |
| Solubilitate | în apă și bună în acetonă |
| Presiune de vapori | 44,2 de atmosferă fizicăi[2] |
| Pericol | |
| Fraze R | R5, R6, R12 |
| Fraze S | (S2), S9, S16, S33 |
| NFPA 704 | |
| Sunt folosite unitățile SI și condițiile de temperatură și presiune normale dacă nu s-a specificat altfel. | |
| Modifică date / text | |
Acetilena (nume sistematic etină) este o hidrocarbură alifatică nesaturată, cu o triplă legătură, descoperită de Humphry Davy în 1836 și sintetizată din elemente de Marcellin Berthelot în 1862. Este un gaz incolor, fără miros în stare pură, foarte solubil în acetonă. Formează acetiluri de cupru, argint, mercur, litiu, sodiu, potasiu, calciu, etc. Dă reacții de adiție, de polimerizare etc. Se poate obține prin reacția dintre carbid (acetilura de calciu) și apă sau din metan, prin oxidare parțială cu oxigen ori prin cracare în arc electric.
Este un compus de mare importanță, constituind baza pentru obținerea unui număr foarte mare de compuși în industria chimică. Din acetilenă se prepară aldehida acetică, acetona, clorura de vinil, acetatul de vinil, vinilacetilena, nitrilul acrilic.
Se folosește de asemenea la sudura oxiacetilenică și la iluminat. Acetilena se păstrează sub presiune în tuburi de construcție specială, umplute cu o masă poroasă imbibată cu acetona sau dimetilformamidă. Nu se poate păstra în stare pură sub presiune deoarece are tendința de a exploda la o presiune mai mare de 1.5 bar, fiind instabilă termodinamic în raport cu elementele componente.
În 1962, în R.P.R. se fabrica la Râșnov din gaz metan, iar la Turda (reg. Cluj) și Târnăveni (reg. Mureș) din carbid.
Producere[modificare | modificare sursă]
Se produce prin electrocracarea metanului în arc electric.
Până în 1950 era produsă de la carbid prin reacția cu apa.
Structură[modificare | modificare sursă]
Carbonul din acetilenă are orbitali hibrizi 2s cu 2p.
Proprietăți chimice[modificare | modificare sursă]
Este un compus instabil termodinamic față de elementele componente, se poate forma din elemente la temperaturi foarte ridicate[3].
Polimerizare[modificare | modificare sursă]
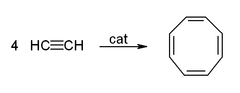
Acetilena poate suferi reacții de polimerizare, pentru a se obține compuși ciclici: benzenul (prin trimerizare) și ciclooctatetraena (prin tetramerizare):
Siguranță[modificare | modificare sursă]
Acetilena este foarte periculoasă, deoarece este reactivă și se aprinde ușor, datorită legăturilor triple (dintre atomii de carbon.)
Se transportă în vase conținând material poros umplut cu acetonă în care se dizolvă acetilena. Un litru de acetonă poate dizolva circa 250 litri de acetilenă la o presiune de 10 bar.[4][5]
Vezi și[modificare | modificare sursă]
Note[modificare | modificare sursă]
- ^ „Acetilenă”, Ethyne (în engleză), PubChem, accesat în
- ^ http://www.cdc.gov/niosh/npg/npgd0008.html Lipsește sau este vid:
|title=(ajutor) - ^ Nenițescu, ediția a VIII-a (1980), p. 157
- ^ Mine Safety and Health Administration (MSHA) – Safety Hazard Information – Special Hazards of Acetylene Arhivat în , la Wayback Machine.. Msha.gov. Retrieved on 2012-11-26.
- ^ History – Acetylene dissolved in acetone Arhivat în , la Wayback Machine.. Aga.com. Retrieved on 2012-11-26.
Bibliografie[modificare | modificare sursă]
- Constantin D. Albu, Maria Brezeanu, Mică enciclopedie de chimie, Editura Enciclopedică Română, 1974, p 10
- Costin Nenițescu, Chimie Organică, ediția a VIII-a, volumul I, Editura Didactică și Pedagogică, București, 1980
| |||||