Naftalină
| Acest articol sau această secțiune are bibliografia incompletă sau inexistentă. Puteți contribui prin adăugarea de referințe în vederea susținerii bibliografice a afirmațiilor pe care le conține. |
| Naftalină | |
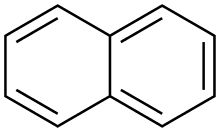 | |
 | |
| Denumiri | |
|---|---|
| Alte denumiri | Nafthalen (IUPAC) Naftacen |
| Identificare | |
| Număr CAS | 91-20-3 |
| ChEMBL | CHEMBL16293 |
| PubChem CID | 931 |
| Informații generale | |
| Formulă chimică | C10H8 |
| Aspect | culoare albă cristalină |
| Masă molară | 128,173 g/mol |
| Proprietăți | |
| Densitate | 1,14 g/cm3 |
| Starea de agregare | solid |
| Punct de topire | 81,2 °C |
| Punct de fierbere | 218 °C |
| Solubilitate | în solvenți organici |
| Presiune de vapori | 0,08 millimetre of mercury[2] |
| Indice de refracție(nD) | 1,5898[3] |
| Sunt folosite unitățile SI și condițiile de temperatură și presiune normale dacă nu s-a specificat altfel. | |
| Modifică date / text | |
Naftalina (greacă naphtha - petrol, țiței) este o substanță solidă, cristalină, albă cu miros caracteristic pătrunzător, cu formula chimică C10H8 care sublimează la temperatura camerei. Ea este o hidrocarbură aromatică cu două nuclee ciclice, fiind o substanță dăunătoare sănătății și mediului înconjurător.
Istoric[modificare | modificare sursă]
Naftalina a fost izolată din cărbune în anul 1819 de chimistul englez Alexander Garden, iar formula chimică a fost descoperită în anul 1866 de chimistul german Emil Erlenmeyer. Naftalina este considerată în mod tradițional o hidrocarbură aromatică policiclică, ea fiind compusă din două nuclee alipite de benzen. Existența celor două inele benzenice a fost demonstrată prin reacții de oxidare la acizi ftalici (C. Graebe, 1866).
Energia de conjugare a naftalinei este de 61 kcal/mol, mai mică decât dublul energiei de conjugare a benzenului (72 kcal). În comparație cu benzenul, naftalina are un caracter mai puțin aromatic. Repartiția celor 10 electroni π ai naftalinei poate fi reprezentată prin trei structuri limită Kekulé care participă la starea fundamentală (structurile cu sarcini despărțite nu au contribuție importantă).

Obținere[modificare | modificare sursă]
Naftalina se obține prin distilarea fracționată a gudroanelor de cărbuni care conțin până la 11 % naftalină. Ea se găsește de asemenea în petrol sau prin arderea lemnului și tutunului sau se formează în depozitele de gunoaie. Naftalina are NE=7.
Utilizare[modificare | modificare sursă]
În trecut naftalina era un produs de combatere a moliilor, azi din cauza mirosului neplăcut este înlocuit de alte substanțe. Azi se cunoaște faptul că naftalina aproape că nu are nici un efect insecticid. La începutul secolului XX era folosit ca gaz de iluminat, dezavantajul era că înfunda conductele. Cu toate că este toxic a fost folosită în trecut în medicină ca dezinfectant intestinal.
Naftalina este utilizată în special la sinteza unor diluanți, coloranți sau adezivi în industria de mase plastice ca PVC, la elaborarea insecticidelor din grupa carbamaților, ca și la fabricarea săpunurilor.
În anul 1987 a fost produs pe glob ca.1 milion de tone, de naftalină din care au fost produse în Europa de vest 250.000 de tone , Europa de est 200.000 de tone , Japonia 200.000 de tone și Statele Unite ale Americii 125.000 de tone .
Efecte asupra sănătații[modificare | modificare sursă]
În cadrul condițiilor de preparare și utilizare poate provoca intoxicații acute sau cronice, de ordin accidental sau profesional. Pătrunde în organism pe cale respiratorie, cutanată și rar pe cale digestivă. După absorbție, în organism se metabolizează pe cale oxidativă, prin hidroxilare, fără deschidere de ciclu.
Compușii hidrixilați rezultați se conjugă cu acidul glucuronic, glicocolul, acidul sulfuric și acidul mercapturic. Conjugarea mercapturică are loc în proporție de 10-15%, când se produce o carență de aminoacizi, manifestată la nivelul cristalinului(cataractă). Eliminarea are loc pe cale renală sub formă de metaboliți și/sau conjugați.
Naftalina este un toxic hemolizant - produce leucopenie, anemii -, hepatotoxic, nefrotoxic, iar la nivel ocular generează cataractă.
În caz de ingerare (copii) se produc tulburări digestive, uneori hipotensiune și deshidratare. La o doză de 30g apare coma, deseori urmată de convulsii. La indivizii cu deficit de glucozo-6'-fosfatdehidrogenază (G-6-PD) se declanșează mai ușor hemoliza, icter hemolitic și nefropatie tubulară.
Inhalarea vaporilor produce cefalee, grețuri, transpirații, lezare renală, nevrită optică (cataractă).
Note[modificare | modificare sursă]
- ^ „Naftalină”, naphthalene (în engleză), PubChem, accesat în
- ^ http://www.cdc.gov/niosh/npg/npgd0439.html Lipsește sau este vid:
|title=(ajutor) - ^ http://books.google.com.ua/books?id=OmkbNgAACAAJ Lipsește sau este vid:
|title=(ajutor)
| |||||||||||||||||
