Formaldehidă
| Metanal | |
 | |
 | |
 | |
| Denumiri | |
|---|---|
| Alte denumiri | Formaldehidă formalină formol aldehidă metilică oxid de metilenă |
| Identificare | |
| Număr CAS | [50-00-0] |
| ChEMBL | CHEMBL1255 |
| PubChem CID | 712 |
| Informații generale | |
| Formulă chimică | CH2O |
| Aspect | gaz incolor |
| Masă molară | 30,03 g/mol |
| Proprietăți | |
| Densitate | 1 kg/m3 |
| Starea de agregare | gaz |
| Punct de topire | -117 °C |
| Punct de fierbere | -19.3 °C |
| Solubilitate | în apă: > 100 g/100 ml (la 20 °C); în etanol, acetonă: > 100 g/100 ml; solvenți organici în cloroform |
| Presiune de vapori | 3890 mmHg la 25 °C |
| NFPA 704 | |
| Sunt folosite unitățile SI și condițiile de temperatură și presiune normale dacă nu s-a specificat altfel. | |
| Modifică date / text | |
Formaldehida (cu denumirea IUPAC metanal, aldehidă metilică sau aldehidă formică, soluția apoasă de formaldehidă 37% fiind cunoscută și sub numele de formol) este cea mai simplă aldehidă, și este un gaz incolor cu miros înțepător. Formula chimică este H2CO sau CH2O. Formaldehida a fost pentru prima oară sintetizată de chimistul rus Aleksandr Butlerov în 1859 dar a fost identificată abia în 1867, de către August Wilhelm von Hofmann.[1][2]
Formaldehida rezultă din arderea materialelor conținătoare de carbon. Poate fi găsită în focuri forestiere, în eșapamentul automobilelor și în fum de țigară. În atmosfera terestră, formaldehida este produsă de acțiunea luminii solare și a oxigenului asupra metanului și a altor hidrocarburi. Cantități mici de formaldehidă sunt produse de metabolismul multor organisme, inclusiv de cel al omului. Totuși, aceasta este metabolizată la acid formic și nu se acumulează în organism.[3]
Formaldehida este una dintre cele mai vechi substanțe chimice folosite în industrie pentru obținerea rășinilor, folosită apoi în fabricarea plăcilor de lemn[4]. De asemenea, formaldehida este o substanța uzuală în fabricarea echipamentelor sportive, a medicamentelor, a alimentelor, a încălțămintei, a componentelor pentru autovehicule, a hârtiei, a produselor textile, etc[4]. Se estimează că în anul 1996, capacitatea de producție de formaldehidă era de 8,7 milioane de tone pe an.[5]
Germania și Italia sunt țările cu cea mai mare producție anuală de formaldehidă din Uniunea Europeană, asigurând aproximativ 10% din cantitatea produsă anual în lume[4]. Europa de Vest are un consum de 30% din consumul global[4].
Obținere[modificare | modificare sursă]
Laborator[modificare | modificare sursă]
Formaldehida a fost sintetizată pentru prima dată în anul 1859 de către chimistul rus Aleksandr Butlerov (1828–86).[1] Acesta a denumit compusul „dioximetilen” (dioxid de metilen) datorită determinării eronate a formulei empirice (C4H4O4). A fost ulterior identificată de către August Wilhelm von Hofmann, care a anunțat obținerea sa prin trecerea vaporilor de metanol în aer peste un fir de platină încălzit.[2] Abia în anul 1869, Hofmann a determinat formula empirică corectă a formaldehidei.[6][7] Metoda lui Hofmann este încă cea utilizată în industrie, însă a suferit modificări.
O altă metodă aplicabilă la nivel de laborator este reacția de oxidare a metanolului sau a iodurii de metil.[8]
Industrie[modificare | modificare sursă]
Formaldehida este obținută la nivel industrial în urma reacției de oxidare catalitică a metanolului. Cei mai comuni catalizatori sunt argintul metalic sau un amestec de oxizi de fier și molibden sau vanadiu. De obicei, metanolul și oxigenul sunt reacționați la aproximativ 250–400 °C în prezența oxidului de fier și oxidului de molibden/vanadiu, când se obține formaldehida:[5]
Procesul catalizat de argint necesită temperaturi mai ridicate, de aproximativ 650 °C. Pe lângă reacția prezentată mai sus, formaldehida se mai obține în acest caz și datorită următorului proces de dehidrogenare:
Formaldehida s-ar putea obține și prin oxidarea metanului, însă la nivel industrial această metodă nu ar fi foarte practică, deoarece metanul se oxidează mult mai greu decât metanolul.[5]
Proprietăți chimice[modificare | modificare sursă]
Formaldehida este un compus de bază în sinteza organică, fiind un precursor pentru mulți compuși chimici importanți. Prezintă caracterul specific aldehidelor, dar este și mai reactivă.
Auto-condensare și hidratare[modificare | modificare sursă]
Formaldehida, spre deosebire de majoritatea aldehidelor, se oligomerizează spontan. Se obțin trimeri, mai exact 1,3,5-trioxanul, și polimeri, mai exact paraformaldehida. Au fost izolați mulți oligomeri ciclici. Formaldehida se poate și hidrata formând un diol geminal, metandiolul, care se condensează formând HO(CH2O)nH.
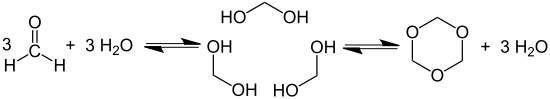
Oxidare[modificare | modificare sursă]
Formaldehida se oxidează la acid formic, care adesea poate să impurifice recipientele.
Hidroximetilare și clorometilare[modificare | modificare sursă]
Formaldehida este un agent electrofil bun, reacționând cu nucleofili precum tioli, amine sau chiar amide, fără necesitatea utilizării de catalizator. Se obțin derivați hidroximetilici care pot fi utilizați în alte reacții. De exemplu, cu aminele se obțin hexahidrotriazine, iar cu hidrogen sulfurat se obține tritian.[9]
În mod analog reacționează și cu apa, dând un produs de hidratare:

În prezența acizilor și arenelor, formaldehida suferă o reacție de substituție electrofilă aromatică, cu obținerea unor derivați hidroximetilați:
Dacă e utilizează acid clorhidric, se obține un derivat de clorometil, conform reacției de clorometilare Blanc:
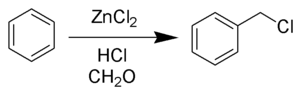
Se pot utiliza și fenoli; dacă sunt substituiți în poziția 4, se obțin calixarene.[10] Se obțin și fenoplaste, precum sunt novolacul și bachelita.
Alte reacții[modificare | modificare sursă]
- Reacția Cannizzaro se face cu catalizatori bazici, și produce acid formic și metanol:

Referințe[modificare | modificare sursă]
- ^ a b Butlerow, A (). Ueber einige Derivate des Jodmethylens [Despre unii derivați ai iodurii de metilen]. Annalen der Chemie und Pharmacie. 111. pp. 242–252.
- ^ a b Vezi: A. W. Hofmann (14 octombrie 1867) "Zur Kenntnis des Methylaldehyds" ([Contribuții] la cunoștințele legate de metilaldehidă), Monatsbericht der Königlich Preussischen Akademie der Wissenschaften zu Berlin, vol. 8, pag. 665–669. Retipărit în:
- A.W. Hofmann, (1868) "Zur Kenntnis des Methylaldehyds", Annalen der Chemie und Pharmacie', vol. 145, no. 3, pag. 357–361.
- A.W. Hofmann (1868) "Zur Kenntnis des Methylaldehyds", Journal für praktische Chemie, vol. 103, no. 1, pag. 246–250.
- ^ „Formaldehyde Is Biodegradable, Quickly Broken Down in the Air By Sunlight or By Bacteria in Soil or Water” (Press release). Formaldehyde Panel of the American Chemistry Council. . Arhivat din original la . Accesat în .
- ^ a b c d Kronospan investeste 10 mil. de euro in platforma proprie, 2 mai 2007, wall-street.ro, accesat la 23 februarie 2010
- ^ a b c Reuss, Günther; Disteldorf, Walter; Gamer, Armin Otto; Hilt, Albrecht (), „Formaldehyde”, Ullmann's Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, doi:10.1002/14356007.a11_619
- ^ Vezi: A.W. Hofmann (5 aprilie 1869) "Beiträge zur Kenntnis des Methylaldehyds", Monatsbericht der Königlich Preussischen Akademie der Wissenschaften zu Berlin, vol. ?, pag. 362–372. Retipărit în:
- Hofmann, A.W. (). „Beiträge zur Kenntnis des Methylaldehyds”. Journal für Praktische Chemie. 107 (1): 414–424. doi:10.1002/prac.18691070161.
- A.W. Hofmann (1869) "Beiträge zur Kenntnis des Methylaldehyds," Berichte der Deutschen Chemischen Gesellschaft, vol. 2, pag. 152–159.
- ^ Read, J. (). Text-Book of Organic Chemistry. London: G Bell & Sons.
- ^ Hooker, Jacob M.; Schönberger, Matthias; Schieferstein, Hanno; Fowler, Joanna S. (). „A Simple, Rapid Method for the Preparation of [11C]Formaldehyde”. Angewandte Chemie International Edition. 47 (32): 5989–5992. doi:10.1002/anie.200800991. PMC 2522306
 . PMID 18604787.
. PMID 18604787.
- ^ Bost, R. W.; Constable, E. W. (), „sym-Trithiane”, Org. Synth., 16: 81; Collective Volume, 2, p. 610
- ^ Gutsche, C. D.; Iqbal, M. (), „p-tert-Butylcalix[4]arene”, Org. Synth.; Collective Volume, 8, p. 75




