Acid aspartic
| Acest articol sau această secțiune are bibliografia incompletă sau inexistentă. Puteți contribui prin adăugarea de referințe în vederea susținerii bibliografice a afirmațiilor pe care le conține. |
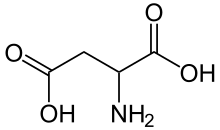
| Acid aspartic | |
 | |
 | |
| Nume IUPAC | acid 2-aminobutandioic |
|---|---|
| Alte denumiri | acid aminosuccinic |
| Identificare | |
| Număr CAS | 617-45-8 |
| ChEMBL | CHEMBL274323 |
| PubChem CID | 5960 |
| Informații generale | |
| Formulă chimică | C4H7NO4 |
| Aspect | cristale incolore |
| Masă molară | 133,1 g/mol |
| Starea de agregare | solidă |
| Punct de topire | 270 °C |
| Punct de fierbere | 340 °C |
| Sunt folosite unitățile SI și condițiile de temperatură și presiune normale dacă nu s-a specificat altfel. | |
| Modifică date / text | |
Acidul aspartic (abreviat Asp sau D), este unul din cei 20 aminoacizi proteinogeni. Codonii sai sunt GAU și GAC. Acesta este un aminoacid ne-esențial. Aspartatul, baza conjugata a acidului aspartic, este un neurotransmițător important care joacă un rol important în potențarea pe termen lung (LTP) și este important în procesele de învățare și memorie, deși într-o măsură mult mică decât glutamatul. Acidul aspartic a fost descoperit în 1827 de către Plisson, atunci când acesta a fiert sparanghel (de unde și vine numele acidului) în soluție bazică concentrată.
Rol[modificare | modificare sursă]
Aspartatul este un aminoacid ne-esențial la mamifere, fiind sintetizat pornind de la oxaloacetat prin transaminare.
- Este un metabolit din ciclul ureei, rezultând din ornitină și citrulină.
- În plante și microorganisme, aspartatul este precursorul mai multor aminoacizi, inclusiv patru care sunt esențiali pentru om: metionina, treonina, izoleucina, și lizina.
- Neurotransmițător excitator; acționează asupra receptorilor NMDA, dar are efecte mai slabe decât glutamatul;
- Gluconeogeneză (sinteza glucozei);
- Sistemul navetă malat-aspartat (glicoliză);
- Sinteza bazelor purinice.
| |||||||||||||||||||||||||||||||

