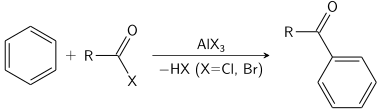Substituție electrofilă aromatică
Substituția electrofilă aromatică (SEAr) este un tip de reacție chimică organică prin care un atom care face parte din nucleul aromatic (de obicei cel de hidrogen) este substituit de un electrofil. Unele dintre cele mai importante astfel de substituții electrofile la nucleul aromatic sunt: nitrarea aromatică, halogenarea aromatică, sulfonarea aromatică și reacțiile Friedel-Crafts de acilare și alchilare.[1][2]
Forma generală a acestui tip de reacție este:
- ArH + EX → ArE + HX
Exemple
[modificare | modificare sursă]Unul dintre cele mai ilustrative exemple de substituție electrofilă aromatică este reacția de etilare a benzenului:
Aproximativ 24.700.000 de tone au fost produse în 1999.[3] După dehidrogenare și polimerizare, se obține un compus foarte important, polistirenul.
Nitrarea benzenului are loc ca urmare a acțiunii ionului nitroniu asupra electrofilului. Sulfonarea duce la formarea de acid benzensulfonic. Halogenarea se poate face cu brom, clor sau iod, când se obțin halogenurile de aril corespunzătoare. Această reacție de halogenarea este catalizată de trihalogenurile de fier sau de aluminiu corespunzătoare halogenului (FeX3, AlX3):
Reacțiile Friedel-Crafts pot să aibă loc fie sub formă de acilare, fie sub formă de alchilare. De obicei, se folosește clorura de aluminiu ca și catalizator, dar la fel de bine poate fi utilizat orice acid Lewis. Se obțin acilbenzeni și alchilbenzeni:
Mecanism de reacție
[modificare | modificare sursă]Mecanismul general al reacției de substituție electrofilă aromatică, notat cu SEAr,[4] începe cu atacul electrofil al speciei E+ asupra nucleului aromatic, etapă notată cu 1. Această etapă conduce la formarea unui cation ciclohexadienil delozalizat, denumit și ion areniu sau complex σ (sigma), notat cu 2b. În condiții normale de reacție, această specie puternic acidă va dona protonul legat de atomul de carbon hibridizat sp3 solventului (sau oricărei baze mai slabe) cu scopul restabilirii aromaticității. Acest fapt are ca urmare substituirea atomului de H cu specia E pe nucleul aromatic. În unele cazuri, unele grupe pot pleca de pe nucleu fără perechea de electroni, de exemplu: grupe silil (precum SiR3+), grupe carboxi (ca COO + H+), grupe iodo (precum I+), și grupe alchil precum terț-butil (ca R+).
Vezi și
[modificare | modificare sursă]Referințe
[modificare | modificare sursă]- ^ Smith, Michael B.; March, Jerry (2007), Advanced Organic Chemistry: Reactions, Mechanisms, and Structure (ed. 6), New York: Wiley-Interscience, ISBN 0-471-72091-7
- ^ Florin Badea (1973) Mecanisme de reacție în chimia organică (ed. 2), București: Editura Științifică; pag.324-398
- ^ Vincent A. Welch, Kevin J. Fallon, Heinz-Peter Gelbke "Ethylbenzene" Ullmann’s Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, 2005. doi:10.1002/14356007.a10_035.pub2
- ^ Gawley, Robert E. (). „A proposal for (slight) modification of the Hughes–Ingold mechanistic descriptors for substitution reactions”. Tetrahedron Letters. 40 (23): 4297–4300. doi:10.1016/S0040-4039(99)00780-7. ISSN 0040-4039.
Legături externe
[modificare | modificare sursă]
| ||||||||||||||||||||