Cristal lichid

Cristalele lichide (LCs) sunt o materie aflată într-o stare de agregare în care are proprietăți între cele ale lichidelor convenționale și cele ale cristalelor solide.[1] De exemplu, un cristal lichid poate curge ca un lichid, dar moleculele pot fi orientate pe o anume direcție, ca într-un cristal. Există mai multe tipuri diferite de faze de cristal lichid, care pot fi distinse prin diferite proprietăți optice (cum ar fi birefringența). Atunci când este privit sub un microscop, folosind o sursă de lumină polarizată, diferitele faze ale cristalului lichid vor părea să aibă texturi(d) distincte. Zonele contrastante din texturi corespund cu domeniile în care moleculele de cristal lichid sunt orientate în direcții diferite. În interiorul unui domeniu, moleculele sunt însă bine ordonate. Materialele ce pot avea stări de cristal lichid pot să nu fie întotdeauna într-o fază de cristal lichid (la fel cum apa se poate transforma în gheață sau abur).
Cristalele lichide pot fi împărțite în faze termotrope(d), liotropice(d) și metalotropice. Cristalele lichide termotrope și liotropice sunt formate în mare parte din molecule organice, deși sunt cunoscute și câteva minerale. Cristalele lichide termotrope prezintă o tranziție de fază în faza de cristal lichid, la schimbarea temperaturii. Cele liotropice prezintă tranziții de fază în funcție de temperatură și concentrația de molecule de cristal lichid într-un solvent (de obicei apa). Cele metalotropice sunt compuse din molecule organice și anorganice; tranziția lor către faza de cristal lichid depinde nu numai de temperatură și concentrație, ci și de raportul de compoziție între moleculele anorganice și cele organice.
Exemple de cristale lichide pot fi găsite atât în lumea naturală, cât și în aplicații tehnologice. Majoritatea afișajelor electronice(d) contemporane folosesc cristale lichide. Fazele liotropice sunt abundente în sistemele vii, dar pot fi găsite și în lumea minerală. De exemplu, multe proteine și membrane celulare sunt cristale lichide. Alte exemple bine-cunoscute de cristale lichide sunt soluțiile de săpun și de diverși detergenți, precum și virusul mozaicului tutunului(d), și unele argile.
Istorie[modificare | modificare sursă]
În 1888, fiziologul botanist austriac Friedrich Reinitzer, care lucra la Karl-Ferdinands-Universität, a examinat proprietățile fizico-chimice ale diferitelor derivate de colesterol, care acum fac parte din clasa materialelor cunoscute sub numele de cristale lichide colesterice. Anterior, alți cercetători au observat efecte distincte de culoare, atunci când se răcesc derivatele de colesterol până aproape de punctul de congelare, dar nu le asociaseră cu un fenomen nou. Reinitzer a înțeles că modificările de culoare din benzoatul de colesteril(d) nu sunt cele mai neobișnuită trăsătură.

El a constatat că benzoatul de colesteril nu se topește în același mod ca și alți compuși, ci are două puncte de topire. La 145.5 °C se topește într-un lichid tulbure, și la 178.5 °C se topește din nou și lichidul tulbure devine limpede. Fenomenul este reversibil. Căutând ajutorul unui fizician, pe 14 martie 1888, el i-a scris lui Otto Lehmann(d), la acel moment Privatdozent(d) la Aachen. Au făcut schimb de scrisori și de probe. Lehmann a examinat lichidul tulbure intermediar și a văzut cristalite(d). Colegul vienez al lui Reinitzer, von Zepharovich, a indicat și el că lichidul intermediar este cristalin. Schimbul de scrisori cu Lehmann s-a încheiat pe 24 aprilie, multe întrebări rămânând fără răspuns. Reinitzer și-a prezentat rezultatele, creditându-i pe Lehmann și von Zepharovich, la o reuniune a Societății de Chimie din Viena la 3 mai 1888.[2]
Până în acel moment, Reinitzer descoperise și descrisese și alte trei caracteristici importante ale cristalelor lichide colesterice (nume inventat de Otto Lehmann în 1904): existența a două puncte de topire, reflectarea luminii polarizate circular(d), și capacitatea de a roti direcția de polarizare a luminii.
După descoperirea accidentală, Reinitzer nu a mai urmărit studierea cristalelor lichide. Cercetarea a fost continuată de Lehmann, care a realizat că a întâlnit un fenomen nou și că este în postura de a-l investiga: în anii postdoctorali, el dobândise expertiză în cristalografie și microscopie. Lehmann a început un studiu sistematic, mai întâi asupra benzoatului de colesteril, și apoi asupra unor compuși înrudiți care prezentau fenomenul de dublă topire. El a reușit să facă observații în lumină polarizată, și microscopul lui era echipat cu etapă fierbinte (susținător de eșantion echipat cu încălzitor) pentru a-i permite observații la temperaturi ridicate. Faza tulbure intermediară susținea în mod cert curgerea, dar alte caracteristici, cum ar fi signatura sub microscop, l-a convins pe Lehmann că are de a face cu un solid. Până la sfârșitul lunii august 1889, el și-a publicat rezultatele în Zeitschrift fuer Physikalische Chemie(d).[3]

Munca lui Lehmann a fost continuată și extinsă în mod semnificativ de către chimistul german Daniel Vorländer(d), care, de la începutul secolului al XX-lea și până la pensionarea sa în anul 1935, a sintetizat cele mai multe dintre cristalele lichide cunoscute. Cu toate acestea, cristalele lichide nu erau populare în rândul oamenilor de știință și materialul a rămas o curiozitate științifică timp de aproximativ 80 de ani.[4]
După al Doilea Război Mondial, lucrul la sinteza de cristale lichide a fost reluat la laboratoarele universitare de cercetare din Europa. George William Gray(d), un cercetător important în domeniul cristalelor lichide, a început investigarea acestor materiale în Anglia la sfârșitul anilor 1940. Grupul lui a sintetizat multe materiale noi, care prezentau starea lichid-cristalină și a dezvoltat o mai bună înțelegere a modului de a proiecta molecule care prezintă această stare. Cartea sa Structura moleculară și proprietățile cristalelor lichide[5] a devenit manual în acest subiect. Unul dintre primii chimiști americani care a studiat cristalele lichide a fost Glenn H. Brown, începând din anul 1953, la Universitatea din Cincinnati și mai târziu, la Universitatea de Stat Kent(d). În 1965, el a organizat prima conferință internațională pe tema cristalelor lichide, la Kent, Ohio, la care au participat circa 100 de cercetători de top ai cristalelor lichide. Această conferință a marcat începutul unui efort la nivel mondial pentru a efectua cercetări în acest domeniu, care în curând a condus la dezvoltarea de aplicații practice pentru aceste materiale unice.[6][7]
Cristalele lichide au devenit subiect de cercetare în dezvoltarea afișajelor electronice plate începând cu anul 1962, la RCA Laboratories.[8] Când chimistul-fizician Richard Williams a aplicat un câmp electric unui strat subțire de cristal lichid nematic la 125 °C, el a observat formarea unui model regulat pe care el l-a numit „domeniu” (astăzi denumit „domeniu Williams”). Aceasta l-a condus pe colegul său, George H. Heilmeier(d) să efectueze cercetări în vederea dezvoltării unui panou de afișaj plat cu cristale lichide pentru a înlocui tuburile catodice vidate utilizate în televizoare. Dar para-azoxianisolul(d) pe care îl foloseau Williams și Heilmeier prezenta stare de cristal lichid nematic numai la peste 116 °C, ceea ce făcea imposibilă utilizarea sa într-un sistem de afișare comercial. Era nevoie de un material care putea funcționa la temperatura camerei.
În 1966, Joel E. Goldmacher și Joseph A. Castellano, cercetători chimiști în grupul Heilmeier de la RCA, a descoperit că amestecurile realizate exclusiv din compuși nematici care diferă doar în numărul de atomi de carbon în partea terminală a lanțurilor ar putea produce cristale lichide nematice la temperatura camerei. Un amestec ternar de compuși de bază Schiff a avut ca rezultat un material care avea o gamă nematică de 22-105 °C.[9] Funcționarea la temperatura camerei a permis producția primului dispozitiv practic de afișare cu cristale lichide.[10] Echipa a început apoi să pregătească numeroase amestecuri de compuși nematici, dintre care mulți aveau puncte de topire mult mai mici. Aceasta tehnică de amestecare a compușilor nematici pentru a obține o gamă largă de temperaturi de funcționare(d) a devenit în cele din urmă standard în industrie și este folosită până astăzi pentru a adapta materialele pentru a satisface anumite aplicații.
În 1969, Hans Kelker reușit să sintetizeze o substanță care are fază nematică la temperatura camerei, MBBA(d), una dintre cele mai populare subiecte de cercetare a cristalelor lichide.[11] Pasul următor către comercializarea afișajelor cu cristale lichide a fost sinteza unor substanțe chimice stabile (cianobifenili) cu temperaturi de topire scăzute, de către George Gray(d).[12] Munca sa împreună cu Ken Harrison și UK MOD (RRE Malvern(d)), în 1973, a condus la proiectarea de noi materiale și la adoptarea rapidă a LCD-urilor cu suprafață mică în produsele electronice.
Aceste molecule sunt în formă de tijă, unele create în laborator și unele apărute spontan în natură. De atunci, au fost descoperite două noi tipuri de molecule LC, ambele artificiale: în formă de disc (create de grupul lui S. Chandrasekhar în India, 1977)[necesită citare] și cele în formă de castron (inventate de Lui Lam[13] în China, 1982, și sintetizate în Europa trei ani mai târziu).
În 1991, când afișajele cu cristale lichide erau deja bine stabilite, Pierre-Gilles de Gennes, care lucra la Universitatea Paris-Sud, a primit Premiul Nobel pentru Fizică „pentru descoperirea faptului că metodele dezvoltate pentru a studia fenomene în sisteme simple pot fi generalizate la forme mai complexe de materie, în special cu cristale lichide și polimeri”.[14]
Designul materialelor lichid-cristaline[modificare | modificare sursă]
Se cunosc un număr mare de compuși chimici care prezintă una sau mai multe faze de cristal lichid. În ciuda diferențelor semnificative de compoziție chimică, aceste molecule au unele caracteristici comune în proprietăți fizice și chimice. Există trei tipuri de cristale lichide termotrope: discotice, calamitice și cele în formă de castron. Discoticele sunt molecule în formă de disc plat formate dintr-un miez de inele aromatice adiacente; cele în formă de castron au o formă tridimensională .[15][16] Acest lucru permite o ordonare bidimensională pe coloane, atât pentru cele discotice cât și pentru cele în formă de castron. Moleculele calamitice (în formă de tijă) au o geometrie alungită, anizotropă, care permite alinierea preferențială(d) de-a lungul unei direcții spațiale.
- Forma moleculară ar trebui să fie relativ subțire, plată sau de castron, mai ales în cadre moleculare rigide.
- Lungimea moleculară trebuie să fie de cel puțin 1,3 nm, în concordanță cu prezența grupurilor alchil lungi pe multe cristale lichide la temperatura camerei.
- Structura nu ar trebui să fie ramificată sau unghiulară, cu excepția moleculelor în formă de castron.
- Un punct de topire scăzut este de preferat pentru a evita fazele lichid-cristaline metastabile, monotrope. Comportamentul mezomorfic la temperaturi scăzute este de obicei mai util din punct de vedere tehnologic, și grupurile terminale alchi promovează acest lucru.
O formă extinsă, rigidă din punct de vedere structural, extrem de anizotropă pare a fi principalul criteriu pentru comportamentul cristalelor lichide, și, ca rezultat, multe materiale lichid-cristaline sunt bazate pe inele de benzen.[17]
Fazele de cristal lichid[modificare | modificare sursă]
Diversele faze de cristal lichid (numite mezofaze(d)) pot fi caracterizate prin tipul de ordonare. Se pot distinge ordinea pozițională (dacă moleculele sunt aranjate în vreo structură ordonată) și ordinea de orientare (dacă moleculele sunt în mare parte orientate în aceeași direcție). Mai mult, ordinea poate fi fie cu rază scurtă de acțiune (numai între moleculele apropiate una de alta) sau cu rază lungă (extindere mai mare, uneori la dimensiuni macroscopice). Majoritatea cristalelor lichide termotrope vor avea o fază izotropă la temperaturi ridicate, adică încălzirea le va transforma în cele din urmă într-o fază de lichid convențional caracterizată prin ordonare moleculară aleatoare și izotropă (fără vreo ordine pe scară largă), și cu comportament de curgere similar oricărui lichid. În alte condiții (de exemplu, la temperatură mai mică), un cristal lichid ar putea popula una sau mai multe faze, cu structură de orientare anizotropă semnificativă și cu ordonare de orientare pe scară redusă, în timp ce încă mai are o capacitatea de a curge.[1][18]
Ordonarea fazelor de cristal lichid este extinsă la scară moleculară. Această ordine se extinde la dimensiunea întregului domeniu, care poate fi de ordinul micrometrilor, dar de obicei nu se extinde la scară macroscopică la fel de des ca în cazul cristalelor solide clasice. Cu toate acestea, unele tehnici, cum ar fi utilizarea de limite sau aplicarea unui câmp electric pot fi folosite pentru a aplica un singur domeniu de ordonare la nivelul unui eșantion macroscopic de cristale lichide. Ordonarea într-un cristal lichid s-ar putea extinde de-a lungul unei singure dimensiuni, materialul fiind, în esență, dezordonat în celelalte două direcții.[19][20]
Cristale lichide termotrope[modificare | modificare sursă]
Fazele termotrope sunt cele care apar într-un anumit interval de temperatură. Dacă creșterea temperaturii este prea mare, agitația termică va distruge ordonarea cooperativă a fazei de cristal lichid, împingând materialul într-o fază lichidă izotropă convențională. La temperatură prea scăzută, cele mai multe materiale vor forma cristale convenționale.[1][18] Multe cristale lichide termotrope prezintă o varietate de faze pe măsura variației temperaturii. De exemplu, la încălzire un anumit tip de molecule cu cristale lichide (numite mezogene(d)) pot prezenta diferite faze smectice, urmate de faza nematică și în cele din urmă de cea izotropă, pe măsură ce temperatura este crescută. Un exemplu de compus ce prezintă comportament de cristal lichid termotrop este para-azoxianisolul(d).[21]
Faza nematică[modificare | modificare sursă]


Una dintre cele mai comune faze a cristalelor lichide este cea nematică. Cuvântul nematic vine din grecescul νήμα (cu litere latine, nema), care înseamnă „fir”. Acest termen provine de la defectele topologice(d) observate în nematice, denumite oficial „disclinații(d)”. Nematicele prezintă și așa-numitele defecte topologice „arici”. Într-o fază nematică, moleculele organice calamitice (în formă de tijă) nu au ordine pozițională, dar se auto-aliniază pentru a avea o ordine direcțională la scară mare cu axele mai lungi aproximativ paralele.[22] Astfel, moleculele sunt libere să curgă și pozițiile centrelor lor de masă sunt distribuite la întâmplare, ca într-un lichid, dar ele își mențin în continuare ordinea direcțională pe scară largă. Majoritatea nematicelor sunt uniaxiale: au o singură axă care este mai lungă și preferată, celelalte două fiind echivalente (poate fi aproximată cu un cilindru). Cu toate acestea, unele cristale lichide sunt nematice biaxial(d), în sensul că, în plus față de orientarea axei mai lungi, ele se orientează și de-a lungul unei axe secundare.[23] Nematicele au fluiditate similară cu cea a lichidelor obișnuite (izotrope) dar ele pot fi ușor aliniate de un câmp electric sau magnetic extern. Nematicele aliniate au proprietățile optice ale cristalelor uniaxiale și acest lucru le face extrem de utile în ecranele cu cristale lichide (LCD).[8]
Fazele smectice[modificare | modificare sursă]

Fazele smectice, care se găsesc la temperaturi mai mici decât cea nematică, formează straturi bine definite care pot aluneca unul peste altul într-o manieră similară cu cea în care alunecă săpunul. Cuvântul „smectic” provine de la cuvântul latin „smecticus”, care înseamnă „curățare”, sau cu proprietăți ca săpunul.[24] Smecticele sunt astfel ordonate pozițional de-a lungul unei singure direcții. În faza smectică A, moleculele sunt orientate de-a lungul normalei la strat, în timp ce în faza smectică C, ele sunt înclinate față de aceasta. Aceste faze sunt asemănătoare lichidelor doar între straturi. Există multe faze smectice diferite, toate caracterizate de diferite tipuri și grade de ordonare pozițională și orientațională.[1][18]
Faze chirale[modificare | modificare sursă]

Faza chirală nematică prezintă chiralitate (preferință pentru dreapta/stânga). Această fază este adesea numită fază colesterică(d) pentru că a fost observată pentru prima dată ala derivații colesterolului. Numai moleculele chirale (adică, cele care nu au plane interne de simetrie) poate da naștere la o astfel de fază. Această fază prezintă o răsucire a moleculelor perpendicular pe directoare, cu axa moleculară paralelă cu directoarea. Unghiul finit de răsucire între moleculele adiacente este cauzat de aglomerarea lor asimetrică, care are ca rezultat ordine chirală pe scară mai mare. În faza smectică C* (asteriscul denotă fază chirală), moleculele au ordonare pozițională într-o structură stratificată (ca și în alte faze smectice), cu moleculele înclinate la un anumit unghi în raport cu normala la strat. Chiralitatea induce o răsucire finită azimutală de la un strat la altul, care la rândul ei produce o răsucire în spirală a axei moleculare în jurul normalei la strat.[18][19][20]
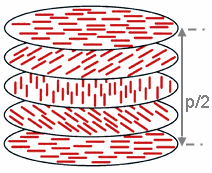
Perioada chiralei, p, se referă la distanța la care moleculele de cristal lichid suferă o răsucire totală de 360° (dar structura fazei chirale nematice se repetă la fiecare jumătate de perioadă, deoarece în această fază directoarele de 0° și ±180° sunt echivalente). Perioada p se schimbă de regulă atunci când se modifică temperatura sau când se adaugă alte molecule la materialul gazdă (un material-gazdă achiral va forma o fază chirală dacă este dopat cu o material chiral), permițând perioadei unui anumit material să fie reglată corespunzător. În unele sisteme de cristale lichide, perioada este de același ordin de mărime ca lungimea de undă a luminii vizibile. Acest lucru face ca aceste sisteme să prezinte proprietăți optice unice, cum ar fi reflexiile Bragg și emisii laser cu prag scăzut,[25] și aceste proprietăți sunt exploatate în mai multe aplicații optice.[4][19] Pentru cazul reflexiilor Bragg, doar reflexia de cel mai mic ordin este permisă dacă lumina este incidentă de-a lungul axei elicoidale, în timp ce pentru incidențe oblice de ordin superior, reflexiile devin permise. Cristalele lichide nematice prezintă și proprietatea unică că reflectă lumina polarizată circular atunci când ea este incidentă de-a lungul axei elicoidale, și pe cea polarizată eliptic(d) dacă ea cade într-un unghi oblic.[26]
Fazele albastre sunt faze de cristal lichid care apar în intervalul de temperatură între o fază chirală nematică fază și una lichidă izotropă. Fazele albastre au o structură tridimensională cubică de defecte cu perioade ale structurii cristaline de câteva sute de nanometri, și, astfel, ele prezintă reflexii Bragg(d) selective în gama de lungimi de undă a luminii vizibile corespunzătoare structurii cristaline cubice. S-a prezise teoretic în 1981 că aceste faze pot poseda simetrie icosahedrală similară cu quasicristalele(d).[27][28]
Deși fazele albastre sunt de interes pentru modulatoarele rapide de lumină sau pentru cristalele fotonice(d) acordabile, ele există într-o gamă foarte îngustă de temperaturi, de obicei, de mai puțin de câteva grade kelvin. Recent, s-a demonstrat stabilizarea fazelor albastre pe un interval de temperatură mai mare de 60 K, inclusiv la temperatura camerei (260-326 K).[29][30] Fazele albastre stabilizate la temperatura camerei permit comutare electro-optică cu timpi de răspuns de ordinul a 10-4 s.[31]
În mai 2008, a fost dezvoltat primul ecran LCD cu fază albastră(d).[32]
Faze discotice[modificare | modificare sursă]
Moleculele de cristal lichid în formă de disc se pot orienta într-un strat, manieră cunoscută ca fază discotică nematică. Discurile se pot grupa unul peste altul, formând coloane. Coloanele pot fi organizate în tablouri dreptunghiulare sau hexagonale. Sunt cunoscute și faze chirale discotice, similare celei chirale nematie.
Cristale lichide liotrope[modificare | modificare sursă]

Un cristal lichid liotrop(d) este format din două sau mai multe componente care prezintă proprietăți lichid-cristaline în anumite intervale de concentrație. În fazele liotrope(d), moleculele de solvent umplu spațiul din jurul compușilor pentru a oferi fluiditate sistemului.[33] În contrast cu cristalele lichide termotrope, cele liotrope au un alt grad de libertate, al concentrației, care le permite să inducă o varietate de faze diferite.
Un compus care are două părți nemiscibile, una hidrofilă și alta hidrofobă, în aceeași moleculă se numește o moleculă amfifilă. Multe molecule amfifile prezintă secvențe de faze lichid-cristaline liotrope în funcție de echilibrul volumetric între părțile hidrofilă și hidrofobă. Aceste structuri sunt formate prin segregarea micro-fazelor a două componente incompatibile pe scară nanometrică. Săpunul este un exemplu cotidian de cristal lichid liotrop.
Conținutul de molecule de apă sau alt solvent schimbă structurile auto-asamblate. La concentrații amfifile foarte scăzute, moleculele se vor dispersa aleatoriu, fără nici o ordonare. La concentrații puțin mai mari (dar încă scăzute), moleculele amfifile se vor asambla spontan în micele sau vezicule(d). Acest lucru se face în așa fel încât să „ascundă” partea hidrofobă din amfifilă în interiorul micelelor de bază, expunând o suprafață hidrofilă (solubilă în apă) pentru soluția apoasă. Aceste obiecte sferice nu se ordonează ele însele în soluție. La concentrație mai mare, ansamblurile vor deveni ordonate. Un exemplu tipic de fază este o fază colonară hexagonală, unde amfifilele formează cilindri lungi (din nou, cu o suprafață hidrofilă), care se aranjează în structuri aproximativ hexagonale. La concentrații și mai mari, se poate forma o fază lamelară, în care foi întinse de amfifile sunt separate de straturi subțiri de apă. Pentru unele sisteme, poate exista și o fază cubică (vâscos izotropă) între cea hexagonală și cea lamelară, în care se formează sfere care creează o densă rețea cubică. Aceste sfere pot fi legate și una de alta, formând o fază cubică bicontinuă.
Obiectele create de amfifile sunt, de obicei, sferice (ca în cazul micelelor), dar pot fi și în formă de disc (bicele), tijă, sau biaxiale (cu toate trei axele distincte). Aceste nano-structuri anizotrope auto-asamblate se pot apoi ordona la fel ca și cristalele lichide termotrope, formând versiuni la scară mare ale tuturor fazelor termotrope (cum ar fi o fază nematică de micele în formă de tijă).
Pentru unele sisteme, la concentrații mari, se observă și faze inverse, adică se poate genera o fază colonară hexagonală inversă (coloane de apă încapsulate în amfifile) sau o fază micelară inversă (un eșantion masiv de cristal lichid cu cavități sferice de apă).
P progresie generică a fazelor, de la concentrație de amfifilă mică la concentrație mare, este:
- Faza cubică discontinuă (faza micelară cubică(d))
- Faza hexagonală(d) (faza colonară hexagonală; de mijloc)
- Faza lamelară(d)
- Faza cubică bicontinuă
- Faza colonară hexagonală inversă
- Faza cubică inversă (faza micelară inversă)
Chiar și în cadrul aceleiași faze, structurile auto-asamblate sunt acordabile prin concentrație: de exemplu, în fazele lamelare, distanțele între straturi cresc cu volumul de solvent. Deoarece cristalele liotrope se bazează pe un echilibru subtil al interacțiunilor intermoleculare, este mult mai dificilă analiza structurilor și proprietățile acestora decât a celor ale cristalelor lichide termotrope.
Faze și caracteristici similare pot fi observate în copolimerii nemiscibili dibloc.
Cristale lichide metalotrope[modificare | modificare sursă]
Fazele cristalelor pot fi bazate și faze anorganice cu punct de topire scăzut, ca ZnCl2, care au o structură formată din tetraedre legate și formează cu ușurința sticlă. Adăugarea unor molecule cu lanțuri lungi, similare săpunului, duce la o serie de noi faze care prezintă o varietate de comportamente lichid-cristaline atât ca funcție de compoziția anorganic-organică cât și de raportul de temperatură. Această clasă de materiale se numesc metalotrope.[34]
Analiza de laborator a mezofazelor[modificare | modificare sursă]
Mezofazele(d) termotrope sunt detectate și caracterizate prin două metode majore, metoda originală a fost utilizarea microscopiei optice termice, în care un mic eșantion de material era plasat între două polarizatoare încrucișate; proba era apoi încălzită și răcită. Cum faza izotropă nu ar afecta în mod semnificativ polarizarea luminii, ea ar părea foarte întunecată, întrucât fazele cristalină și lichid-cristalină vor polariza lumina într-un mod uniform, ceea ce duce la gradiente de luminozitate și de culoare. Această metodă permite caracterizarea fazei particulare, întrucât diferitele faze sunt definite prin ordine specifică, care trebuie să fie observată. Cea de-a doua metodă, calorimetria diferențială, permite o determinare mai exactă a tranzițiilor de fază și a entalpiilor de tranziție. Un mic eșantion este încălzit într-un mod care generează o schimbare foarte precisă a temperaturii în raport cu timpul. În timpul tranzițiilor de fază, fluxul de căldură necesar pentru a menține această rată de încălzire sau răcire se va schimba. Aceste modificări pot fi observate și li se pot atribui diferite tranziții de fază, cum ar fi tranzițiile-cheie ale cristalelor lichide.
Mezofazele liotrope sunt analizate într-o manieră similară, deși aceste experimente sunt ceva mai complexe, întrucât concentrația de mezogen este un factor-cheie. Aceste experimente sunt efectuate la diferite concentrații de mezogen(d) în scopul de a le analiza impactul.
Cristale lichide biologice[modificare | modificare sursă]
Fazele lichid-cristaline liotrope sunt abundente în sistemele vii, studiul cărora este denumit polimorfism lipidic(d). În consecință, cristalele lichide liotrope atrag atenția în mod deosebit în domeniul chimiei biomimetice. În special, membranele biologice și membranele celulare sunt o formă de cristale lichide. Moleculele lor constitutive (de exemplu, fosfolipidele) sunt perpendiculare pe suprafața membranei, dar membrana este flexibilă. Aceste lipide au forme diverse. Moleculele constituente pot să se amestece între ele cu ușurință, dar nu au tendința de a părăsi membrana din cauza nivelului ridicat de energie necesar acestui proces. Moleculele lipidice se pot întoarce de pe o parte a membranei pe alta. Aceste faze lichid-cristaline membranare pot găzdui și proteine importante, cum ar fi receptorii care „plutesc” liber în interiorul, sau parțial în afara membranei, de exemplu, CCT.
Multe alte structuri biologice prezintă comportament de cristale lichide. De exemplu, o soluție de proteine concentrată care este extrudată de un păianjen pentru a genera mătase este, în fapt, un cristal lichid. Ordonarea exactă a moleculelor mătăsii este esențială pentru renumita lor rezistență. ADN-ul și multe polipeptide pot forma și ele faze de cristal lichid, aceasta reprezentând o parte importantă a cercetării academice actuale.
Cristale lichide minerale[modificare | modificare sursă]
Se pot găsi exemple de cristale lichide și în lumea minerală, cele mai multe dintre ele fiind liotrope. Primul descoperit a fost oxidul de vanadiu (V)(d), de către Zocher în 1925.[35] De atunci, alte câteva au mai fost descoperite și studiate în detaliu.[36] Existența unei faze nematice reale în cazul familiei argilelor smectice a fost avansată de către Langmuir în 1938,[37] dar a rămas deschisă pentru o foarte lungă perioadă de timp și rezolvată doar recent.[38][39] Odată cu dezvoltarea rapidă a nanoștiințelor, și a sintezei de nanoparticule anizotrope, numărul de astfel de minerale cristale lichide este în creștere rapidă, de exemplu, cu nanotuburile de carbon și grafen. A fost descoperită o fază lamelară, H3Sb3P2O14, care prezintă hiperumflare până la ~250 nm pentru distanța interlamelară.[40]
Formarea de modele în cristalele lichide[modificare | modificare sursă]
Anizotropia cristalelor lichide este o proprietate neobservată la alte lichide. Această anizotropie face ca curgerea cristalelor lichide să se comporte mai diferențiat decât a fluidelor obișnuite. De exemplu, injectarea unui flux de cristal lichid între două plăci paralele determină o orientare a moleculelor cuplată cu curgerea, rezultatul fiind apariția unor modele dendritice.[41] Această anizotropie se manifestă și în tensiune superficială între diferite faze de cristal lichid. Această anizotropie determină forma de echilibru la temperatură de coexistență, și este atât de puternică încât de obicei apar forme. Atunci când temperatura este schimbată, una din faze creste, formând morfologii diferite în funcție de schimbările de temperatură.[42] Întrucât creșterea este controlată de difuzia căldurii, anizotropia în conductivitatea termică favorizează creșterea în direcții specifice, ceea ce are și ea efect asupra formei finale.[43]
Tratarea teoretică a cristalelor lichide[modificare | modificare sursă]
Tratarea teoretică microscopică a fazelor fluide poate deveni destul de complicată, din cauza densității crescute de material, în sensul că interacțiunile puternice nu pot fi ignorate. În cazul cristalelor lichide, anizotropia tuturor acestor interacțiuni complică analiza și mai mult. Există mai multe teorii simple, totuși, care cel puțin prezic comportamentul general al tranzițiilor de fază în sistemele cu cristale lichide.
Directoarea[modificare | modificare sursă]
După cum am văzut deja mai sus, cristalele nematice sunt compuse din molecule cilindrice, având axele lungi aproximativ aliniate între moleculele vecine. Pentru a descrie această structură anizotropă, se introduce un vector unitar adimensional n numit directoare, pentru a reprezenta direcția preferată a orientării moleculelor în apropiere de orice punct. Pentru că nu există polaritate fizică (nu contează sensul, ci doar direcția) de-a lungul axei directoare, n și -n sunt complet echivalente.[18]
Parametrul de ordine[modificare | modificare sursă]

Descrierea cristalelor lichide implică o analiză a ordinii. Un parametru de ordine sub forma unui tensor simetric de rangul al doilea este folosit pentru a descrie ordinea orientațională a unui cristal lichid nematic, deși un parametru scalar este de obicei suficient pentru a descrie cristalele lichide uniaxiale. Pentru a conferi o cantitate, parametrul de ordine orientațională este, de obicei, definit pe baza mediei celui de al doilea polinom Legendre:
unde este unghiul dintre axele moleculare ale cristalului lichid și directoarea locală (adică direcția preferată într-un element de volum al unui eșantion de cristal lichid reprezentând și axa sa optică locală). Parantezele indică medierea atât temporală cât și spațială. Această definiție este convenabilă, deoarece pentru un eșantion complet aleator și izotrop, S=0, în timp ce pentru un eșantion perfect aliniat S=1. Pentru un eșantion tipic de cristal lichid, S este între 0,3 și 0,8, și, în general, scade cu cât temperatura este mai ridicată. În special, o scădere bruscă a parametrului de ordine la 0 se observă atunci când sistemul trece printr-o tranziție de fază de la o fază de cristal lichid la una izotropă.[44] Parametrul de ordonare poate fi măsurat experimental într-o serie de moduri; de exemplu, diamagnetismul, birefringența, împrăștierea Raman(d), RMN și RES pot fi folosite pentru a determina S.[20]
Ordinea într-un cristal lichid poate fi caracterizată și prin utilizarea altor polinoame Legendre de grad par (toate polinoamele de grad impar au media zero pentru că directoarea poate fi îndreptată în oricare dintre cele două direcții antiparalele). Aceste medii de ordin superior sunt mai dificil de măsurat, dar pot aduce informații suplimentare despre ordonarea moleculară.[1]
Un parametru de ordine pozițională mai este folosit pentru a descrie ordonarea unui cristal lichid. Acesta este caracterizat prin variația densității centrului de masă al moleculelor de cristal lichid de-a lungul unui vector. În caz de variație pozițională de-a lungul axei z, densitatea este de multe ori dată de:
Parametrul complexul de ordine pozițională este definit ca și densitatea medie. De obicei, numai primii doi termeni sunt păstrați și cei de grad mai mare sunt ignorați pentru că cele mai multe faze pot fi descrise în mod adecvat folosind funcții sinusoidale. Pentru un nematic perfect și pentru o fază smectică va lua valori complexe. Natura complexă a acestui parametru permite mai multe paralele între tranzițiile de fază nematice și smectice și de la conductor la supraconductor.[18]
Modelul tijei rigide Onsager[modificare | modificare sursă]
Un model simplu, care prezice tranzițiile de fază liotrope este modelul tijei rigide propus de Lars Onsager. Această teorie consideră volumul exclus din centrul de masă al unui cilindru idealizat în timp ce se apropie de altul. În mod special, dacă cilindrii sunt orientați paralel cu unul de altul, există foarte puțin volum exclus din centrul de masă al cilindrului care se apropie (se poate apropia destul de mult de celălalt cilundru). Dacă, cu toate acestea, cilindrii sunt înclinați unul față de celălalt, atunci există un volum mare din jurul cilindrului în care nu poate pătrunde centrul de masă al celuilalt cilindru (din cauza respingerii între cele două obiecte idealizate). Astfel, acest aranjament unghiular vede o scădere a entropiei poziționale a cilindrului care se apropie (există mai puține stări disponibile pentru acesta).[45][46]
Viziunea fundamentală aici este că, în timp aranjamentele paralele de obiecte anizotrope duc la o scădere a entropiei de orientare, există o creștere a entropiei de poziție. Astfel, în unele cazuri ordonarea pozițională va fi favorabilă din punct de vedere al entropiei. Această teorie prezice astfel că o soluție obiecte în formă de cilindru va trece printr-o tranziție de fază, la o concentrație suficientă, într-o fază nematică. Deși acest model este conceptual util, formularea matematică face mai multe presupuneri care îi limitează aplicabilitatea la sisteme reale.[46]
Teoria câmpului mediu Maier–Saupe[modificare | modificare sursă]
Această teorie statistică, propusă de Alfred Saupe și Wilhelm Maier, include contribuțiile unui potențial intermoleculare de atracție venite de la un moment de dipol indus între moleculele adiacente de cristale lichide. Atracția anizotropă stabilizează alinierea paralelă a moleculelor vecine, și teoria consideră o medie a câmpului mediu de interacțiune. Rezolvată autoconsistent, această teorie prezice tranzițiile de fază nematic termotropic-izotrop, conforme experimentelor.[47][48][49]
Modelul lui McMillan[modificare | modificare sursă]
Modelul lui McMillan, propus de William McMillan,[50] este o extensie a teoriei câmpului mediu Maier–Saupe folosită pentru a descrie tranziția de fază a unui cristal lichid dintr-o fază nematică la una smectică A. Se estimează că tranziția de fază poate fi continuă sau discontinuă, în funcție de intensitatea interacțiunii pe rază scurtă între molecule. Ca urmare, ea permite un punct critic triplu unde se întâlnesc fazele nematică, izotropă și smectică A. Deși prezice existența unui punct critic triplu, ea nu îi și prezice valoarea. Modelul utilizează doi parametri de ordine care descriu ordinea orientațională și pozițională a cristalului lichid. Primul este pur și simplu media celui de-al doilea polinom Legendre și parametrul de ordinul al doilea este dat de:
Valorile zi, θ,mși d sunt poziția moleculei, unghiul dintre axa moleculară și directoare, și spațierea între straturi. Energia potențială postulată a unei molecule este dată de:
Aici, constantă α cuantifică intensitatea interacțiunii între moleculele adiacente. Potențialul este apoi utilizat pentru a obține proprietățile termodinamice ale sistemului, presupunând echilibru termic. El are ca rezultat două ecuații auto-consistente care trebuie să fie rezolvate numeric, soluțiile lor fiind cele trei faze stabile ale cristalului lichid.[20]
Teoria continuumului elastic[modificare | modificare sursă]
În acest formalism, un material cristal lichid este tratat ca un continuum; detaliile moleculare sunt complet ignorate. Mai degrabă, această teorie consideră perturbații de la un eșantion presupus orientat. Distorsiunile cristalului lichid sunt de obicei descrise de densitatea de energie liberă Frank(d). Se pot identifica trei tipuri de distorsiuni care ar putea apărea într-un eșantion orientat: (1) răsuciri ale materialului, în cazul în care moleculele vecine sunt forțate să fie înclinate una față de alta, mai degrabă decât aliniate; (2) evazarea a materialului, în cazul în care îndoirea are loc perpendicular pe directoare; și (3) curbarea materialului, în cazul în care deformarea este paralelă cu directoarea și cu axa moleculară. Toate aceste trei tipuri de distorsiuni atrag o pierdere de energie. Acestea sunt distorsiuni care sunt induse de condițiile la limită la marginile domeniului sau de recipient. Răspunsul materialului poate fi apoi descompus în termeni bazați pe constantele elastice corespunzătoare celor trei tipuri de distorsiuni. Teoria continuumului elastic este un instrument deosebit de puternic pentru modelarea dispozitivelor cu cristale lichide[51] și bistratelor lipidice.[52]
Influențele externe asupra cristalelor lichide[modificare | modificare sursă]
Oamenii de știință și inginerii sunt capabili de a utiliza cristale lichide într-o varietate de aplicații pentru că perturbațiile externe pot provoca schimbări semnificative în proprietățile macroscopice ale sistemelor de cristalel lichide. Câmpuri electrice și magnetice pot fi folosite pentru a induce aceste modificări. Magnitudinea câmpurilor, precum și viteza cu care moleculele se aliniază, sunt caracteristici importante cu care tratează industria. Tratamentele speciale de suprafață pot fi utilizate în dispozitive cu cristale lichide pentru a forța anumite orientări ale directoarei.
Efectul câmpurilor electric și magnetic[modificare | modificare sursă]
Capacitatea directoarei de a se alinia de-a lungul unui câmp extern este cauzată de natura electrică a moleculelor. Dipolii electrici permanenți apar atunci când un capăt al moleculei are o sarcină pozitivă netă în timp ce celălalt capăt are o sarcină negativă netă. Atunci când un câmp electric extern este aplicat pe cristale lichide, moleculele de dipol tind să se orienteze pe direcția câmpului.
Chiar dacă o moleculă nu formează un dipol permanent, acesta poate fi încă influențată de un câmp electric. În unele cazuri, câmpul produce o ușoară rearanjare a electronilor și protonilor în molecule, de așa natură încât rezultă un dipol electric indus. Deși nu este la fel de puternic ca dipoli permanenți, el prezintă totuși orientarea cu câmpul extern. Efectele câmpurilor magnetice asupra moleculelor de cristale lichide sunt analoage celor date de câmpurile electrice. Deoarece câmpurile magnetice sunt generate de sarcini electrice în mișcare, dipolii magnetici permanenți sunt produși de electroni care se deplasează. Atunci când se aplică un câmp magnetic, moleculele vor tinde să se alinieze cu sau împotriva câmpului.
Pregătiri ale suprafețelor[modificare | modificare sursă]
În absența unui câmp exterior, directoarea unui cristal lichid este liberă să se îndrepte în orice direcție. Este posibil, cu toate acestea, să se forțeze o directoare să se îndrepte într-o anumită direcție prin introducerea unui agent extern în sistem. De exemplu, atunci când un strat subțire de polimer (de obicei o poliimidă) este întins pe un substrat de sticlă și frecat într-o singură direcție cu o cârpă, se observă că moleculele de cristale lichide aflate în contact cu suprafața se aliniază cu direcția frecării. Mecanismul actualmente acceptat pentru acest lucru se crede că este o creștere a creșterii epitaxiale a straturilor de cristal lichid pe lanțurile de polimer parțial aliniate în apropiere de straturile superficiale ale poliimidei.
Tranziția Fredericks[modificare | modificare sursă]
Concurența între orientarea produsă de ancorarea la suprafață și de efectele câmpului electric sunt adesea exploatate în dispozitive cu cristale lichide. Dacă se ia în considerare cazul în care molecule de cristale lichide sunt aliniate paralel cu suprafața și se aplică un câmp electric perpendicular pe celulă, atunci în primul rând, pe măsură ce câmpul electric crește în intensitate, nu apare nicio schimbare a alinierii. Cu toate acestea, la o anumită intensitate a câmpului electric, deformarea se produce. Deformarea se produce în cazul în care directoarea își schimbă orientarea de la o moleculă la alta. Apariția unor astfel de schimbări asupra unei stări deformate se numește tranziției Fredericks și poate fi produsă și prin aplicarea unui câmp magnetic suficient de puternic.
Tranziția Fredericks este fundamentală pentru funcționarea multor ecrane cu cristale lichide pentru că orientarea directoarei (și, astfel, proprietățile ei) pot fi controlate cu ușurință prin aplicarea unui câmp.
Efectul chiralității[modificare | modificare sursă]
După cum s-a descris deja, mileculele chirale de cristal lichid dau de obicei naștere la mezofaze chirale. Acest lucru înseamnă că molecula trebuie să posede o formă de asimetrie, de obicei, un centru Stereocentru. O cerință suplimentară este ca sistemul să nu fie racemic: un amestec de molecule cu orientare spre dreapta și spre stânga va anula efectul chiral. Datorită naturii cooperative a ordonării în cristale lichide, un dopaj cu o cantitate mică de chiral într-o mezofază altfel achirală este însă de multe ori suficient să se selecteze o direcționare a domeniului, pentru a face ca sistemul în ansamblu să fie chiral.
Fazele chirale prezintă, de obicei, o răsucire elicoidală a moleculelor. Dacă perioada acestei răsuciri este de ordinul lungimii de undă a luminii vizibile, atunci se pot observa efecte optice interesante de interferență. Răsucirea chirală care aparee în fazele chirale poate face sistemul să răspundă diferit la lumina polarizată circular spre dreapta și spre stânga. Aceste materiale pot fi astfel utilizate ca filtre de polarizare(d).[53]
Este posibil ca molecule chirale să producă mezofaze esențialmente achirale. De exemplu, în anumite intervale de concentrație și de masă moleculară, ADN-ul va forma o fază achirală liniar hexatică. O observație recentă interesantă este formarea mezofazelor chirale din molecule de cristal lichid achirale. În mod special, molecule bent-core (numite uneori cristale lichide-banană) au fost prezentate ca formând cristale lichide cu faze care sunt chirale.[54] În orice eșantion, diverse domenii vor avea orientare opusă, dar în orice domeniu dat, va fi prezentă o ordonare chirală puternică. Mecanismul de acest al acestei chiralități macroscopice nu este încă foarte clar. Se pare că moleculele se stivuiesc în straturi și se orientează în cadrul straturilor într-o manieră înclinată. Aceste faze de cristal lichid faze pot fi feroelectrice(d) sau anti-feroelectrice, ambele fiind de interes pentru aplicații.[55][56]
Chiralitatea poate fi încorporată într-o fază și prin adăugarea unui dopant(d) chiral, care nu poate forma singur cristale lichide. Amestecurile nematice răsucite(d) sau super-răsucite(d) conțin adesea o cantitate mică de astfel de dopanți.
Aplicațiile cristalelor lichide[modificare | modificare sursă]


Cristalele lichide și-au găsit o largă utilizare în afișajele cu cristale lichide, care se bazează pe proprietățile optice ale unor substanțe lichid-cristaline în prezența sau în absența unui câmp electric. Într-un dispozitiv tipic, un strat de cristale lichide (de grosime de obicei de circa 4 µm) se află între două filtre de polarizare care sunt traversate (orientate la 90° una față de alta). Aliniera cristalelor lichide este aleasă astfel încât faza sa relaxată să fie una răsucită.[8] Această fază răsucită reorientează lumina care a trecut prin primul polarizor, permițând transmiterea acesteia prin cel de-al doilea polarizor (și reflectată înapoi la observator, dacă există și un reflector). Dispozitivul apare astfel transparent. Atunci când un câmp electric este aplicat stratului de cristal lichid, axa moleculară lungă tinde să se alinieze paralel cu câmpul electric, astfel, detorsionându-se treptat în centrul stratul de cristal lichid. În această stare, moleculele de cristal lichid nu reorientează lumina, astfel încât lumina polarizată de primul polarizor este absorbită de cel de-al doilea polarizor, iar aparatul își pierde transparența cu creșterea tensiunii. În acest fel, câmpul electric poate fi folosit pentru a face un pixel să comute între transparent și opac la comandă. Sistemele LCD color folosesc aceeași tehnică, cu filtre de culoare folosite pentru a genera pixeli roșii, verzi și albaștri.[8] Cristalele lichide chirale smectice sunt folosite în LCD-uri feroelectrice care sunt modulatoare binare de lumină cu comutare rapidă. Principii similare pot fi folosite pentru a face alte dispozitive optice pe bază de cristale lichide.[57]
Filtrele acordabile cu cristale lichide(d) sunt folosite ca dispozitive electrooptice(d), de exemplu, în imagistica hiperspectrală(d).
Cristalele lichide termotrope(d) chirale a căror perioadă variază puternic cu temperatura pot fi folosite drept termometre rudimentare cu cristale lichide(d), deoarece culoarea materialului se va schimba pe măsură ce variază perioada. Tranzițiile de culoare ale cristalelor lichide sunt folosite în multe termometre de acvariu și de piscină, precum și la termometrele pentru sugari sau de baie.[58] Alte materiale în stare de cristal lichid își schimbă culoarea atunci când sunt întinse sau presate. Astfel, foile de cristale lichide sunt adesea folosite în industrie pentru a căuta puncte fierbinți, a mapa fluxul de căldură, a măsura modelele de distribuție a tensiunii, și așa mai departe. Cristalele lichide în formă lichidă sunt utilizate pentru a detecta puncte fierbinți generate electric în analiza eșecurilor(d) în industria semiconductorilor.[59]
Laserele cu cristale lichide(d) pot folosi un cristal lichid ca mediu de amplificare ca mecanism de reacție distribuită în loc de oglinzi exterioare. Emisiile într-o bandă fotonică creată de structura dielectrică periodică a cristalului lichid oferă un dispozitiv cu prag redus și amplificare mare cu emisie monocromatică stabilă.[60][61]
Foile și rolele de cristale lichide cu polimeri dispersați (PDLC)(d) sunt disponibile ca peliculă inteligentă(d) susținută cu adeziv, care pot fi aplicată pe ferestre și comutată electric între transparență și opacitate.
Multe lichide obișnuite, cum ar fi apa cu săpun, sunt de fapt cristale lichide. Săpunul formează o varietate de faze de cristal lichid, în funcție de concentrația în apă.[62]
Coloanele de cristale lichide cu molecule în formă de castron pot fi utilizate drept comutatoare rapide.[63]
Referințe[modificare | modificare sursă]
- ^ a b c d e Chandrasekhar, S.(d) (). Liquid Crystals (ed. 2nd). Cambridge: Cambridge University Press. ISBN 0-521-41747-3.
- ^ Reinitzer, Friedrich (). „Beiträge zur Kenntniss des Cholesterins”. Monatshefte für Chemie (Wien). 9 (1): 421–441. doi:10.1007/BF01516710.
- ^ Lehmann, O. (). „Über fliessende Krystalle”. Zeitschrift für Physikalische Chemie. 4: 462–72.
- ^ a b Sluckin, T. J.; Dunmur, D. A. & Stegemeyer, H. (). Crystals That Flow – classic papers from the history of liquid crystals. London: Taylor & Francis. ISBN 0-415-25789-1.
- ^ Gray, G. W. (1962) Molecular Structure and the Properties of Liquid Crystals, Academic Press
- ^ Stegemeyer, H (). „Professor Horst Sackmann, 1921 – 1993”. Liquid Crystals Today. 4: 1. doi:10.1080/13583149408628630.
- ^ Liquid Crystals Arhivat în , la Archive.is. kfupm.edu.sa
- ^ a b c d Castellano, Joseph A. (). Liquid Gold: The Story of Liquid Crystal Displays and the Creation of an Industry. World Scientific Publishing. ISBN 978-981-238-956-5.
- ^ Goldmacher, Joel E. and Castellano, Joseph A. “Electro-optical Compositions and Devices,” U.S. Patent 3.540.796, emis la data de 17 noiembrie 1970.
- ^ Heilmeier, G. H.; Zanoni, L. A.; Barton, L. A. (). „Dynamic Scattering in Nematic Liquid Crystals”. Applied Physics Letters. 13: 46. Bibcode:1968ApPhL..13...46H. doi:10.1063/1.1652453.
- ^ Kelker, H.; Scheurle, B. (). „A Liquid-crystalline (Nematic) Phase with a Particularly Low Solidification Point”. Angew. Chem. Int. Ed. 8 (11): 884. doi:10.1002/anie.196908841.
- ^ Gray, G.W.; Harrison, K.J.; Nash, J.A. (). „New family of nematic liquid crystals for displays”. Electronics Lett. 9 (6): 130. doi:10.1049/el:19730096.
- ^ Lin, Lei (Lam, Lui) (1982). "Liquid crystal phases and the 'dimensionality' of molecules". Wuli (Physics) 11, 171-178.
- ^ „History and Properties of Liquid Crystals”. Nobelprize.org. Accesat în .
- ^ Lam, Lui (1994). "Bowlics". Liquid Crystalline and Mesomorphic Polymers, eds. Valery P. Shibaev and Lui Lam. New York: Springer.
- ^ Lin, Lei (Lam, Lui) (1987). "Bowlic liquid crytals". Mol. Cryst. Liq. Cryst 146: 41-54.
- ^ „copie arhivă”. Arhivat din original la . Accesat în .
- ^ a b c d e f
de Gennes, P.G.; Prost (). The Physics of Liquid Crystals [Fizica cristalelor lichide]. Oxford: Clarendon Press. ISBN 0-19-852024-7. Mai multe valori specificate pentru
|first1=și|first=(ajutor) - ^ a b c Dierking, I. (). Textures of Liquid Crystals. Weinheim: Wiley-VCH. ISBN 3-527-30725-7.
- ^ a b c d Collings, P.J. & Hird, M (). Introduction to Liquid Crystals. Bristol, PA: Taylor & Francis. ISBN 0-7484-0643-3.
- ^ Shao, Y.; Zerda, T. W. (). „Phase Transitions of Liquid Crystal PAA in Confined Geometries”. Journal of Physical Chemistry B. 102 (18): 3387–3394. doi:10.1021/jp9734437.
- ^ Rego, J.A.; Harvey, Jamie A.A.; MacKinnon, Andrew L.; Gatdula, Elysse (ianuarie 2010). „Asymmetric synthesis of a highly soluble 'trimeric' analogue of the chiral nematic liquid crystal twist agent Merck S1011” (PDF). Liquid Crystals. 37 (1): 37–43. doi:10.1080/02678290903359291. Arhivat din original (PDF) la . Accesat în .
- ^ Madsen, L. A.; Dingemans, T. J.; Nakata, M.; Samulski, E. T. (). „Thermotropic Biaxial Nematic Liquid Crystals”. Phys. Rev. Lett. 92 (14): 145505. Bibcode:2004PhRvL..92n5505M. doi:10.1103/PhysRevLett.92.145505. PMID 15089552.
- ^ „smectic”. Merriam-Webster Dictionary.
- ^ Kopp, V. I.; Fan, B.; Vithana, H. K. M.; Genack, A. Z.; Fan; Vithana; Genack (). „Low threshold lasing at the edge of a photonic stop band in cholesteric liquid crystals”. Opt. Lett. 23 (21): 1707–1709. Bibcode:1998OptL...23.1707K. doi:10.1364/OL.23.001707. PMID 18091891.
- ^ Priestley, E. B.; Wojtowicz, P. J. & Sheng, P. (). Introduction to Liquid Crystals. Plenum Press. ISBN 0-306-30858-4.
- ^ Kleinert H. and Maki K. (). „Lattice Textures in Cholesteric Liquid Crystals” (PDF). Fortschritte der Physik. 29 (5): 219–259. Bibcode:1981ForPh..29..219K. doi:10.1002/prop.19810290503.
- ^ Seideman, T (). „The liquid-crystalline blue phases” (PDF). Rep. Prog. Phys. 53 (6): 659–705. Bibcode:1990RPPh...53..659S. doi:10.1088/0034-4885/53/6/001.
- ^ Coles, Harry J.; Pivnenko, Mikhail N. (). „Liquid crystal 'blue phases' with a wide temperature range”. Nature. 436 (7053): 997–1000. Bibcode:2005Natur.436..997C. doi:10.1038/nature03932. PMID 16107843.
- ^ Yamamoto, Jun; Nishiyama, Isa; Inoue, Miyoshi; Yokoyama, Hiroshi (). „Optical isotropy and iridescence in a smectic blue phase”. Nature. 437 (7058): 525. Bibcode:2005Natur.437..525Y. doi:10.1038/nature04034.
- ^ Kikuchi H, Yokota M, Hisakado Y, Yang H, Kajiyama T.; Yokota; Hisakado; Yang; Kajiyama (). „Polymer-stabilized liquid crystal blue phases”. Nature Materials. 1 (1): 64–8. Bibcode:2002NatMa...1...64K. doi:10.1038/nmat712. PMID 12618852.
- ^ „Samsung Develops World's First 'Blue Phase' Technology to Achieve 240 Hz Driving Speed for High-Speed Video”. Accesat în .
- ^ Qizhen Liang; Pengtao Liu; Cheng Liu; Xigao Jian; Dingyi Hong; Yang Li. (). „Synthesis and Properties of Lyotropic Liquid Crystalline Copolyamides Containing Phthalazinone Moieties and Ether Linkages”. Polymer. 46 (16): 6258–6265. doi:10.1016/j.polymer.2005.05.059.
- ^ Martin, James D.; Keary, Cristin L.; Thornton, Todd A.; Novotnak, Mark P.; Knutson, Jeremey W.; Folmer, Jacob C. W. (). „Metallotropic liquid crystals formed by surfactant templating of molten metal halides”. Nature Materials. 5 (4): 271–5. Bibcode:2006NatMa...5..271M. doi:10.1038/nmat1610. PMID 16547520.
- ^ Zocher, H (). „Uber freiwillige Strukturbildung in Solen. (Eine neue Art anisotrop flqssiger Medien)”. Z Anorg Allg Chem. 147: 91. doi:10.1002/zaac.19251470111.
- ^ Davidson, Patrick; Gabriel, Jean-Christophe P. (). „Mineral Liquid Crystals from Self-Assembly of Anisotropic Nanosystems”. Top Curr Chem. 226: 119. doi:10.1007/b10827.
- ^ Langmuir, I (). „The role of attractive and repulsive forces in the formation of tactoids, thixotropic gels, protein crystals and coacervates”. J Chem Phys. 6: 873. Bibcode:1938JChPh...6..873L. doi:10.1063/1.1750183.
- ^ Gabriel, jean-Christophe P.; Sanchez, Clément; Davidson, Patrick (). „Observation of Nematic Liquid-Crystal Textures in Aqueous Gels of Smectite Clays”. J. Phys. Chem. 100: 11139. doi:10.1021/jp961088z.
- ^ Paineau, E; Philippe, A. M.; Antonova, K.; Bihannic, I.; Davidson, P.; Dozov, I; Gabriel, J.C. P.; Impéror-Clerc, M.; Levitz, P.; Meneau, F.; Michot, L. (). „Liquid–crystalline properties of aqueous suspensions of natural clay nanosheets”. Liquid Crystals Reviews. 1: 110. doi:10.1080/21680396.2013.842130.
- ^ Gabriel, Jean-Christophe P.; Camerel, Franck; Lemaire, Bruno J.; Desvaux, Hervé; Davidson, Patrick; Batail, Patrick (). „Swollen liquid-crystalline lamellar phase based on extended solid-like sheets”. Nature. 413: 504. Bibcode:2001Natur.413..504G. doi:10.1038/35097046.
- ^ Buka, A.; Palffy-Muhoray, P.; Rácz, Z. (). „Viscous fingering in liquid crystals”. Phys. Rev. A. 36 (8): 3984. Bibcode:1987PhRvA..36.3984B. doi:10.1103/PhysRevA.36.3984.
- ^ González-Cinca, R.; Ramírez-Piscina, L.; Casademunt, J.; Hernández-Machado, A.; Kramer, L.; Tóth Katona, T.; Börzsönyi, T.; Buka, Á. (). „Phase-field simulations and experiments of faceted growth in liquid crystal”. Physica D. 99 (2–3): 359. Bibcode:1996PhyD...99..359G. doi:10.1016/S0167-2789(96)00162-5.
- ^ González-Cinca, R; Ramı́Rez-Piscina, L; Casademunt, J; Hernández-Machado, A; Tóth-Katona, T; Börzsönyi, T; Buka, Á (). „Heat diffusion anisotropy in dendritic growth: phase field simulations and experiments in liquid crystals”. Journal of Crystal Growth. 193 (4): 712. Bibcode:1998JCrGr.193..712G. doi:10.1016/S0022-0248(98)00505-3.
- ^ Ghosh, S. K. (). „A model for the orientational order in liquid crystals”. Il Nuovo Cimento D. 4 (3): 229. Bibcode:1984NCimD...4..229G. doi:10.1007/BF02453342.
- ^ Onsager, Lars (). „The effects of shape on the interaction of colloidal particles”. Annals of the New York Academy of Sciences. 51 (4): 627. Bibcode:1949NYASA..51..627O. doi:10.1111/j.1749-6632.1949.tb27296.x.
- ^ a b Vroege, G J; Lekkerkerker, H N W (). „Phase transitions in lyotropic colloidal and polymer liquid crystals”. Rep. Progr. Phys. 55 (8): 1241. Bibcode:1992RPPh...55.1241V. doi:10.1088/0034-4885/55/8/003.
- ^ Maier W. and Saupe A.; Saupe (). „Eine einfache molekulare theorie des nematischen kristallinflussigen zustandes”. Z. Naturforsch. A (în German). 13: 564. Bibcode:1958ZNatA..13..564M. doi:10.1515/zna-1958-0716.
- ^ Maier W. and Saupe A.; Saupe (). „Eine einfache molekular-statistische theorie der nematischen kristallinflussigen phase .1”. Z. Naturforsch. A (în German). 14: 882. Bibcode:1959ZNatA..14..882M. doi:10.1515/zna-1959-1005.
- ^ Maier W. and Saupe A.; Saupe (). „Eine einfache molekular-statistische theorie der nematischen kristallinflussigen phase .2”. Z. Naturforsch. A (în German). 15: 287. Bibcode:1960ZNatA..15..287M. doi:10.1515/zna-1960-0401.
- ^ McMillan, W. (). „Simple Molecular Model for the Smectic A Phase of Liquid Crystals”. Phys. Rev. A. 4 (3): 1238. Bibcode:1971PhRvA...4.1238M. doi:10.1103/PhysRevA.4.1238.
- ^ Leslie, F. M. (). „Continuum theory for nematic liquid crystals”. Continuum Mechanics and Thermodynamics. 4 (3): 167. Bibcode:1992CMT.....4..167L. doi:10.1007/BF01130288.
- ^ Watson, M. C.; Brandt, E. G.; Welch, P. M.; Brown, F. L. H. (). „Determining Biomembrane Bending Rigidities from Simulations of Modest Size”. Physical Review Letters. 109 (2): 028102. Bibcode:2012PhRvL.109b8102W. doi:10.1103/PhysRevLett.109.028102.
- ^ Fujikake, H.; Takizawa, K.; Aida, T.; Negishi, T.; Kobayashi, M. (). „Video camera system using liquid-crystal polarizing filter toreduce reflected light”. IEEE Transactions on Broadcasting. 44 (4): 419. doi:10.1109/11.735903.
- ^ Achard, M.F.; Bedel, J.Ph.; Marcerou, J.P.; Nguyen, H.T.; Rouillon, J.C. (). „Switching of banana liquid crystal mesophases under field”. European Physical Journal E. 10 (2): 129–34. Bibcode:2003EPJE...10..129A. doi:10.1140/epje/e2003-00016-y. PMID 15011066.
- ^ Baus, Marc; Colot, Jean-Louis (). „Ferroelectric nematic liquid-crystal phases of dipolar hard ellipsoids”. Phys. Rev. A. 40 (9): 5444. Bibcode:1989PhRvA..40.5444B. doi:10.1103/PhysRevA.40.5444.
- ^ Uehara, Hiroyuki; Hatano, Jun (). „Pressure-Temperature Phase Diagrams of Ferroelectric Liquid Crystals”. J. Phys. Soc. Jpn. 71 (2): 509. Bibcode:2002JPSJ...71..509U. doi:10.1143/JPSJ.71.509.
- ^ Alkeskjold, Thomas Tanggaard; Scolari, Lara; Noordegraaf, Danny; Lægsgaard, Jesper; Weirich, Johannes; Wei, Lei; Tartarini, Giovanni; Bassi, Paolo; Gauza, Sebastian; Wu, Shin-Tson; Bjarklev, Anders (). „Integrating liquid crystal based optical devices in photonic crystal”. Optical and Quantum Electronics. 39 (12–13): 1009. doi:10.1007/s11082-007-9139-8.
- ^ Plimpton, R. Gregory "Pool thermometer" U.S. Patent 4,738,549 emis la 19 aprilie 1988
- ^ „Hot-spot detection techniques for ICs”. acceleratedanalysis.com. Arhivat din original la . Accesat în .
- ^ Kopp, V. I.; Fan, B.; Vithana, H. K. M.; Genack, A. Z. (). „Low-threshold lasing at the edge of a photonic stop band in cholesteric liquid crystals”. Optics Express. 23 (21): 1707–1709. Bibcode:1998OptL...23.1707K. doi:10.1364/OL.23.001707. PMID 18091891.
- ^ Dolgaleva, Ksenia; Simon K.H. Wei; Svetlana G. Lukishova; Shaw H. Chen; Katie Schwertz; Robert W. Boyd (). „Enhanced laser performance of cholesteric liquid crystals doped with oligofluorene dye”. Journal of the Optical Society of America. 25 (9): 1496–1504. Bibcode:2008JOSAB..25.1496D. doi:10.1364/JOSAB.25.001496.
- ^ Luzzati, V.; Mustacchi, H.; Skoulios, A. (). „Structure of the Liquid-Crystal Phases of the Soap–water System: Middle Soap and Neat Soap”. Nature. 180 (4586): 600. Bibcode:1957Natur.180..600L. doi:10.1038/180600a0.
- ^ Bock, H.; Helfrich, W.; Heppke, G. (1992). "Switchable columnar liquid crystalline systems". European Patent EP0529439B1 (filing date: 08/14/1992; publication date: 02/14/1996).
Legături externe[modificare | modificare sursă]
- „History and Properties of Liquid Crystals”. Nobelprize.org. Accesat în .










