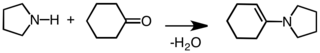Pirolidină
| Pirolidină | |
 | |
 | |
| Identificare | |
|---|---|
| Număr CAS | 123-75-1 |
| ChEMBL | CHEMBL22830 |
| PubChem CID | 31268 |
| Formulă chimică | C₄H₉N[1] |
| Masă molară | 71 u.a.m.[1] |
| Proprietăți | |
| Densitate | 1 g/cm³ |
| Punct de topire | −63 °C[2] |
| Punct de fierbere | 87 °C |
| Sunt folosite unitățile SI și condițiile de temperatură și presiune normale dacă nu s-a specificat altfel. | |
| Modifică date / text | |
Pirolidina (denumită și tetrahidropirol sau azolidină) este un compus organic heterociclic, care prezintă formula moleculară (CH2)4NH. Din punct de vedere structural, este o amină secundară ciclică, cu heterociclu saturat. Este un lichid incolor, miscibil cu apa și cu majoritatea solvenților organici. Prezintă un miros caracteristic, amoniacal.
Pirolidinele sunt derivații pirolidinei, un exemplu fiind aminoacidul prolină. Multe medicamente sunt derivați de pirolidină, un exemplu fiind lincosamidele.[3]
Obținere
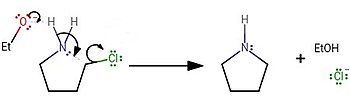
[modificare | modificare sursă]Pirolidina se obține în urma reacției dintre 1,4-butandiol și amoniac, în prezența unui catalizator de tip oxid.[4] În laborator, se poate obține în urma reacției dintre 4-clorobuta-1-amina și o bază tare:
Proprietăți
[modificare | modificare sursă]Pirolidina prezintă caracter bazic, comparabil cu al altor dialchil-amine.[5] Spre deosebire de restul aminelor secundare, pirolidina prezintă o structură ciclică.
Pirolidina este utilizată ca precursor în sinteza unor compuși organici mai complecși. Un exemplu este utilizarea sa pentru activarea cetonelor și aldehidelor în reacția de adiție nucleofilă, prin formare de enamine:[6]
Note
[modificare | modificare sursă]- ^ a b c „Pirolidină”, PYRROLIDINE (în engleză), PubChem, accesat în
- ^ Jean-Claude Bradley Open Melting Point Dataset
- ^ Pubchem. „Lincosamides”. pubchem.ncbi.nlm.nih.gov (în engleză). Accesat în .
- ^ Karsten Eller, Erhard Henkes, Roland Rossbacher, Hartmut Höke "Amines, Aliphatic" din Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, 2005. doi:10.1002/14356007.a02_001
- ^ H. K. Hall, Jr. (). „Correlation of the Base Strengths of Amines”. J. Am. Chem. Soc. 79 (20): 5441. doi:10.1021/ja01577a030.
- ^ R. B. Woodward, I. J. Pachter, and M. L. Scheinbaum (), „2,2-(Trimethylenedithio)cyclohexanone”, Org. Synth., 54: 39; Collective Volume, 6, p. 1014