2,4-Dinitrofenilhidrazină
| 2,4-Dinitrofenilhidrazină | |
 | |
 | |
 | |
| Nume IUPAC | (2,4-Dinitrofenil)hidrazină |
|---|---|
| Alte denumiri | 2,4-DNPH 2,4-DNP Reactivul Brady Reactivul Borche |
| Identificare | |
| Număr CAS | 119-26-6 |
| ChEMBL | 352799 |
| PubChem CID | 3772977 |
| Informații generale | |
| Formulă chimică | C6H6N4O4 |
| Aspect | Pudră roșie sau oranj |
| Masă molară | 198.14 Da |
| Proprietăți | |
| Punct de topire | 198 – 202 °C |
| Solubilitate | Redusă |
Inflamabil, posibil carcinogen | |
| Sunt folosite unitățile SI și condițiile de temperatură și presiune normale dacă nu s-a specificat altfel. | |
| Modifică date / text | |
2,4-dinitrofenilhidrazina (DNPH) este un compus organic cu formula chimică C6H3(NO2)2NHNH2. Dinitrofenilhidrazina este o substanță solidă, cu o culoare roșie-oranj. Este o hidrazină substituită. Sub formă solidă, este relativ sensibilă la șoc și frecare. Din acest motiv, dinitrofenilhidrazina este de obicei utilizată sub formă de pulbere umedă. DNPH este un precursor al medicamentului Sivifen.
Sinteză[modificare | modificare sursă]
Poate fi preparată prin reacția sulfatului de hidrazină cu 2,4-dinitroclorobenzen:
Testul DNP[modificare | modificare sursă]
DNPH este un reactiv folosit în analiza organică calitativă. Atunci când DNPH este folosit astfel, poartă denumirea de reactivul Brady (denumit după chimistul american Saint Elmo Brady) sau reactivul Borsche (denumit după chimistul german Walther Borsche). Acesta este preparat prin dizolvarea 2,4-dinitrofenilhidrazinei într-o soluție care conține metanol și o cantitate de acid sulfuric concentrat. Reactivul Borsche este utilizat pentru detectarea cetonelor și aldehidelor. Un rezultat pozitiv este semnalat prin depunerea unui precipitat galben, oranj sau roșu de dinitrofenilhidrazonă. Carbonilii aromatici formează precipitate roșii, în timp ce carbonilii alifatici formează precipitate cu o culoare mai galbenă.[1] Reacția dintre 2,4-dinitrofenilhidrazină și o cetonă generică pentru a forma o hidrazonă este prezentată mai jos:
- RR'C=O + C6H3(NO2)2NHNH2 → C6H3(NO2)2NHN=CRR' + H2O
Această reacție este o reacție de condensare, deoarece două molecule se unesc, rezultând în eliminare de apă. Mecanistic, este un exemplu de reacție de adiție-eliminare: adiție nucleofilă a grupării -NH2 la gruparea carbonil C=O, urmată de eliminarea unei molecule de H2O:[2]
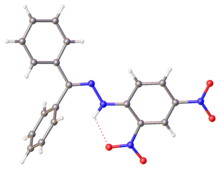
Structura cu raze X a hidrazonei benzofenonei derivate din DNP. Parametrii: C=N, 128 pm; N–N, 1.38 pm, N–N–C(Ar), 119[3]

Hidrazonele derivate din DNP au puncte de topire caracteristice, facilitând identificarea carbonilului. În special, această utilizare a 2,4-dinitrofenilhidrazinei a fost dezvoltată de Brady și Elsmie.[4] Tehnicile spectroscopice și spectrometrice moderne au înlocuit aceste tehnici.
Dinitrofenilhidrazina nu reacționează cu alte grupe funcționale care conțin carbonil, cum ar fi acizii carboxilici, amidele și esterii, pentru care există stabilitate asociată rezonanței, deoarece o pereche de electroni interacționează cu orbitalul p al carbonului care are gruparea carbonil, rezultând într-o delocalizare crescută în moleculă. Această stabilitate s-ar pierde prin adăugarea unui reactiv la gruparea carbonil. Prin urmare, acești compuși sunt mai rezistenți la reacțiile de adăugare. De asemenea, cu acizii carboxilici există efectul compusului care acționează ca bază, lăsând carboxilatul rezultat încărcat negativ și, prin urmare, invulnerabil la atacul nucleofil.
Siguranță[modificare | modificare sursă]
Pot rezulta explozii din utilizarea DNPH.[5]
Vezi și[modificare | modificare sursă]
Referințe[modificare | modificare sursă]
- ^ „copie arhivă” (PDF). Arhivat din original (PDF) la . Accesat în .
- ^ Adapted from Chemistry in Context, 4th Edition, 2000, Graham Hill and John Holman
- ^ Tameem, Abdassalam Abdelhafiz; Salhin, Abdussalam; Saad, Bahruddin; Rahman, Ismail Ab.; Saleh, Muhammad Idiris; Ng, Shea-Lin; Fun, Hoong-Kun (). „Benzophenone 2,4-dinitrophenylhydrazone”. Acta Crystallographica Section E. 62 (12): o5686–o5688. doi:10.1107/S1600536806048112.
- ^ Brady, Oscar L.; Elsmie, Gladys V. (). „The use of 2:4-dinitrophenylhydrazine as a reagent for aldehydes and ketones”. Analyst(d). 51 (599): 77–78. Bibcode:1926Ana....51...77B. doi:10.1039/AN9265100077.
- ^ „Bomb disposal squads detonate chemical stocks in British schools”. The Guardian. . Accesat în .


