Hidrazonă

Hidrazonele reprezintă o clasă de compuși organici cu structura generală R
1R
2C=NNH
2.[1] Sunt asemănătoare cu cetonele și aldehidele, în structura cărora se înlocuiește atomul de oxigen cu o grupă funcțională NNH
2.
Obținere[modificare | modificare sursă]
Hidrazonele se pot obține prin reacția dintre hidrazină și o cetonă sau o aldehidă:[2][3]
Fenilhidrazina reacționează cu zaharurile reducătoare pentru a forma hidrazone, cunoscute sub numele specific de osazone; formarea lor a fost dezvoltată de către chimistul german Emil Fischer, ca test pentru a diferenția monozaharidele.[4][5]
Proprietăți[modificare | modificare sursă]
Hidrazonele sunt sensibile la reacții de hidroliză:
- R2C=N−NR'2 + H2O → R2C=O + H2N−NR'2
Alchilhidrazonele sunt de 102 până la 103 ori mai sensibile la hidroliză decât oximele analoge.[6]
Hidrazonele acționează ca intermediari în reacțiile de reducere Wolff-Kishner, care este un proces de reducere a compușilor carbonilici la alcani:[7]

Gallery[modificare | modificare sursă]
- Exemple de hidrazone
-
Hidrazona benzofenonei[8]
-
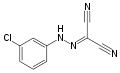
Hidrazona m-clorofenil carbonil cianurii
-
Giromitrină, o toxină
-
Dihidralazină, un medicament antihipertensiv
-
Furazolidonă, un medicament antiinfecțios
Vezi și[modificare | modificare sursă]
Referințe[modificare | modificare sursă]
- ^ March, Jerry (1985), Advanced Organic Chemistry: Reactions, Mechanisms, and Structure (3rd ed.), New York: Wiley, ISBN 0-471-85472-7
- ^ Stork, G.; Benaim, J. (), „Monoalkylation of α,β-Unsaturated Ketones via Metalloenamines: 1-butyl-10-methyl-Δ1(9)-2-octalone”, Org. Synth., 57: 69; Collective Volume, 6, p. 242
- ^ Day, A. C.; Whiting, M. C. (), „Acetone hydrazone”, Org. Synth., 50: 3; Collective Volume, 6, p. 10
- ^ Fischer, Emil (). „Schmelzpunkt des Phenylhydrazins und einiger Osazone”. Berichte der Deutschen Chemischen Gesellschaft. 41: 73–77. doi:10.1002/cber.19080410120.
- ^ Fischer, Emil (). „Ueber einige Osazone und Hydrazone der Zuckergruppe”. Berichte der Deutschen Chemischen Gesellschaft. 27 (2): 2486–2492. doi:10.1002/cber.189402702249.
- ^ Kalia, J.; Raines, R. T. (). „Hydrolytic stability of hydrazones and oximes”. Angew. Chem. Int. Ed. 47 (39): 7523–6. doi:10.1002/anie.200802651. PMC 2743602
 . PMID 18712739.
. PMID 18712739.
- ^ Carey, Francis A.; Sundberg, Richard J. (). Advanced Organic Chemistry: Part B: Reactions and Synthesis (ed. 5th). New York: Springer. p. 453. ISBN 978-0387683546.
- ^ Tameem, Abdassalam Abdelhafiz; Salhin, Abdussalam; Saad, Bahruddin; Rahman, Ismail Ab.; Saleh, Muhammad Idiris; Ng, Shea-Lin; Fun, Hoong-Kun (). „Benzophenone 2,4-dinitrophenylhydrazone”. Acta Crystallographica Section E. 62 (12): o5686–o5688. doi:10.1107/S1600536806048112.


![Hidrazona benzofenonei[8]](http://upload.wikimedia.org/wikipedia/commons/thumb/7/75/Benzophenone_hydrazone-structure.png/120px-Benzophenone_hydrazone-structure.png)