Aminoacid
| Acest articol are nevoie de atenția unui expert în medicină. Recrutați unul sau, dacă sunteți în măsură, ajutați chiar dumneavoastră la îmbunătățirea articolului! |
| Acest articol sau această secțiune are bibliografia incompletă sau inexistentă. Puteți contribui prin adăugarea de referințe în vederea susținerii bibliografice a afirmațiilor pe care le conține. |
Aminoacizii sunt compuși cu funcțiune mixtă (compuși care au grupe funcționale diferite în molecula lor) care conțin în molecula lor grupările -NH2 și -COOH.

Formula generală a aminoacizilor este:
Nomenclatură[modificare | modificare sursă]
Aminoacizii se denumesc folosind cuvântul „acid“, urmat de „amino“ și numele acidului corespunzător. Prin prefixele „di“, „tri“ etc., se arată numărul de grupe amino și carboxil, iar poziția relativă a două grupe funcționale se precizează cu literele grecești „α“, „β“, „γ“, „δ“, „ε“, în care acidul este α dacă grupările amino și carboxil se leagă de un același carbon, β dacă grupările amino și carboxil se leagă la atomi de carbon alăturați, iar, pe măsură ce crește distanța, se vor numi γ, δ, ε. În cazul compușilor aromatici, se folosesc prefixele „orto“, „meta“, „para“.
, acid α amino-propanoic
, acid β amino-propanoic
Tipuri de aminoacizi naturali[modificare | modificare sursă]
Un aminoacid este natural dacă este alifatic și α. Există 20 de aminoacizi ce intră în componența proteinelor. Aceștia sunt: alanină, valină, leucină, izoleucină, prolină, triptofan, fenilalanină, metionină, glicocol, serină, treonină, tirozină, asparagină, glutamină, cisteină, acid aspartic, acid glutamic, arginină, lizină, histidină (acesta din urmă constituie un aminoacid esențial pentru copiii cu vârsta sub 1 an). Dintre aceștia, 8 sunt esențiali, adică nu pot fi produși de organismul uman și trebuie aduși din exterior, prin alimentație (valina, leucina, izoleucina, triptofanul, fenilalanina, metionina, lizina și treonina).
După numărul grupelor carboxil și amino[modificare | modificare sursă]
Aminoacizi monoaminici și monocarboxilici[modificare | modificare sursă]
, acid amino-acetic (glicina, glicocol) 
, acid α-amino-propanoic (α-alanină) 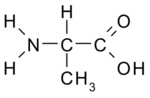
, acid α-amino-izovalerianic (valină) 
Aminoacizi monoaminici și dicarboxilici[modificare | modificare sursă]
, acid aminosuccinic (acid asparagic)
, acid α aminoglutaric (acid glutamic)
Aminoacizi diaminici și monocarboxilici[modificare | modificare sursă]
, acid α, ε diamino-capronic (lisină) 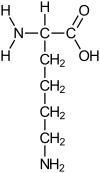
După alte grupări incluse[modificare | modificare sursă]
Aminoacizi hidroxilați[modificare | modificare sursă]
, acid α amino β hidroxi propanoic (serină) 
Aminoacizi tiolici[modificare | modificare sursă]
, acid α amino β tio propanoic (cisteină) 
Proprietăți fizice[modificare | modificare sursă]
Aminoacizii sunt substanțe solide, cristalizate. Au puncte de topire foarte ridicate (P.t.>250 °C datorită legăturilor de H ce se stabilesc între grupările -COOH la moleculele vecine) și sunt solubili în H2O dar insolubili în compuși organici. Aminoacizii inferiori au gust dulce iar cei superiori au gust amar. Sunt incolori la temperatura camerei.
Proprietăți chimice[modificare | modificare sursă]
Caracter de amfion[modificare | modificare sursă]
Amfionii sunt structuri chimice care, în cadrul aceleeași molecule, conțin ambele tipuri de sarcini.
, în prezența H2O
Caracter de amfion/Caracter amfoter[modificare | modificare sursă]
, cation al aminoacidului
, anion al aminoacidului
Soluții[modificare | modificare sursă]
Aminoacizii se folosesc la prepararea soluțiilor tampon. Acestea sunt soluțiile în care, dacă se adaugă o cantitate limitată (mică) de acid sau de bază, aceasta este neutralizată și pH-ul soluției nu se schimbă.
Reacții caracteristice acizilor organici[modificare | modificare sursă]
Deoarece conțin gruparea carboxil, care este specifică acizilor carboxilici, aminoacizii reacționează la această grupare în același fel.
Reacții caracteristice aminelor[modificare | modificare sursă]
Datorită grupării amino, care este specifică aminelor, conținută în moleculă, aminoacizii reacționează la această grupare în mod similar.
Reacția de condensare[modificare | modificare sursă]
În timpul acestei reacții se formează legături noi între atomi ce aparțin la molecule distincte, numite legături peptidice. Rezultatul reacției sunt peptidele.
| |||||||||||||||||||||||||||||||














