Cloropren
| Cloropren | |
 | |
 | |
| Nume IUPAC | 2-cloro-1,3-butadienă |
|---|---|
| Alte denumiri | Cloropren |
| Identificare | |
| Număr CAS | 126-99-8 |
| ChEMBL | CHEMBL555660 |
| PubChem CID | 31369 |
| Informații generale | |
| Formulă chimică | C4H5Cl |
| Aspect | lichid incolor |
| Masă molară | 88,5365 g/mol |
| Proprietăți | |
| Densitate | 0,9598 g/cm3 |
| Starea de agregare | lichidă |
| Punct de topire | −130 °C |
| Punct de fierbere | 59,4 °C |
| Solubilitate | apă: 0,026 g/100 mL |
| Presiune de vapori | 188 de millimetre of mercuryi[1] |
| Indice de refracție(nD) | 1,4583 |
| Pericol | |
| Fraze R | R11, R45, R20/22, R36/37/38, R48/20 |
| Fraze S | S45, S53 |
| NFPA 704 | |
| Sunt folosite unitățile SI și condițiile de temperatură și presiune normale dacă nu s-a specificat altfel. | |
| Modifică date / text | |
Cloroprenul este denumirea comună pentru compusul organic 2-cloro-1,3-butadienă, care are formula chimică CH2=CCl-CH=CH2. Este un lichid incolor, fiind un monomer important folosit pentru producerea polimerului numit policloropren, un tip de cauciuc sintetic. Policloroprenul este cunoscut mai pe larg sub denumirea de neopren, [2] care este numele comercială dată de firma DuPont.
Obținere[modificare | modificare sursă]
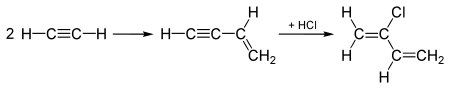
Din 1960, cloroprenul se produce prin intermediul sintezei acetilenice. În cadrul acesteia, acidul clorhidric reacționează cu vinilacetilena astfel: [2]
Această sinteză are câteva dezavantaje, cum ar fi consumul mare de energie.
Procedeul modern de sintetizare al cloroprenului folosit de majoritatea fabricanților folosește butadiena în diferite forme. Un atom de clor se adiționează 1-2 la 1,3-butadienă dând 3,4-dicloro-1-butenă. Apoi se elimină un atom de hidrogen din poziția a 3-a și altul de clor din poziția a 4-a sub formă de HCl și se formează o legătură dublă între carbonii 3 și 4 ai moleculei, obținându-se cloroprenul.