Amalgam
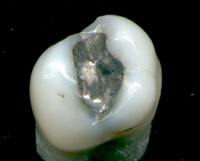
Un amalgam este un aliaj al mercurului cu un alt metal. [1] Aproape toate metalele pot forma amalgame cu mercurul, iar printre excepții se numără: fierul, nichelul, cobaltul, platina, wolframul și tantalul. Amalgamele de argint sunt importante în stomatologie (mai exact în odontologie), iar cele de aur sunt folosite la extracția aurului din minereu.
Amalgamele cu un conținut mic de metal străin, de până la 1%, sunt lichide, iar cele cu conținut mai mare sunt solide, uneori cristalizate. [2]
Tipuri[modificare | modificare sursă]
Amalgam dentar[modificare | modificare sursă]
Amalgamul dentar este un amestec al mercurului cu unele metale, precum argint, cupru, indiu, staniu și zinc. Este destul de ieftin și relativ ușor de manipulat în timpul folosirii în tehnica dentară.
Amalgam de potasiu[modificare | modificare sursă]
Reacția de amalgamare a metalelor alcaline este exotermă. În urma amalgamării potasiului se obțin diferite specii chimice, precum compuși intermetalici de forma KHg și KHg2.[3] KHg este un compus cu aspect auriu, cu un punct de topire de 178 °C, iar KHg2 este un compus argintiu, cu un punct de topire de 278 °C. Aceste amalgame sunt foarte sensibile față de aer și apă, dar pot fi manipulate sub azot. Distanța dintre cei doi atomi de mercur Hg-Hg este de aproximativ 300 picometri, în timp ce distanța dintre Hg-K este de aproximativ 358 pm.[3]
Amalgam de sodiu[modificare | modificare sursă]
Reacția de amalgamare a sodiului este puternic exotermă și are loc cu o degajare puternică de căldură. Se obțin diverse specii chimice, precum Hg4Na, Hg2Na, HgNa3, etc. [2] În prezența apei, amalgamul de sodiu se descompune într-o soluție de hidroxid de sodiu concentrată, hidrogen și mercur. Dacă se folosește alcool absolut în locul apei, se formează un alcoxid de sodiu în locul soluției alcaline.
Vezi și[modificare | modificare sursă]
Note[modificare | modificare sursă]
- ^ „Amalgam” la DEX online Accesat pe 28 mai 2016
- ^ a b Nenițescu, Costin D. Chimie Generală. București: Editura Didactică și Pedagogică. pp. 1069–1070.
- ^ a b E J Duwell; N C Baenziger (). „The Crystal Structures of KHg and KHg2”. Acta Crystallogr. 8 (11): 705–710. doi:10.1107/S0365110X55002168.
