Lizozim

Lizozimul (muramidază) este o enzimă bacteriolitică cu greutate moleculară de 14,4 kiloDaltoni(kDa). Are capacitatea de a distruge peretele celular al bacteriilor Gram-pozitive (în special), prin hidrolizarea legăturii glicozidice β-1,4 dintre acidul N-acetilmuramic (NAM) și N-acetilglucozamină (NAG) (carbohidrați prezenți în peretele bacterian). Se găsește în cantitate mare în secreții, cum ar fi: lacrimi, salivă și mucus, în citoplasma neutrofilelor polimorfonucleare (PMN), dar cea mai mare cantitate de lizozim se întâlnește în albușul de ou.
Istoric[modificare | modificare sursă]
Lizozimul a fost descoperit de Alexander Fleming, în 1921, în timp ce savantul încerca să demonstreze că propriul mucus nazal are capacitatea de a inhiba creșterea unei bacterii în cultură. El a realizat că acest fapt se datora unei proteine prezente în mucus, care determina liza celulei bacteriene. Și astfel a numit proteina, lizozim.[1] Într-un studiu ulterior, împreună cu colaboratorul său, V.D. Allison, au detectat lizozim în serul sangvin uman, salivă, lapte și alte lichide biologice.
În ciuda activității sale antimicrobiene, lizozimul s-a dovedit a fi ineficient împotriva bolilor cauzate de bacterii. Ineficiența lizozimului asupra bacteriilor patogene a fost interpretată de Fleming ca fiind de fapt eficiența împotriva unor anumite bacterii care, în absența lizozimului ar fi patogene, însă prezența lui le contracarează acțiunea, ele fiind astfel considerate nepatogene.[2] Acest lucru a stimulat interesul lui Fleming asupra agenților antimicrobieni, ceea ce l-a condus la descoperirea penicilinei în 1928, pentru care a primit Premiul Nobel în 1945. În 1966, David Chilton Phillips, utilizând cromatografia cu raze X, a determinat structura lizozimului, prima descifrare a unei enzime. În urma muncii sale, Phillips a reușit să explice mecanismul activității catalitice a lizozimului.
Structura lizozimului[modificare | modificare sursă]
Fiind o proteină, lizozimul prezintă trei nivele de organizare a structurii sale:
Structura primară[modificare | modificare sursă]
Structura primară a lizozimului este un polipeptid care conține 129 aminoacizi aranjați într-o secvență liniară. Cele opt resturi de cisteină participă la formarea a patru legături disulfurice dispuse la diferite distanțe ale lanțului. Acei aminoacizi care fac parte din situsul aparent de legare al substratului sunt mascați.[3]
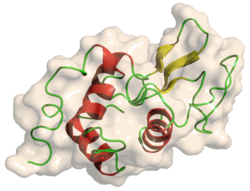
Structura secundară[modificare | modificare sursă]
Lizozimul are 5 regiuni helicale (3 sunt α helix standard, în timp ce două sunt intermediari între 3-10 helix și α helix), 5 regiuni de foi β pliate, la întâmplare și β turns.
Structura terțiară[modificare | modificare sursă]
În condiții fiziologice, lizozimul se împachetează într-o structură compactă, globulară, după principiul: partea hidrofobă în interior iar partea hidrofilă la exterior, cu o despicătură lungă pe suprafața proteinei. Această crăpătură este situsul activ implicat în legarea de carbohidratul bacterian (NAM/NAG) și în cele din urmă în scindarea acestuia.
Caracteristici fizico-chimice[modificare | modificare sursă]
- Greutate moleculară: 14,388 kDa (Jollés, 1969)
- Compoziție: 129 aminoacizi aranjați într-o secvența liniară pentru a forma un singur lanț polipeptidic
- pH-ul optim: 9,2 (Davies și col., 1969)
- Coeficientul de extincție: E281,5 = 26,4 (Aune și Tanford,1969)
- Punctul izoelectric: pI = 11,0 (Alderton și col., 1945)
- Inhibitori: enzima este inhibată de suprafața activă a reactivilor cum ar fi dodecil-sulfatul, alcooli și acizii grași (Smith și Stoker, 1949). Derivații imidazolului și ai indolului sunt inhibitori ai formării complexelor schimb-transfer (Shinitzky și col. 1966; Swan 1972)
Note[modificare | modificare sursă]
- ^ Fleming A. On a remarkable bacteriolytic element found in tissues and secretion. Proc Roy Soc Ser B, 93, 306-317, 1922
- ^ Maurois, A. Alexander Fleming, Editura Medicală, 1965
- ^ Canfield and Liu, J. Biol. Chem. 240, 1997
