Carbonat de potasiu
Aspect
| Carbonat de potasiu | |
 | |
 | |
 | |
| Denumiri | |
|---|---|
| Alte denumiri | Potasă |
| Identificare | |
| Număr CAS | 584-08-7 |
| ChEMBL | CHEMBL2105894 |
| PubChem CID | 516886 11430, 516886 |
| Informații generale | |
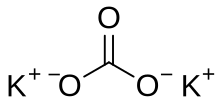
| Formulă chimică | K2CO3 |
| Aspect | solid alb higroscopic |
| Masă molară | 138,205 g/mol |
| Proprietăți | |
| Densitate | 2,43 g/cm3 |
| Starea de agregare | solidă |
| Punct de topire | 891 °C |
| Punct de fierbere | se descompune |
| Solubilitate în apă | |
| 112 g/100 mL (20 °C) 156 g/100 mL (100 °C) | |
| Pericol | |
| Fraze R | R22, R36, R37, R38 |
| Fraze S | R? |
| NFPA 704 | |
| Sunt folosite unitățile SI și condițiile de temperatură și presiune normale dacă nu s-a specificat altfel. | |
| Modifică date / text | |
Carbonatul de potasiu este sarea potasiului cu acidul carbonic și are formula K2CO3. Este un solid alb, solubil în apă și insolubil în metanol, [2] care formează o soluție puternic alcalină. Compusul poate fi obținut în urma reacției dintre hidroxid de potasiu și dioxidul de carbon din atmosferă. Carbonatul de potasiu este delicvescent și adesea are aspectul unui solid umed, și de asemenea este utilizat în producerea săpunurilor și sticlei.
Obținere
[modificare | modificare sursă]În prezent, carbonatul de potasiu poate fi fabricat prin electroliza clorurii de potasiu. În urma acestui proces se obține hidroxid de potasiu, care poate fi carbonatat folosindu-se dioxid de carbon:
Referințe
[modificare | modificare sursă]- ^ „Carbonat de potasiu”, POTASSIUM CARBONATE (în engleză), PubChem, accesat în
- ^ Solubility of Potassium Carbonate and Potassium Hydrocarbonate in Methanol



