Ligamentul încrucișat anterior
| Ligament încrucișat anterior | |
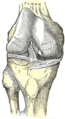
 Diagrama genunchiului drept. Ligament anterior încrucișatetichetat în centrul imaginii. | |
| Detalii | |
|---|---|
| Latină | ligamentum cruciatum anterius |
| Parte din | knee joint[*] |
| Resurse externe | |
| Gray's | p.342 |
| TA | A03.6.08.007 |
| FMA | 44614 |
| Terminologie anatomică | |
Ligamentul încrucișat anterior (LIA sau ACL în engleză) este unul din cele două ligamente încrucișate (celălalt fiind ligamentul încrucișat posterior) ale genunchiului uman. Cele două ligamente sunt numite și ligamente „cruciforme”, deoarece sunt dispuse într-o formațiune încrucișată.[1] Numele încrucișat este potrivit deoarece LIA traversează ligamentul încrucișat posterior pentru a forma un „X”. Este compus din material puternic, fibros și ajută la controlul mișcării excesive a articulației genunchiului. Acest lucru se realizează prin limitarea mobilității articulației. Ligamentul încrucișat anterior este unul dintre cele patru ligamente principale ale genunchiului, rolul său principal fiind acela de stabilizator al genunchiului.[2] LIA este ligamentul care este accidentat cel mai des dintre cele patru ligamente ale genunchiului.
Structură[modificare | modificare sursă]
LIA provine din adâncul crestăturii femurului distal. Fibrele sale proximale se extind de-a lungul peretelui medial al condilului femural lateral. Cele două fascicule ale LIA sunt anteromedial și posterolateral, denumite în funcție de locul în care fasciculele se introduc în platoul tibial. Platoul tibial este o regiune critică care suportă greutăți pe extremitatea superioară a tibiei. LIA se atașează în fața eminenței intercondiliene a tibiei, unde se îmbină cu cornul anterior al meniscului medial .
Scop[modificare | modificare sursă]
Scopul LIA este de a rezista mișcărilor de translație a tibiei anterioare și de rotație a tibiei interne; acest lucru este important pentru a avea stabilitate de rotație.[3] Această funcție previne subluxația tibială anterioară a articulațiilor tibiofemurale laterale și mediale, ceea ce este important pentru fenomenul pivot-shift.[3] LIA are mecanoreceptori care detectează modificări ale direcției de mișcare, poziției articulației genunchiului și modificări ale accelerației, vitezei și tensiunii.[4] Un factor cheie în instabilitatea după leziunile LIA este modificarea funcției neuromusculare secundară diminuării informațiilor somatosenzoriale.[4] Pentru sportivii care participă la sporturi care implică schimbări rapide de direcție, pivotări, sărituri și decelerare rapidă, genunchiul trebuie să fie stabil în extensia terminală, care reprezintă mecanismul de șurub.[4]
Semnificație clinică[modificare | modificare sursă]
Rănire[modificare | modificare sursă]

O ruptură de LIA este una dintre cele mai frecvente leziuni ale genunchiului.[5] Cele mai multe rupturi LIA sunt rezultatul unui mișcări fără contact, cum ar fi o schimbare bruscă a direcției care determină rotirea genunchiului spre interior.[6] Pe măsură ce genunchiul se rotește spre interior, se exercită o presiune suplimentară asupra LIA, deoarece femurul și tibia, care sunt cele două oase care se articulează împreună formând articulația genunchiului, se mișcă în direcții opuse, provocând ruperea LIA. Majoritatea sportivilor necesită o intervenție chirurgicală reconstructivă a LIA, în care LIA rupt este complet îndepărtat și înlocuit cu o bucată de țesut de tendon sau ligament de la pacient (autogrefă) sau de la un donator (alogrefă).[7] Tratamentul conservator are rezultate slabe în leziunile LIA, deoarece LIA nu poate forma un cheag fibros, deoarece primește majoritatea nutrienților din lichidul sinovial; aceasta spăla celulele reparatoare, îngreunând formarea țesutului fibros. Cele mai frecvente două surse de țesut sunt ligamentul rotulian și tendonul ischiochimbilor.[8] Ligamentul patelar este adesea folosit, deoarece sunt extrase dopuri osoase de la fiecare capăt al grefei, ceea ce ajută la integrarea grefei în tunelurile osoase în timpul reconstrucției.[9] Operația este artroscopică, ceea ce înseamnă că o cameră minusculă este introdusă printr-o tăietură chirurgicală mică.[7] Camera trimite video la un monitor mare, astfel încât chirurgul să poată vedea orice deteriorare a ligamentelor. În cazul unei autogrefe, chirurgul face o tăietură mai mare pentru a obține țesutul necesar. În cazul unei alogrefe, în care materialul este donat, acest lucru nu este necesar, deoarece nu este prelevat niciun țesut direct din propriul corp al pacientului.[10] Chirurgul realizează o gaură care formează tunelul osos tibial și tunelul osos femural, permițând ghidarea noii grefe de LIA a pacientului.[10] Odată ce grefa este trasă prin tunelurile osoase, două șuruburi sunt plasate în tunelul osos tibial și femural.[10] Timpul de recuperare variază de obicei între unu și doi ani, dar uneori este mai lung, depinzând dacă pacientul a ales o autogrefă sau o alogrefă.
La aproximativ o săptămână după producerea accidentării și rănirii LIA, sportivul este de obicei înșelat de faptul că poate merge normal și nu simte prea multă durere.[10] Acest lucru este periculos, întrucât unii sportivi încep să-și reia unele activități precum jogging-ul, care printr-o mișcare sau răsucire greșită, ar putea deteriora oasele. Sportivii accidentați trebuie să înțeleagă semnificația fiecărui pas al unei leziuni LIA pentru a evita complicațiile și pentru a asigura o recuperare adecvată.
Tratamentul nonoperator al LIA[modificare | modificare sursă]
Reconstrucția LIA este cel mai frecvent tratament pentru o ruptură LIA, dar nu este singurul tratament disponibil. Unii ar putea considera că este mai benefic să finalizeze un program de reabilitare nonoperator. Ruta nonoperatorie se adresează atât persoanelor care urmează să continue cu activitatea fizică care implică pivotarea, precum și celor care nu mai participă la acele activități specifice.[11] În compararea abordărilor operatorii și nonoperatorii ale rupturilot LIA, au fost observate puține diferențe între grupurile chirurgicale și nechirurgicale, fără diferențe semnificative în ceea ce privește funcția genunchiului sau forța musculară raportată de pacienți.[12]
Principalele obiective de atins în timpul reabilitării unei rupturi de LIA este de a recăpăta o stabilitate funcțională suficientă, de a maximiza puterea musculară completă și de a scădea riscul de rănire.[13] De obicei, trei faze sunt implicate în tratamentul nonoperator - faza acută, faza de antrenament neuromuscular și faza de revenire la sport. În timpul fazei acute, reabilitarea se concentrează pe simptomele acute care apar imediat după accidentare și care cauzează neplăceri. Utilizarea exercițiilor terapeutice și a modalităților terapeutice adecvate este crucială în această fază pentru a ajuta la repararea deficiențelor cauzate de vătămare. Faza de antrenament neuromuscular este folosită pentru a ca pacientul să își recapete puterea maximă atât la nivelul extremității inferioare, cât și a mușchilor de bază. Această fază începe atunci când pacientul își recapătă întreaga gamă de mișcare, fără a forța suplimentar extremitățile inferioare. În această fază, pacientul realizează echilibru avansat, propriocepție, condiționare cardiovasculară și intervenții neuromusculare.[14] În faza finală, revenirea la sport, pacientul se concentrează pe activități specifice sportului și pe agilitate. Se recomandă utilizarea unei orteze de performanță pentru stabilizarea genunchiului în timpul activităților de pivotare.
Tratamentul operator al LIA[modificare | modificare sursă]
Chirurgia ligamentului încrucișat anterior este o operație complexă care necesită expertiză în domeniul medicinei ortopedice și sportive. Mulți factori ar trebui să fie luați în considerare atunci când discutăm despre intervenția chirurgicală, inclusiv nivelul de competiție al sportivului, vârsta, accidentarea anterioară a genunchiului, alte leziuni suferite, alinierea picioarelor și alegerea grefei. În mod obișnuit, sunt posibile patru tipuri de grefă, grefa os-rotulă-tendon-os, tendoanele semitendinoase și gracilis (tendonul ischio-jambier cvadruplu), tendonul cvadricepsului și o alogrefă.[15] Deși s-au efectuat cercetări ample despre care grefe sunt cele mai bune, chirurgul alege de obicei tipul de grefă cu care este cel mai confortabil. Dacă este reabilitată corect, reconstrucția ar trebui să dureze. De fapt, 92,9% dintre pacienți sunt mulțumiți de alegerea grefei.[15]
Preabilitarea a devenit o parte integrantă a procesului de reconstrucție a LIA. Aceasta înseamnă că pacientul face exerciții înainte de operație pentru a menține factori precum amplitudinea de mișcare și puterea. Pe baza unui test de hop cu un singur picior și a unei evaluări auto-raportate, funcția prehab a îmbunătățit; aceste efecte au fost susținute la 12 săptămâni postoperator.[16]
Reabilitarea postchirurgicală este esențială în recuperarea după reconstrucție. Acest lucru durează de obicei de la 6 luni până la 12 luni pentru ca pacientul să revină la viață așa cum era înainte de vătămare.[17] Reabilitarea poate fi împărțită în etapele: protecția grefei, îmbunătățirea amplitudinii de mișcare, reducerea umflăturilor și recăpătarea controlului muscular.[17] Fiecare fază are exerciții diferite în funcție de nevoile pacienților. De exemplu, în timp ce ligamentul se vindecă, articulația pacientului nu ar trebui folosită pentru a suporta greutățile, dar pacientul ar trebui să întărească cvadricepsul și ischiobigiolarele făcând seturi de exerciții de schimbare a greutății. Faza a doua necesită pentru pacient susținerea completă a greutății și corectarea tiparelor de mers și presupune exerciții precum cele de echilibru. În faza a treia pacientul începe să alerge și poate face antrenamente acvatice pentru a ajuta la reducerea stresului articular și a rezistenței cardiorespiratorii. Faza a patra include mișcări multiplanare și poate include un program de alergare și începerea exercițiilor de agilitate și pliometrice. În cele din urmă, faza cinci se concentrează pe mișcări specifice sportului sau vieții, în funcție de pacient.[17]
O analiză din 2010 din Los Angeles Times a două studii medicale a discutat dacă reconstrucția LIA este recomandabilă. Un studiu a constatat că la copiii sub 14 ani care au avut reconstrucție LIA rezultatele după o intervenție chirurgicală timpurie au fost mai bune decât cele a celor care au suferit o intervenție chirurgicală întârziată. Pentru adulții între 18 și 35 de ani, totuși, pacienții care au suferit o intervenție chirurgicală timpurie urmată de reabilitare nu s-au descurcat mai bine decât cei care au avut terapie de reabilitare și o intervenție chirurgicală ulterioară.[18]
Primul raport s-a concentrat pe copii și pe momentul reconstrucției LIA. Leziunile LIA la copii sunt o provocare, deoarece copiii au plăci de creștere deschise în partea inferioară a femurului sau a osului coapsei și în partea superioară a tibiei. O reconstrucție a LIA traversează de obicei plăcile de creștere, prezentând un risc teoretic de rănire a plăcii de creștere, oprind creșterea picioarelor sau determinând creșterea piciorului într-un unghi neobișnuit.
Cel de-al doilea studiu s-a concentrat pe adulți. Nu a găsit nicio diferență statistică semnificativă în ceea ce privește performanța și rezultatele durerii pentru pacienții care primesc reconstrucție precoce a LIA față de cei care primesc terapie fizică cu opțiune pentru o intervenție chirurgicală ulterioară. Acest lucru ar sugera că mulți pacienți fără instabilitate, flambare sau cedare după un curs de reabilitare pot fi gestionați nonoperator, dar a fost limitat la rezultate după doi ani și nu a implicat pacienți care erau sportivi în activitate.[19] Pacienții implicați în sporturi care necesită pivotare, răsucire sau accelerare sau decelerare rapidă ar putea să nu poată participa la aceste activități fără reconstrucția LIA. [20]
Leziuni LIA la femei[modificare | modificare sursă]
Diferențele de risc între rezultatele leziunilor LIA la bărbați și femei pot fi atribuite unei combinații de factori multipli, inclusiv factori anatomici, hormonali, genetici, poziționali, neuromusculari și de mediu.[21] Dimensiunea ligamentului încrucișat anterior este adesea cea mai raportată diferență. Studiile analizează lungimea, aria secțiunii transversale și volumul LIA-urilor. Cercetătorii folosesc cadavre și plasarea in vivo pentru a studia acești factori, iar majoritatea studiilor confirmă că femeile au ligamente încrucișate anterioare mai mici. Alți factori care ar putea contribui la riscuri mai mari de ruptură de LIA la femei includ greutatea și înălțimea pacientului, dimensiunea și adâncimea crestăturii intercondiliene, diametrul LIA, mărimea pantei tibiale, volumul coloanelor tibiale, convexitatea suprafetelor articulare tibio-femurale laterale si a concavitatii platoului tibial medial.[22] În timp ce se vorbește cel mai mult despre factorii anatomici, factorii extrinseci, inclusiv modelele dinamice de mișcare, ar putea fi cel mai important factor de risc atunci când vine vorba de leziunea LIA.[23] Factorii de mediu joacă, de asemenea, un rol important. Factorii extrinseci sunt controlați de individ. Acestea ar putea fi puterea, condiționarea, pantofii purtați și motivația.
Galerie[modificare | modificare sursă]
-
Articulația genunchiului drept, din față, prezentând ligamentele interioare
-
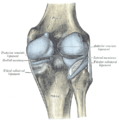
Articulația genunchiului stâng din spate, arătând ligamentele interioare
-
Capul tibiei drepte văzut de sus, prezentând meniscurile și atașamentele ligamentelor
-
Capsula articulației genunchiului drept (distens), aspect posterior
-
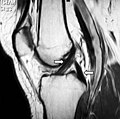
RMN-ul arată semnal normal al ambelor ligamente încrucișate (săgeți)
-
Articulația genunchiului, disecție profundă, vedere anteromedială
Vezi și[modificare | modificare sursă]
Note[modificare | modificare sursă]
- ^ „Canine Cranial Cruciate Ligament Disease” (PDF). Melbourne Veterinary Referral Centre. pp. 1–2. Arhivat din original (PDF) la . Accesat în .
- ^ Ellison, A. E.; Berg, E. E. (). „Embryology, anatomy, and function of the anterior cruciate ligament”. The Orthopedic Clinics of North America. 16 (1): 3–14. doi:10.1016/S0030-5898(20)30463-6. PMID 3969275.
- ^ a b Noyes, Frank R. (ianuarie 2009). „The Function of the Human Anterior Cruciate Ligament and Analysis of Single- and Double-Bundle Graft Reconstructions”. Sports Health. 1 (1): 66–75. doi:10.1177/1941738108326980. ISSN 1941-7381. PMC 3445115
 . PMID 23015856.
. PMID 23015856.
- ^ a b c Liu-Ambrose, T. (decembrie 2003). „The anterior cruciate ligament and functional stability of the knee joint”. British Columbia Medical Journal (în engleză). 45 (10): 495–499. Accesat în .
- ^ Cimino, Francesca; Volk, Bradford Scott; Setter, Don (). „Anterior Cruciate Ligament Injury: Diagnosis, Management, and Prevention”. American Family Physician (în engleză). 82 (8): 917–922. ISSN 0002-838X. PMID 20949884.
- ^ MD, Michael Khadavi, MD and Michael Fredericson. „ACL Injury: Causes and Risk Factors”. Sports-health (în engleză). Accesat în .
- ^ a b „ACL reconstruction - Mayo Clinic”. www.mayoclinic.org (în engleză). Accesat în .
- ^ Samuelsen, Brian T.; Webster, Kate E.; Johnson, Nick R.; Hewett, Timothy E.; Krych, Aaron J. (octombrie 2017). „Hamstring Autograft versus Patellar Tendon Autograft for ACL Reconstruction: Is There a Difference in Graft Failure Rate? A Meta-analysis of 47,613 Patients”. Clinical Orthopaedics and Related Research. 475 (10): 2459–2468. doi:10.1007/s11999-017-5278-9. ISSN 1528-1132. PMC 5599382
 . PMID 28205075.
. PMID 28205075.
- ^ „When Would You Use Patellar Tendon Autograft as Your Main Graft Selection?”. www.healio.com (în engleză). Accesat în .
- ^ a b c d „ACL Injury: Does It Require Surgery? - OrthoInfo - AAOS”. Accesat în .
- ^ Paterno, Mark V. (). „Non-operative Care of the Patient with an ACL-Deficient Knee”. Current Reviews in Musculoskeletal Medicine. 10 (3): 322–327. doi:10.1007/s12178-017-9431-6. ISSN 1935-973X. PMC 5577432
 . PMID 28756525.
. PMID 28756525.
- ^ „Options for nonoperative treatment of ACL injuries exist, but remain controversial” (în engleză). Accesat în .
- ^ Physiopedia Contributors (). „Anterior Cruciate Ligament (ACL) Rehabilitation”. Physiopedia.
- ^ Paterno, Mark V. (). „Non-operative Care of the Patient with an ACL-Deficient Knee”. Current Reviews in Musculoskeletal Medicine. 10 (3): 322–327. doi:10.1007/s12178-017-9431-6. ISSN 1935-973X. PMC 5577432
 . PMID 28756525.
. PMID 28756525.
- ^ a b Macaulay, Alec A.; Perfetti, Dean C.; Levine, William N. (ianuarie 2012). „Anterior Cruciate Ligament Graft Choices”. Sports Health. 4 (1): 63–68. doi:10.1177/1941738111409890. ISSN 1941-7381. PMC 3435898
 . PMID 23016071.
. PMID 23016071.
- ^ Shaarani, Shahril R.; O'Hare, Christopher; Quinn, Alison; Moyna, Niall; Moran, Raymond; O'Byrne, John M. (septembrie 2013). „Effect of prehabilitation on the outcome of anterior cruciate ligament reconstruction”. The American Journal of Sports Medicine. 41 (9): 2117–2127. doi:10.1177/0363546513493594. ISSN 1552-3365. PMID 23845398.
- ^ a b c „Rehabilitation Guidelines for ACL Reconstruction in the Adult Athlete (Skeletally Mature)” (PDF). UW Health. Arhivat din original (PDF) la . Accesat în .
- ^ Stein, Jeannine (). „Studies on ACL surgery”. The Los Angeles Times. Arhivat din original la . Accesat în .
- ^ Stein, Jeannine (). „Studies on ACL surgery”. The Los Angeles Times. Arhivat din original la . Accesat în .
- ^ Frobell, Richard B.; Roos, Ewa M.; Roos, Harald P.; Ranstam, Jonas; Lohmander, L. Stefan (). „A Randomized Trial of Treatment for Acute Anterior Crut Tears”. New England Journal of Medicine. 363 (4): 331–342. doi:10.1056/NEJMoa0907797. PMID 20660401.
- ^ Chandrashekara, Naveen; Mansourib, Hossein; Slauterbeckc, James; Hashemia, Javad (). „Sex-based differences in the tensile properties of the human anterior cruciate ligament”. Journal of Biomechanics. 39 (16): 2943–2950. doi:10.1016/j.jbiomech.2005.10.031. PMID 16387307.
- ^ Schneider, Antione; Si-Mohamed, Salim; Magnussen, Robert; Lustig, Sebastien; Neyret, Philippe; Servien, Elvire (octombrie 2017). „Tibiofemoral joint congruence is lower in females with ACL injuries than males with ACL injuries”. Knee Surgery, Sports Traumatology, Arthroscopy. 25 (5): 1375–1383. doi:10.1007/s00167-017-4756-7. PMID 29052744.
- ^ Lloyd Ireland, Mary (). „The female ACL: why is it more prone to injury?”. Orthopedic Clinics of North America. 33 (2): 637–651. doi:10.1016/S0030-5898(02)00028-7. PMC 4805849
 . PMID 12528906.
. PMID 12528906.