Oxidare organică
Oxidarea organică diferă de cea din domeniul chimiei anorganice și aceasta deoarece nu are loc transferul propriu-zis de electroni. Oxidarea speciilor chimice are loc cu:
- cedare de hidrogen -reacția se numește dehidrogenare
- acceptare de oxigen-reacția se numește oxidare.
Tipuri de reacții[modificare | modificare sursă]
Oxidarea alcanilor[modificare | modificare sursă]
- Toți alcanii reacționează cu aerul sau oxigenul, în urma acestor reacții rezultând produși cu diferite trepte de oxidare. Ecuația generala de oxidare totală sau a arderii este:
Reacția este puternic exotermă cu o entalpie standard de formare ΔH=-886kJmol-1.Pentru fiecare grupare -CH2 valoarea acestei entalpii crește cu circa 650kJ;se pare că lanțurile ramificate ale alcanilor au o valoare mult mai mică față de lanțurile liniare cu același număr de atomi de carbon, fapt care se pare că explică și stabilitatea lor mult mai mare.
- Arderea incompletă a alcanilor duce la formarea de amestecuri de substanțe: etanul de exemplu dă prin oxidare un amestec de alcool metilic (CH 3-OH), C2H5-OH(etanol sau alcool etilic), CH3-CHO (aldehidă acetică) și CH3COOH (acid acetic). Metanul prin ardere incompletă dă naștere la așa numitul gaz de sinteză, o sursă importantă de sinteză pentru mulți compuși organici:
- La oxidarea alcanilor superiori are loc o rupere a moleculei cu formare de acizi carboxilici(mono)
Reacția are loc prin încălzire la 1000C, în prezența de stearat de zinc, sau a permanganatului de potasiu.
Oxidarea alchenelor[modificare | modificare sursă]
- Alchenele suferă o reacție de oxidare în mediu puternic acid în prezență de acid sulfuric și de bicromat de potasiu sau permanganat de potasiu.
![]() ;
Reacțiile prezintă importanță pentru stabilirea structurii alchenelor disubstituite(atomii de hidrogen ai carbonilor dublei legături sunt substituiți cu radicali diferiți).
;
Reacțiile prezintă importanță pentru stabilirea structurii alchenelor disubstituite(atomii de hidrogen ai carbonilor dublei legături sunt substituiți cu radicali diferiți).
- Reacția Prilejaev, o reacție de epoxidare [1] alchenelor cu peracizi organici (de regulă acidul meta-cloroperbenzoic sau acidul perbenzoic), conduce la formarea de epoxizi
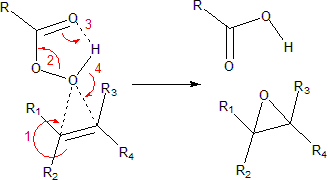
Reacția are loc la temperaturi scăzute, este dată de majoritatea alchenelor.
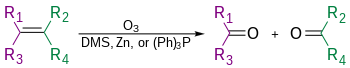
Oxidarea alchinelor[modificare | modificare sursă]
Alchinele se oxidează[3] Arhivat în , la Wayback Machine. mult mai greu decît alchenele, reacția avînd loc numai în prezența unor oxidanți foarte puternici de tipul ozonului, capabili să rupă tripla legătură:
Oxidarea arenelor[modificare | modificare sursă]
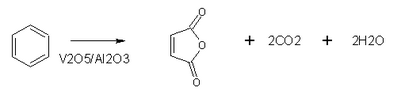
- Benzenul adiționează ozonul formând o triozonidă instabilă, explozivă.

Benzenul se oxidează în condiții energice, catalizator pentaoxidul de vanadiu V2O5, temperaturi de 4500C.
- Omologii superiori ai benzenului se oxidează la catena laterală cu formare de acid benzoic.
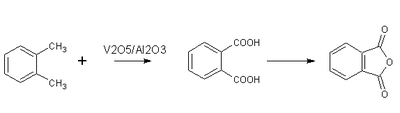
- Xilenii formează acizii corespunzători
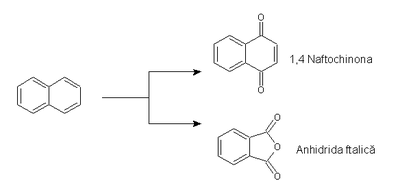
- Naftalina are 2 căi de oxidare: cu acidul cromic sau cu oxigen molecular/V2O5.
- Antracenul se oxidează cu acid cromic (K2Cr2O7/H2SO4) dar și cu săruri de ceriu/acid azotic[4]

- Antracenul poate adiționa oxigen formînd un fotoxid:

- Arenele polinucleare de tipul benzopirenului[5] Arhivat în , la Wayback Machine.(un poluant foarte des întîlnit),sunt transformate prin intermediul unei enzime (epoxidaza hepatică)în 7,8 dihidroxi-9,10 epoxi7,8,9,10 tetrahidrobenzopiren.

Oxidarea alcoolilor[modificare | modificare sursă]
Alcooli suferă reacția de oxidare sau de dehidrogenare trecând în compuși carbonilici., sau acizi carboxilici
- Alcoolii primari se oxidează la aldehidă care poate oxidată până la acid carboxilic:
;
- Alcoolii secundari se transformă în cetonă:
;
- Oxidarea Swern[6] Arhivat în , la Wayback Machine.
Alcooli sunt oxidați la aldehide prin intermediul sulfoxizilor.

- Oxidarea biochimică.
Etanolul este oxidat în organism de către alcool dehidrogenază[7].
La acest proces participă și niște substanțe denumite coenzime sau cofactori, de tipul NAD (nicotinamidadinucleotid); acesta joacă rol de acceptor de electroni astfel că procersul poate fi exprimat astfel:
Bibliografie[modificare | modificare sursă]
- en Epoxide
- en IUPAC.org
- en Organic-chemistry.org
- en CEM.MSU.edu Arhivat în , la Wayback Machine.
- en Chem.uic.edu Arhivat în , la Wayback Machine.
- en Pubs.Acs.org
- en Ctarr.MyWeb.uga.edu Arhivat în , la Wayback Machine.
- en Faculty.Mansfield.edu[nefuncțională]
| ||||||||||||||||||||




![{\displaystyle +5[O]\longrightarrow R-COOH+CO_{2}+H_{2}O}](https://wikimedia.org/api/rest_v1/media/math/render/svg/b913c38fa50539620ef762aa83f964e944a1eeab)

![{\displaystyle +3[O]\longrightarrow {\begin{matrix}R-&C=O\\\quad /&\\R&\end{matrix}}+R'-COOH}](https://wikimedia.org/api/rest_v1/media/math/render/svg/0b2fc9e83f05d31a9e9d7268cef88ee0ecb10b1c)
![{\displaystyle +4[O]\longrightarrow R-COOH+R'-COOH}](https://wikimedia.org/api/rest_v1/media/math/render/svg/f3bc992ffe6f3051706583b5a24048fe2dc738b8)

![{\displaystyle R-CH_{2}-OH+[O]\longrightarrow R-CHO+[O]\longrightarrow R-COOH}](https://wikimedia.org/api/rest_v1/media/math/render/svg/72a601f07b7bf6d7c4ff9963dbebf39569bac8ad)
![{\displaystyle {\begin{matrix}R-&CH-OH\\\quad /&\\R'&\end{matrix}}+[O]\longrightarrow {\begin{matrix}R-&CH-O\\\quad /&\\R'&\end{matrix}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/f2c4d14176c89f48e58dbf27d62d5f18ac92a6ba)

