Reacție Eschweiler-Clarke
Reacția Eschweiler-Clarke (de asemenea denumită și metilare Eschweiler-Clarke) este o reacție chimică de metilare (alchilare) în urma căreia o amină primară sau secundară este metilată cu un amestec de acid formic și formaldehidă.[1][2][3][4] Este și un tip de aminare reductivă, de aceea în urma acestei reacții nu se pot obține săruri de amoniu cuaternar, iar ultimul produs de reacție posibil este o amină terțiară. Reacția a fost denumită după chimistul german Wilhelm Eschweiler (1860-1936) și după chimistul britanic Hans Thacher Clarke (1887-1972).

Mecanism de reacție
[modificare | modificare sursă]Prima etapă de metilare a aminei începe cu formarea unui intermediar imină în urma reacției cu formaldehida. Acidul formic este o sursă de ion hidrură și are rolul de a reduce imina la amină secundară. Formarea de dioxid de carbon gazos care se elimină din mediul de reacție favorizează desfășurarea mecanismului. În mod similar se obține amina terțiară, dar reacția decurge mai lent din cauza dificultății formării ionului iminiu.
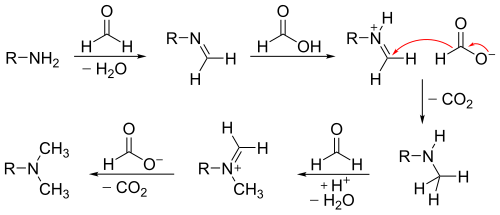
Din schema mecanismului se poate observa că formarea unei sări de amoniu nu este posibilă, deoarece amina terțiară nu poate să formeze o imină sau un ion iminiu. De obicei, în aceste condiții aminele chirale nu racemizează.[5]
Vezi și
[modificare | modificare sursă]Note
[modificare | modificare sursă]- ^ Eschweiler, W. (). „Ersatz von an Stickstoff gebundenen Wasserstoffatomen durch die Methylgruppe mit Hülfe von Formaldehyd”. Ber. 38: 880–882. doi:10.1002/cber.190503801154.
- ^ Clarke, H. T.; Gillespie, H. B.; Weisshaus, S. Z. (). „The Action of Formaldehyde on Amines and Amino Acids”. Journal of the American Chemical Society. 55 (11): 4571. doi:10.1021/ja01338a041.
- ^ Moore, M. L. (). „The Leuckart Reaction”. Org. React. 5: 301–330. doi:10.1002/0471264180.or005.07. ISBN 0471264180.
- ^ Icke, R. N.; Wisegarver, B. B.; Alles, G. A. (), „β-Phenylethyldimethylamine”, Org. Synth.; Collective Volume, 3, p. 723
- ^ Farkas, Eugene; Sunman, Cheryl J. (). „Chiral synthesis of doxpicomine”. J. Org. Chem. 50 (7): 1110. doi:10.1021/jo00207a037.)
