Baterie alcalină

Bateriile alcaline sunt un tip de baterii a căror sursă de energie electrică este dependentă de reacția chimică dintre zincul metalic și dioxidul de mangan.
Procese chimice
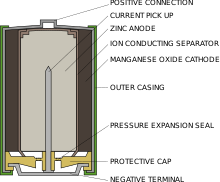
[modificare | modificare sursă]Într-o baterie alcalină, electrodul negativ este zincul metalic, iar cel pozitiv este format din dioxid de mangan (MnO2). Electrolitul, de obicei hidroxid de potasiu, nu este consumat în timpul reacției deoarece cantitatea de ioni OH− consumată este egală cu cea produsă.
Semireacțiile care au loc sunt:[1][2]
- Zn(s) + 2OH−(aq) → ZnO(s) + H2O(l) + 2e− [Eoxidare° = +1.28 V]
- 2MnO2(s) + H2O(l) + 2e− → Mn2O3(s) + 2OH−(aq) [Ereducere° = +0.15 V]
Reacția totală este:
- Zn(s) + 2MnO2(s)
 ZnO(s) + Mn2O3(s) [e° = +1.43 V]
ZnO(s) + Mn2O3(s) [e° = +1.43 V]
Tensiune electrică
[modificare | modificare sursă]Tensiunea electrică nominală a unei baterii alcaline noi fabricate are standardul stabilit de 1,5 V. Totuși, tensiunea poate varia de la 1,5 la 1,65 V în funcție de puritatea dioxidului de mangan utilizat la fabricarea bateriei sau de conținutul de oxid de zinc din electrolit. Bateria descărcată poate prezenta o tensiune de 0,8 până la 1 V. O tensiune mărită poate fi realizată prin conectarea în serie a mai multor baterii (se poate ajunge la o tensiune de 4,5 până la 5 V).[3]
Vezi și
[modificare | modificare sursă]Referințe
[modificare | modificare sursă]- ^ Manual práctico de electricidad para ingenieros. Donald G. Fink. Editorial Reverté, 1981. ISBN 8429130268, pg.157
- ^ „Battery Chemistry Tutorial and FAQ from PowerStream describes the chemical properties of common and uncommon electrochemical cells”, Powerstream.com, accesat în
- ^ Reddy, David Linden, Thomas B. (). Linden's handbook of batteries (ed. 3). New York: McGraw-Hill. pp. 10–12. ISBN 0-07-135978-8.

