Acinetobacter baumannii
| Acinetobacter baumannii | |
 | |
| Clasificare științifică | |
|---|---|
| Supradomeniu | Biota |
| Domeniu | Bacteria |
| Regn | Pseudomonadati |
| Încrengătură | Pseudomonadota |
| Clasă | Gammaproteobacteria |
| Ordin | Pseudomonadales |
| Familie | Moraxellaceae |
| Gen | Acinetobacter |
| Nume binomial | |
| Acinetobacter baumannii[1] | |
| Bouvet, Grimont, 1986 | |
| Modifică date / text | |
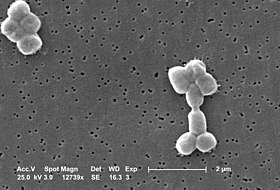
Acinetobacter baumannii este o bacterie gram-negativă, de obicei scurtă, aproape rotundă în formă de tijă (coccobacillus). Acesta poate fi un agent patogen oportunist la om, care afectează persoanele cu sistemul imunitar compromis, și care este din ce în ce mai frecvent cauza infecțiilor spitalicești (nosocomiale). În timp ce alte specii din genul Acinetobacter sunt adesea găsite în probe de sol (ceea ce duce la concepția greșită că A. baumannii este un organism care trăiește de asemenea în sol), A. baumannii este aproape exclusiv prezentă în medii spitalicești[2]. Deși ocazional a fost identificată în probe de sol și apă din natură[3], habitatul său natural este încă necunoscut.
Bacteriile din acest gen nu prezintă flagel, o structură ca un bici folosită pentru locomoție, dar prezintă motilitate prin spasme sau de grup. Acest lucru poate fi datorat activității pililor de tip IV, care pot fi extinși și retrași. Motilitatea în A. baumannii poate fi de asemenea datorată excreției de exopolizaharide, prin care se creează un film de polizaharide cu masă moleculară mare în urma bacteriei care îi permite astfel să avanseze[4]. Microbiologii clinici diferențieză membrii din genul Acinetobacter de alte Moraxellaceae prin efectuarea unui test al oxidazei, deoarece Acinetobacter spp. sunt singurii membri ai Moraxellaceae cărora le lipsesc oxidazele citocromului c[5].
A. baumannii este parte a complexului ACB (A. baumannii, A. calcoaceticus și speciile genomice Acinetobacter 13TU). Membrii complexului ACB sunt dificil de diferențiat și reprezintă membrii genului care sunt cei mai relevanți din punct de vedere clinic[6][7]. A. baumannii este de asemenea un patogen ESKAPE (Enterococcus faecium, Staphylococcus aureus, Klebsiella pneumoniae, Acinetobacter baumannii, Pseudomonas aeruginosa, Enterobacter sp.), un grup de agenți patogeni cu o rată ridicată de rezistență la antibiotice, care sunt responsabili de majoritatea infecțiilor nosocomiale[8].
Colocvial, A. baumannii este numită și „Iraqibacter” datorită apariției aparent bruște în spitalele militare din timpul Războiului din Irak[9]. Bacteria a continuat să fie o problemă pentru veteranii și soldații care au luptat în Irak și Afganistan. Tulpinile A. baumannii rezistente la antibiotice s-au răspândit în spitale civile, ca urmare a transportului de soldați infectați prin mai multe unități medicale[4].
Semne și simptome ale infecției[modificare | modificare sursă]
A. baumannii este un agent patogen oportunist, care profită de o serie de alte boli, fiecare cu propriile simptome. Unele infecții posibile în care poate apărea A. baumannii sunt:
- Pneumonie
- Infecții ale sângelui
- Meningită
- Infecțiilor postchirurgicale, inclusiv bacteria care cauzează fasceită necrozantă
- Infecții de tract urinar
Simptomele infecției cu A. baumannii sunt de multe ori imposibil de distins de alte infecții cauzate de alte bacterii oportuniste, precum Klebsiella pneumoniae și Streptococcus pneumoniae.
Simptomele infecției cu A. baumannii variază de la febră și frisoane, erupții cutanate, confuzie și/sau stare mentală alterată, dureri sau senzații de usturime la urinare, nevoia puternică de a urina frecvent, sensibilitate la lumină, greață (cu sau fără vărsături), dureri musculare și în piept, probleme de respirație și tuse (cu sau fără mucus galben, verde sau sângeros)[10]. În unele cazuri, A. baumannii poate să nu prezinte simptome sau urme de infecție, precum în cazul colonizării unei răni deschise sau traheostomii.
Tratament[modificare | modificare sursă]
Pentru că cele mai multe infecții sunt acum rezistente la mai multe medicamente, stabilirea susceptibilităților tulpinii este necesară pentru ca tratamentul să fie de succes. În mod tradițional, infecțiile au fost tratate cu imipenem sau meropenem, dar a fost observată o creștere constantă în A. baumannii rezistente la carbapenem[11]. În consecință, metodele de tratament de multe ori se bazează pe polimixine, în special colistin[12]. Colistinul este considerat un medicament de ultimă instanță pentru că de multe ori provoacă leziuni renale, printre alte efecte secundare[13]. Metodele de prevenire în spitale se concentrează pe creșterea frecvenței spălării mâinilor și îmbunătățirea procedurilor de sterilizare[14]. Acinetobacter baumannii a fost tratată recent cu ajutorul bacteriofagilor (virusuri anti-bacteriene)[15].

Incidența în spitale[modificare | modificare sursă]
Fiind cunoscută ca o infecție oportunistă, infecțiile cu A. baumanii sunt extrem de răspândite în spitale. A. baumanii prezintă risc foarte mic pentru persoanele sănătoase[16], dar factorii care cresc riscurile de infecție includ:
- Un sistem imunitar slăbit
- Boli pulmonare cronice
- Diabet
- Șederi prelungit în spital
- Boli care necesită utilizarea unui ventilator
- Răni deschise tratate într-un spital
- Tratamente care necesită dispozitive invazive, precum catetere urinare
A. baumanii se poate răspândi prin contact direct cu suprafețe, obiecte și pielea persoanelor contaminate[10].
Introducerea bacteriei A. baumannii și, ulterior, prezența în spitale este bine documentată[17]. A. baumannii este de obicei adusă în spital de un pacient colonizat. Datorită capacității sale de a supraviețui pe suprafețe artificiale și rezistenței la uscare, bacteria poate rămâne prezentă și infecta pacienți noi după mult timp. Dezvoltarea A. baumannii este suspectată a fi favorizată în spital datorită utilizării constante de antibiotice de către pacienții din spital[18]. Acinetobacter pot fi transmisă prin contactul dintre persoane sau prin contactul cu suprafețe contaminate[19]. Acinetobacter poate intra prin răni deschise, catetere și tuburi de respirat[20]. Într-un studiu din 2009 al unităților de terapie intensivă din Europa, A. baumannii a fost găsită responsabilă pentru 19,1% din cazurile de pneumonie asociată utilizării ventilatorului[21].
| Țară | Referință |
|---|---|
| Australia | [22][23] |
| Brazilia | [24][25][26][27] |
| China | [28][29][30][31] |
| Germania | [32][32][33][34] |
| India | [35][36][37] |
| Coreea De Sud | [38][39][40][41] |
| Regatul Unit | [42][43] |
| Statele Unite Ale Americii | [44][45][46][47] |
Un studiu din 2013 din Indonezia a arătat că infecțiile neonatale cu A. baumanii s-au datorat acelorași tulpini de bacterii găsite în spitalele în care nou-născuții au petrecut primele zile. Aceste tulpini au fost găsite pe suprafețe dure, precum și pe mâinile personalului medical[48].
Note[modificare | modificare sursă]
- ^ Species Acinetobacter baumannii (în engleză), LPSN[*], accesat în
- ^ Antunes, LCS; Visca, P; Towner, KJ (). „Acinetobacter baumannii: evolution of a global pathogen”. Pathogens and Disease. 71 (3): 292–301. doi:10.1111/2049-632X.12125. PMID 24376225.
- ^ Yeom, J; Shin, JH; Yang, JY; Kim, J; Hwang, GS (). „(1)H NMR-Based Metabolite Profiling of Planktonic and Biofilm Cells in Acinetobacter baumannii 1656-2”. PLoS ONE. 8 (3): e57730. Bibcode:2013PLoSO...857730Y. doi:10.1371/journal.pone.0057730. PMC 3590295
 . PMID 23483923.
. PMID 23483923.
- ^ a b McQueary, CN; Kirkup, BC; Si, Y; Barlow, M; Actis, LA; Craft, DW; Zurawski, DV (iunie 2012). „Extracellular stress and lipopolysaccharide modulate Acinetobacter baumannii surface-associated motility”. Journal of Microbiology. 50 (3): 434–43. doi:10.1007/s12275-012-1555-1. PMID 22752907.
- ^ Garrity, G., ed. (). „Pts. A & B: The Proteobacteria”. Bergey's Manual of Systematic Bacteriology. 2 (ed. 2nd ed., rev.). New York: Springer. p. 454. ISBN 978-0-387-95040-2.
- ^ O'Shea, MK (mai 2012). „Acinetobacter in modern warfare”. International Journal of Antimicrobial Agents. 39 (5): 363–75. doi:10.1016/j.ijantimicag.2012.01.018. PMID 22459899.
- ^ Gerner-Smidt, P (octombrie 1992). „Ribotyping of the Acinetobacter calcoaceticus-Acinetobacter baumannii complex”. Journal of Clinical Microbiology. 30 (10): 2680–5. PMC 270498
 . PMID 1383266.
. PMID 1383266.
- ^ Rice, LB (). „Federal funding for the study of antimicrobial resistance in nosocomial pathogens: no ESKAPE”. The Journal of Infectious Diseases. 197 (8): 1079–81. doi:10.1086/533452. PMID 18419525.
- ^ Drummond, Katie. „Pentagon to Troop-Killing Superbugs: Resistance Is Futile”. Wired.com. Condé Nast. Accesat în .
- ^ a b „What Is Acinetobacter Baumannii?”. Everyday Health. Accesat în .
- ^ Su, CH; Wang, JT; Hsiung, CA; Chien, LJ; et al. (). „Increase of carbapenem-resistant Acinetobacter baumannii infection in acute care hospitals in Taiwan: Association with hospital antimicrobial usage”. PLOS ONE. 7 (5): e37788. Bibcode:2012PLoSO...737788S. doi:10.1371/journal.pone.0037788. PMC 3357347
 . PMID 22629456.
. PMID 22629456.
- ^ Abbo, A; Navon-Venezia, S; Hammer-Muntz, O; Krichali, T; et al. (ianuarie 2005). „Multidrug-resistant Acinetobacter baumannii”. Emerging Infectious Diseases. 11 (1): 22–9. doi:10.3201/eid1101.040001. PMC 3294361
 . PMID 15705318.
. PMID 15705318.
- ^ Spapen, H; Jacobs, R; Van Gorp, V; Troubleyn, J; et al. (). „Renal and neurological side effects of colistin in critically ill patients”. Annals of Intensive Care. 1 (1): 14. doi:10.1186/2110-5820-1-14. PMC 3224475
 . PMID 21906345.
. PMID 21906345.
- ^ „Acinetobacter in Healthcare Settings”. CDC. Accesat în .
- ^ „He was dying. Antibiotics weren't working. Then doctors tried a forgotten treatment”. Mother Jones (în engleză). Accesat în .
- ^ „Acinetobacter in Healthcare Settings”. Centers for Disease Control and Prevention. US Department of Health and Human Services. Accesat în .
- ^ Jones, A; Morgan, D; Walsh, A; Turton, J; Livermore, D; Pitt, T; Green, A; Gill, M; Mortiboy, D (iunie 2006). „Importation of multidrug-resistant Acinetobacter spp infections with casualties from Iraq”. The Lancet Infectious Diseases. 6 (6): 317–8. doi:10.1016/S1473-3099(06)70471-6. PMID 16728314.
- ^ Dijkshoorn, L; Nemec, A; Seifert, H (decembrie 2007). „An increasing threat in hospitals: multidrug-resistant Acinetobacter baumannii”. Nature Reviews Microbiology. 5 (12): 939–51. doi:10.1038/nrmicro1789. PMID 18007677.
- ^ „Acinetobacter in Healthcare Settings - HAI - CDC”. www.cdc.gov. Accesat în .
- ^ Multirezistente Acinetobacter baumanni (MDRAB)." CINE Regiunea Pacificului de Vest, WPRO | CINE Regiunea Pacificului de Vest, 1 Nov. 2010, www.wpro.who.int/mediacentre/factsheets/fs_20101102/en/.
- ^ Koulenti, D; Lisboa, T; Brun-Buisson, C; Krueger, W; Macor, A; Sole-Violan, J; Diaz, E; Topeli, A; DeWaele, J (august 2009). EU-VAP/CAP Study, Group. „Spectrum of practice in the diagnosis of nosocomial pneumonia in patients requiring mechanical ventilation in European intensive care units”. Critical Care Medicine. 37 (8): 2360–8. doi:10.1097/ccm.0b013e3181a037ac. PMID 19531951.
- ^ Ng, J; Gosbell, IB; Kelly, JA; Boyle, MJ; Ferguson, JK (noiembrie 2006). „Cure of multiresistant Acinetobacter baumannii central nervous system infections with intraventricular or intrathecal colistin: case series and literature review”. The Journal of Antimicrobial Chemotherapy. 58 (5): 1078–81. doi:10.1093/jac/dkl347. PMID 16916866.
- ^ Farrugia, DN; Elbourne, LD; Hassan, KA; Eijkelkamp, BA; Tetu, SG; Brown, MH; Shah, BS; Peleg, AY; Mabbutt, BC (). „The Complete Genome and Phenome of a Community-Acquired Acinetobacter baumannii”. PLoS ONE. 8 (3): e58628. Bibcode:2013PLoSO...858628F. doi:10.1371/journal.pone.0058628. PMC 3602452
 . PMID 23527001.
. PMID 23527001. 
- ^ Werneck, JS; Picão, RC; Carvalhaes, CG; Cardoso, JP; Gales, AC (februarie 2011). „OXA-72-producing Acinetobacter baumannii in Brazil: a case report”. The Journal of Antimicrobial Chemotherapy. 66 (2): 452–4. doi:10.1093/jac/dkq462. PMID 21131320.
- ^ Martins, N; Martins, IS; de Freitas, WV; de Matos, JA; Magalhães, AC; Girão, VB; Dias, RC; de Souza, TC; Pellegrino, FL (iunie 2012). „Severe infection in a lung transplant recipient caused by donor-transmitted carbapenem-resistant Acinetobacter baumannii”. Transplant Infectious Disease. 14 (3): 316–20. doi:10.1111/j.1399-3062.2011.00701.x. PMC 3307813
 . PMID 22168176.
. PMID 22168176.
- ^ Superti, SV; Martins Dde, S; Caierão, J; Soares Fda, S; Prochnow, T; Zavascki, AP (). „Indications of carbapenem resistance evolution through heteroresistance as an intermediate stage in Acinetobacter baumannii after carbapenem administration”. Revista do Instituto de Medicina Tropical de Sao Paulo. 51 (2): 111–3. doi:10.1590/s0036-46652009000200010. PMID 19390741.
- ^ Gionco, B; Pelayo, JS; Venancio, EJ; Cayô, R; Gales, AC; Carrara-Marroni, FE (octombrie 2012). „Detection of OXA-231, a new variant of blaOXA-143, in Acinetobacter baumannii from Brazil: a case report”. The Journal of Antimicrobial Chemotherapy. 67 (10): 2531–2. doi:10.1093/jac/dks223. PMID 22736746.
- ^ Zhao, WS; Liu, GY; Mi, ZH; Zhang, F (martie 2011). „Coexistence of blaOXA-23 with armA and novel gyrA mutation in a pandrug-resistant Acinetobacter baumannii isolate from the blood of a patient with haematological disease in China”. The Journal of Hospital Infection. 77 (3): 278–9. doi:10.1016/j.jhin.2010.11.006. PMID 21281989.
- ^ Xiao, SC; Zhu, SH; Xia, ZF; Ma, B; Cheng, DS (noiembrie 2009). „Successful treatment of a critical burn patient with obstinate hyperglycemia and septic shock from pan-drug-resistant strains”. Medical Science Monitor. 15 (11): CS163–5. PMID 19865060.
- ^ Wu, YC; Hsieh, TC; Sun, SS; Wang, CH; Yen, KY; Lin, YY; Kao, CH (noiembrie 2009). „Unexpected cloud-like lesion on gallium-67 scintigraphy: detection of subcutaneous abscess underneath the skin with normal appearance in a comatose patient in an intensive care setting”. The American Journal of the Medical Sciences. 338 (5): 388. doi:10.1097/maj.0b013e3181a6dd36. PMID 19770790.
- ^ Duan, X; Yang, L; Xia, P (martie 2010). „Septic arthritis of the knee caused by antibiotic-resistant Acinetobacter baumannii in a gout patient: a rare case report”. Archives of Orthopaedic and Trauma Surgery. 130 (3): 381–4. doi:10.1007/s00402-009-0958-x. PMID 19707778.
- ^ a b Wagner, JA; Nenoff, P; Handrick, W; Renner, R; Simon, J; Treudler, R (februarie 2011). „Necrotizing fasciitis caused by Acinetobacter baumannii : A case report”. Der Hautarzt; Zeitschrift für Dermatologie, Venerologie, und Verwandte Gebiete (în German). 62 (2): 128–30. doi:10.1007/s00105-010-1962-3. PMID 20835812.
- ^ Aivazova, V; Kainer, F; Friese, K; Mylonas, I (ianuarie 2010). „Acinetobacter baumannii infection during pregnancy and puerperium”. Archives of Gynecology and Obstetrics. 281 (1): 171–4. doi:10.1007/s00404-009-1107-z. PMID 19462176.
- ^ Schulte, B; Goerke, C; Weyrich, P; Gröbner, S; Bahrs, C; Wolz, C; Autenrieth, IB; Borgmann, S (decembrie 2005). „Clonal spread of meropenem-resistant Acinetobacter baumannii strains in hospitals in the Mediterranean region and transmission to South-west Germany”. The Journal of Hospital Infection. 61 (4): 356–7. doi:10.1016/j.jhin.2005.05.009. PMID 16213625.
- ^ Piparsania, S; Rajput, N; Bhatambare, G (). „Intraventricular polymyxin B for the treatment of neonatal meningo-ventriculitis caused by multi-resistant Acinetobacter baumannii--case report and review of literature”. The Turkish Journal of Pediatrics. 54 (5): 548–54. PMID 23427525.
- ^ John, TM; Jacob, CN; Ittycheria, CC; George, AM; Jacob, AG; Subramaniyam, S; Puthiyaveettil, J; Jayaprakash, R (martie 2012). „Macrophage activation syndrome following Acinetobacter baumannii sepsis”. International Journal of Infectious Diseases. 16 (3): e223–4. doi:10.1016/j.ijid.2011.12.002. PMID 22285540.
- ^ Sharma, A; Shariff, M; Thukral, SS; Shah, A (octombrie 2005). „Chronic community-acquired Acinetobacter pneumonia that responded slowly to rifampicin in the anti-tuberculous regime”. The Journal of Infection. 51 (3): e149–52. doi:10.1016/j.jinf.2004.12.003. PMID 16230195.
- ^ Jeong, HL; Yeom, JS; Park, JS; Seo, JH; Park, ES; Lim, JY; Park, CH; Woo, HO; Youn, HS (). „Acinetobacter baumannii isolation in cerebrospinal fluid in a febrile neonate”. The Turkish Journal of Pediatrics. 53 (4): 445–7. PMID 21980849.
- ^ Hong, KB; Oh, HS; Song, JS; Lim, JH; Kang, DK; Son, IS; Park, JD; Kim, EC; Lee, HJ (iulie 2012). „Investigation and control of an outbreak of imipenem-resistant Acinetobacter baumannii Infection in a Pediatric Intensive Care Unit”. The Pediatric Infectious Disease Journal. 31 (7): 685–90. doi:10.1097/inf.0b013e318256f3e6. PMID 22466324.
- ^ Lee, YK; Kim, JK; Oh, SE; Lee, J; Noh, JW (decembrie 2009). „Successful antibiotic lock therapy in patients with refractory peritonitis”. Clinical Nephrology. 72 (6): 488–91. doi:10.5414/cnp72488. PMID 19954727.
- ^ Lee, SY; Lee, JW; Jeong, DC; Chung, SY; Chung, DS; Kang, JH (august 2008). „Multidrug-resistant Acinetobacter meningitis in a 3-year-old boy treated with i.v. colistin”. Pediatrics International. 50 (4): 584–5. doi:10.1111/j.1442-200x.2008.02677.x. PMID 18937759.
- ^ Adams, D; Yee, L; Rimmer, JA; Williams, R; Martin, H; Ovington, C (februarie 2011). „Investigation and management of an A. Baumannii outbreak in ICU”. British Journal of Nursing. 20 (3): 140, 142, 144–7. doi:10.12968/bjon.2011.20.3.140. PMID 21378633.
- ^ Pencavel, TD; Singh-Ranger, G; Crinnion, JN (mai 2006). „Conservative treatment of an early aortic graft infection due to Acinetobacter baumanii”. Annals of Vascular Surgery. 20 (3): 415–7. doi:10.1007/s10016-006-9030-2. PMID 16602028.
- ^ Gusten, WM; Hansen, EA; Cunha, BA (). „Acinetobacter baumannii pseudomeningitis”. Heart & Lung. 31 (1): 76–8. doi:10.1067/mhl.2002.120258. PMID 11805753.
- ^ Fitzpatrick, MA; Esterly, JS; Postelnick, MJ; Sutton, SH (). „Successful treatment of extensively drug-resistant Acinetobacter baumannii peritoneal dialysis peritonitis with intraperitoneal polymyxin B and ampicillin-sulbactam”. Annals of Pharmacotherapy. 46 (7–8): e17. doi:10.1345/aph.1r086. PMID 22811349.
- ^ Patel, JA; Pacheco, SM; Postelnick, M; Sutton, S (). „Prolonged triple therapy for persistent multidrug-resistant Acinetobacter baumannii ventriculitis”. American Journal of Health-System Pharmacy. 68 (16): 1527–31. doi:10.2146/ajhp100234. PMID 21817084.
- ^ Sullivan, DR; Shields, J; Netzer, G (iunie 2010). „Fatal case of multi-drug resistant Acinetobacter baumannii necrotizing fasciitis”. The American Surgeon. 76 (6): 651–3. PMID 20583528.
- ^ „Acinetobacter baumannii: Role in Blood Stream Infection in Neonatal Unit, Cipto Mangunkusumo Hospital, Jakarta, Indonesia”. International Journal of Microbiology. 2013: 180763. . doi:10.1155/2013/180763. PMC 3830835
 . PMID 24288538.
. PMID 24288538.
