Reacție haloformă
Reacția haloformă este o reacție organică în care un haloform (compus de forma CHX3, unde X este un halogen; avem ca exemplu cloroform, iodoform, etc) este obținut ca urmare a unei halogenări exhaustive a unei metil-cetone (un compus de forma R–CO–CH3) în prezența unei baze.[1][2][3] Reacția poate fi folosită pentru transformarea grupelor acetil în grupe carbonil sau pentru obținerea cloroformului (CHCl3), bromoformului (CHBr3) sau iodoformului (CHI3).
Mecanism[modificare | modificare sursă]
În prima etapă, are loc disproporționarea halogenului în prezența hidroxidului, obținându-se ionul halogenură corespunzător și ionul hipohalit (mai jos se regăsește ecuația exemplificată pe brom, când rezultă ionii bromură și hipobromit):
Dacă este prezent un alcool secundar, acesta va fi oxidat la cetonă de către hipobromit:

Dacă avem în schimb o metilcetonă, aceasta va intra în reacție cu ionul hipohalit, urmând un proces în trei etape:
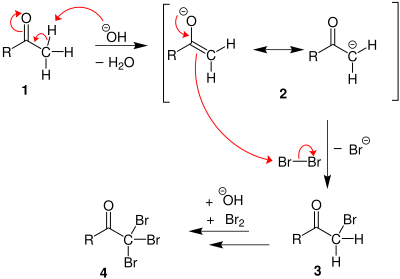
1. În mediul bazic, cetona suferă tautomerie ceto-enolică. Ionul enolat va ataca nucleofil o moleculă de brom.
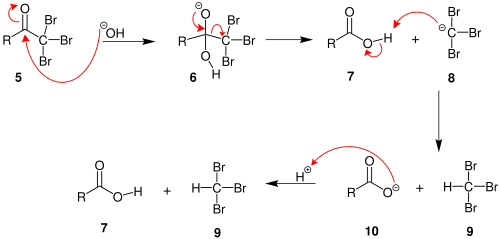
2. În momentul în care poziția alfa a fost complet substituită cu halogen (halogenare exhaustivă), va avea loc un atac nucleofil al hidroxidului, −CX3 eliminându-se și stabilizându-se ulterior (datorită grupelor atrăgătoare de electroni).
3. Anionul −CX3 primește un proton de la solvent sau de la acidul carboxilic format în etapa precedentă, formând haloformul.
Aplicații[modificare | modificare sursă]

În laborator, reacția haloformă este utilizată câteodată pentru identificarea unei metilcetone. De obicei, se utilizează reacția de obținere a iodoformului, când apare un precipitat alb.
Referințe[modificare | modificare sursă]
- ^ March, Jerry; Smith, Michael B. (). Knipe, A.C., ed. March's Advanced Organic Chemistry Reactions, Mechanisms, and Structure (ed. 6th). Hoboken: John Wiley & Sons. p. 484. ISBN 9780470084946.
- ^ Reynold C. Fuson and Benton A. Bull (). „The Haloform Reaction”. Chemical Reviews. 15 (3): 275–309. doi:10.1021/cr60052a001.
- ^ Chakrabartty, in Trahanovsky, Oxidation in Organic Chemistry, pp 343–370, Academic Press, New York, 1978