Legea lui Hess
Legea lui Hess este un principiu folosit în chimie fizică (mai exact în termochimie) care spune că variația totală de entalpie pentru o anumită reacție chimică este aceeași, indiferent dacă aceasta are loc într-o etapă sau mai multe etape.[1][2] A fost denumită după chimistul și fizicianul Germain Hess, care a publicat legea în 1840.
Definire[modificare | modificare sursă]
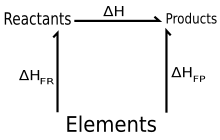
Legea lui Hess spune că variația de entalpie (ΔH) într-o reacție chimică este independentă de modul în care decurge acea reacție (adică independentă de faza inițială și finală). Altfel spus, dacă o reacție poate să aibă loc pe mai multe căi, variația de entalpia totală va fi aceeași.[3] ΔH = nr de molixΔHprodus-nr de molixΔH reactant entalpie de formare standard, iar o indică valori pentru starea standard. Aceasta poate fi considerată ca fiind suma dintre două reacții (reale sau imaginare/ipotetice):
- Reactanți → Elemente componente
- și Elemente → Produși
Utilizare[modificare | modificare sursă]
Cu ajutorul legii lui Hess se poate calcula variația de entalpie pentru o reacție, atunci când nu este posibilă măsurarea directă. La rezultat se ajunge rezolvând o serie de operații algebrice bazate pe ecuațiile chimice ale reacțiilor, doar în cazul în care sunt cunoscute entalpiile de formare pentru fiecare în parte.
Prin adunarea ecuațiilor chimice se obține o ecuație totală, netă. Dacă variația de entalpie se cunoaște pentru fiecare ecuație, atunci rezultatul va fi variația de entalpie pentru ecuația netă obținută:
- Dacă variația e negativă (ΔHnetă < 0), atunci reacția este o reacție exotermă (și cel mai probabil spontană)
- Dacă variația e pozitivă (ΔHnetă > 0), atunci reacția este o reacție endotermă
Pentru determinarea spontaneității unei reacții se poate calcula și entropia.
Vezi și[modificare | modificare sursă]
Referințe[modificare | modificare sursă]
- ^ Mannam Krishnamurthy; Subba Rao Naidu (). „7”. În Lokeswara Gupta. Chemistry for ISEET - Volume 1, Part A (ed. 2012). Hyderabad, India: Varsity Education Management Limited. p. 244.
- ^ „Hess's Law - Conservation of Energy”. University of Waterloo. Arhivat din original la . Accesat în .
- ^ „Legea lui Hess”, scribd, accesat în
Bibliografie[modificare | modificare sursă]
- V. Kirillin, V. Sîcev, A. Șeindlin, Termodinamica, Editura Științifică și Enciclopedică, București, 1985, (traducere din limba rusă), p. 499-504


