Borohidrură de sodiu
| Borohidrură de sodiu | |
 | |
 | |
| Nume IUPAC | Tetrahidroborat de sodiu |
|---|---|
| Identificare | |
| Număr CAS | 16940-66-2 |
| PubChem CID | 4311764 |
| Informații generale | |
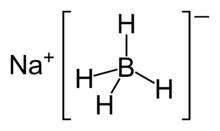
| Formulă chimică | NaBH4 |
| Aspect | cristale albe, higroscopice |
| Masă molară | 37,83 g/mol |
| Proprietăți | |
| Densitate | 1,0740 g/cm3 |
| Punct de topire | 400 °C |
| Punct de fierbere | 500 °C |
| Solubilitate | amoniac, amine, piridine |
| Solubilitate în apă | |
| reacționează | |
| Structură cristalină | cristale cubice |
| Temperatură de aprindere | 70 °C |
| Doza letală medie | 160 mg/kg (oral - șobolan) 230 mg/kg (dermic - iepure) |
| Pericol | |
| Fraze R | R15, R24/25, R35 |
| Fraze S | S7/8, S26, S36, S43, S45 |
H260, H301, H311, H314, P223, P231, P232, P280, P301, P310, P370, P378, P422, | |
| NFPA 704 | |
| Sunt folosite unitățile SI și condițiile de temperatură și presiune normale dacă nu s-a specificat altfel. | |
| Modifică date / text | |
Borohidrura de sodiu, denumită și tetrahidroborat de sodiu [1] este un compus anorganic cu formula chimică NaBH4. Este un solid alb, de obicei întâlnit sub formă de pudră, și este un reactiv de o importanță ridicată fiind un puternic agent reducător. Are aplicații atât în laborator, cât și la scară industrială. Compusul este solubil în alcooli și în unii eteri, dar reacționează cu apa în absența mediului bazic. [2] A fost descoperit în anii 1940 de Hermann Irving Schlesinger.
Proprietăți chimice[modificare | modificare sursă]
Reactivitate[modificare | modificare sursă]
NaBH4 poate reduce foarte mulți compuși carbonilici, dar depinde de condițiile de reacție. În majoritate, este folosit în laborator pentru reducerea aldehidelor și cetonelor la alcoolii corespunzători. De asemenea poate reduce și cloruri de acil, esteri tiolici și imine. În condiții obișnuite nu poate reduce esteri, amide și nici acizi carboxilici. [2]
Reactivitatea compusului NaBH4 poate fi mărită cu ajutorul unor compuși. [3][4] Oxidarea cu iod în tetrahidrofuran are ca rezultat formarea unui complex de tetrahidrofuran și bor, care poate reduce acizii carboxilici. [5]
Formarea de compuși complecși[modificare | modificare sursă]
BH4− poate fi ligand pentru ioni metalici. Astfel de complecși de borohidruri pot fi preparați prin reacția dintre NaBH4 și o halogenură a metalului corespunzător. Un exemplu este următorul compus organo-titanic: [6]
- 2 (C5H5)2TiCl2 + 4 NaBH4 → 2 (C5H5)2TiBH4 + 4 NaCl + B2H6 + H2
Sursă de hidrogen[modificare | modificare sursă]
În prezența catalizatorilor metalici, borohidrura de sodiu reacționează cu formare de hidrogen:
- NaBH4 + 2 H2O → NaBO2 + 4 H2 (ΔH < 0)
Vezi și[modificare | modificare sursă]
Referințe[modificare | modificare sursă]
- ^ Busch, D.H. (). Inorganic Syntheses. 20. Wiley. p. 137. ISBN 9780470132869. Accesat în .
- ^ a b Banfi, L.; Narisano, E.; Riva, R.; Stiasni, N.; Hiersemann, M. "Sodium Borohydride" in Encyclopedia of Reagents for Organic Synthesis (Ed: L. Paquette) 2004, J. Wiley & Sons, New York. doi:10.1002/047084289X.rs052.
- ^ Periasamy, Mariappan; Thirumalaikumar, Muniappan (). „Methods of enhancement of reactivity and selectivity of sodium borohydride for applications in organic synthesis”. Journal of Organometallic Chemistry. 609 (1–2): 137–151. doi:10.1016/S0022-328X(00)00210-2.
- ^ Nora de Souza, Marcus Vinícius; Alves Vasconcelos; Thatyana Rocha (). „Recent methodologies mediated by sodium borohydride in the reduction of different classes of compounds”. Applied Organometallic Chemistry. 20 (11): 798–810. doi:10.1002/aoc.1137.
- ^ Kanth, J. V. Bhaskar; Periasamy, Mariappan (). „Selective reduction of carboxylic acids into alcohols using sodium borohydride and iodine”. The Journal of Organic Chemistry. 56 (20): 5964–5965. doi:10.1021/jo00020a052.
- ^ Lucas, C. R. (). „Bis(5-Cyclopentadienyl) [Tetrahydroborato(1-)]Titanium”. Inorganic Syntheses. 17: 93. doi:10.1002/9780470132487.ch27.

