Pilă de combustie

O pilă de combustie este o celulă electrochimică care convertește energia chimică a unui combustibil (adesea hidrogen) și un agent oxidant (adesea oxigen[1]) în electricitate printr-o pereche de reacții redox.[2]
Pilele de combustie sunt diferite de baterii prin necesitatea unei surse continue de combustibil și oxigen (de obicei luat din aer) pentru a susține reacția chimică, în timp ce într-o baterie energia chimică provine de obicei din metale și ionii lor sau oxizi[3] care de obicei sunt prezente deja în baterie. Pilele de combustie pot produce electricitate continuu cât timp sunt alimentate cu combustibil și oxigen.
Primele pile de combustie au fost inventate de William Robert Grove în 1838. Prima utilizare comercială a pilelor de combustie a avut loc după invenția pilei de combustie alcalină hidrogen-oxigen de către Francis Thomas Bacon în 1932. Astfel de pile au fost utilizate de NASA în programele sale spațiale de la mijlocul anilor 1960 pentru a genera energie pentru sateliți și capsule spațiale. De atunci pilele de combustie au fost utilizate în multe alte aplicații. Pilele de combustie sunt utilizate pentru obținerea energiei necesare sau de rezervă pentru clădiri comerciale, industriale și rezidențiale sau în zone îndepărtate sau inaccesibile. Ele sunt, de asemenea, utilizate pentru alimentarea vehiculelor cu pile de combustie, inclusiv motostivuitoare, automobile, autobuze, bărci, motociclete și submarine.
Există multe tipuri de pile de combustie, dar toate constau dintr-un anod, un catod și un electrolit care permite ionilor, adesea ionilor de hidroniu încărcați pozitiv (protoni), să se deplaseze între cei doi electrozi ai pilei. La anod, un catalizator determină combustibilul să fie oxidat, generând ioni (adesea ioni de hidrogen încărcați pozitiv) și electroni. Ionii se deplasează de la anod la catod prin electrolit. În același timp, electronii parcurg un circuit extern de la anod la catod sub forma unui curent continuu. La catod, un alt catalizator face ca ionii, electronii și oxigenul să reacționeze, formând apă și posibil alte produse. Pilele de combustibil sunt clasificate în funcție de tipul de electrolit pe care îl folosesc și de diferența de timp de pornire variind de la 1 secundă pentru pilele de combustie cu membrană schimbătoare de protoni, până la 10 minute pentru pilele de combustie cu oxizi solizi. O celulă produce potențiale electrice relativ mici, de aproximativ 0,7 V. Pentru tensiuni mai mari, celulele sunt legate în serie. În plus față de electricitate, pilele de combustie produc apă, căldură și, în funcție de sursa de combustibil, cantități mici de dioxid de azot și alte emisii. Eficiența energetică a unei pile de combustie este în general între 40 și 60 %. Dacă și căldura este captată și utilizată într-o schemă de cogenerare, se pot obține randamente energetice de până la 85%.[4]
Avantajele utilizării sistemelor energetice pe bază de pile de combustie sunt:
- produc curent electric continuu la tensiuni scăzute, dar intensități medii;
- nu produc poluarea mediului ambiant;
- funcționează fără vibrații sau zgomote, neavând elemente în mișcare.
Istoric[modificare | modificare sursă]
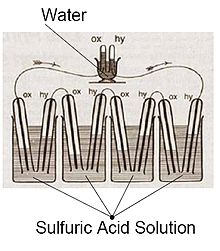
Primele materiale despre pilele de combustie cu hidrogen au apărut în 1838. Într-o scrisoare datată octombrie 1838, dar publicată în ediția din decembrie 1838 a „The London and Edinburgh Philosophical Magazine and Journal of Science”, fizicianul și avocatul galez William Grove a scris despre primele sale pile de combustie. El a folosit o combinație de tablă de fier, cupru și plăci de porțelan și o soluție de sulfat de cupru și acid diluat.[5][6] Într-o scrisoare către aceeași publicație scrisă în decembrie 1838, dar publicată în iunie 1839, fizicianul german Christian Friedrich Schönbein a descris prima pilă de combustibil pe care a inventat-o el. Scrisoarea sa descria curentul generat din hidrogen și oxigen dizolvat în apă.[7] În 1842 Grove a publicat în aceeași revistă schița proiectul său. Pila sa de combustie folosea materiale similare cu cele folosite astăzi la pilele de combustie cu acid fosforic.[8][9] În 1932 Francis Thomas Bacon a realizat o pilă de combustie alcalină staționară de 5 kW, tip de pilă folosit de NASA la mijlocul anilor 1960.[10][11]
În 1955 W. Thomas Grubb, chimist care lucra pentru General Electric (GE), a modificat concepția inițială a pilei de combustie utilizând o membrană de schimb ionic din polistiren sulfonat ca electrolit. Trei ani mai târziu, un alt chimist de la GE, Leonard Niedrach, a conceput o modalitate de depunere a platinei pe membrană, care a servit drept catalizator pentru reacțiile de oxidare a hidrogenului și de reducere a oxigenului. Aceasta a devenit cunoscută sub numele de „pila de combustie Grubb–Niedrach”.[12][13] GE a continuat să dezvolte această tehnologie cu NASA și McDonnell Aircraft, ceea ce a dus la utilizarea ei în timpul Programului Gemini. Aceasta a fost prima utilizare comercială a unei pile de combustie. În 1959 o echipă condusă de Harry Ihrig a construit un tractor cu pile de combustie de 15 kW pentru Allis-Chalmers, care a fost prezentat în SUA la târgurile statale. Acest sistem a folosit hidroxid de potasiu ca electrolit și hidrogen comprimat și oxigen drept reactanți. Mai târziu, în 1959, Bacon și colegii săi au prezentat o unitate de cinci kilowați capabilă să alimenteze o mașină de sudat. În anii 1960, Pratt & Whitney a autorizat folosirea brevetelor americane Bacon în programul spațial american pentru a furniza electricitate și apă potabilă (hidrogenul și oxigenul fiind disponibile din rezervoarele navelor spațiale). În 1991, primul automobil cu pilă de combustie cu hidrogen a fost dezvoltat de Roger Billings.[14][15]
UTC Power a fost prima companie care a produs și comercializat un sistem de pile de combustie staționar, suficient de mare pentru a fi utilizat drept centrală electrică în cogenerare pentru spitale, universități și clădiri mari de birouri.[16]
Aspecte teoretice[modificare | modificare sursă]
Tensiuni și randament[modificare | modificare sursă]
Procesele electrochimice care au loc într-o pilă de combustie constau într-o serie de reacții redox (de reducere/oxidare). În pilă, combustibilul A, de exemplu hidrogenul, este absorbit pe suprafața anodului poros, unde este disociat în ioni și electroni într-un proces de oxidare. Ionii de combustibil migrează prin electrolit de la anod la catod, unde se întâlnesc cu electronii (veniți prin circuitul electric exterior) și oxidantul B. Are loc reacția de reducere, rezultând un produs de reacție (apă, dacă combustibilul este hidrogenul).
În timpul funcționării, electrozii și electrolitul nu suferă nicio modificare structurală, ei servind doar ca suport pentru reacție. La anod are loc oxidarea catalitică a hidrogenului atomic, iar la catod reducerea catalitică a oxigenului atomic. Fenomenul de oxidare și reducere catalitică are loc în regim trifazic (gaz—lichid—solid) la suprafața catalizatorului.
Teoretic, cantitatea de energie electrică produsă de o pilă de combustie este diferența dintre energiile libere Gibbs ale reactanților și produselor reacției:[17]
unde și sunt variația entalpiei, respectiv a entropiei în timpul reacției la temperatura T. Pentru hidrogen kJ/mol iar kJ/mol.
Într-un proces reversibil este convertită complet în curent electric:[18]
unde n este numărul de electroni transferați, F este constanta lui Faraday (96485 C/mol), iar Vr este tensiunea celulei în circuit deschis (reversibilă), care depinde de temperatură. În condiții standard tensiunea reversibilă a celulei este:[18]
- .
Randamentul ideal al unei pile de combustie este:[18]
- .
Randamentul este de 100 % dacă , ceea ce se întâmplă dacă numărul de moli de gaz nu se schimbă, de exemplu în reacția . Dacă în reacție nu intervine doar energia , ci și o cantitate de căldură , care va fi degajată în mediul ambiant.
Tensiunea unei pile de combustie depinde de activitatea reactanților, care, la rândul ei, este în funcție de presiunile lor, p:[19]
unde R este constanta universală a gazelor (R = 8,3145 J/mol K), iar este numărul de moli din reactantul .


În realitate tensiunile sunt ceva mai mici decât cele calculate termodinamic mai sus. Din cauza rezistenței ohmice a electrozilor și electrolitului apare o cădere de tensiune proporțională cu intensitatea curentului i:[20]
- .
Altă cădere de tensiune apare datorită necesității de a învinge barierele de activare, cădere care este liniară în funcție de logaritmul intensități:[21]
unde este o constantă de proces, iar este curentul la echilibru.
Când curentul circulă, cationii formați la anod se deplasează spre catod, ca urmare concentrația acestor ioni variază. Apar căderi de tensiune în dreptul fiecărui electrod, și , a căror sumă este:[21]
unde este intensitatea limită.
Similar, dacă în fluxul de reactanți apar variații de concentrații (de exemplu prin epuizarea reactanților în zona catalizatorilor la sarcini mari[9]), care se pot exprima prin presiuni, apare căderea de tensiune:[22]
Se poate defini randamentul pilei ca raport între tensiunea furnizată V și tensinea reversibilă în condiții standard:[22]
Curba căderilor de tensiune și a randamentului sunut prezentate în figurile alăturate.
Consumul de combustibil și oxidant[modificare | modificare sursă]
Consumul este proporțional cu curentul produs de pilă. Reacția dintre combustibilul A și oxidantul B, rezultând produsele C și D este:[23]
Debitul masic de combustibil pentru curentul i este:[23]
- [kg/s]
unde MA este masa molară a combustibilului, în [g/mol].
Raportul stoechiometric dintre oxidant și combustibil este:[23]
- .
Pentru o pilă cu hidrogen, raportul stoechiometric este:[24]
Coeficientul de excedent de aer este definit drept raportul dintre cantitatea reală de oxidant care intră în reacție și cantitatea stoechiometrică:[24]
Dacă amestecul este bogat, la amestecul este stoechiometric, iar la amestecul este sărac. Întotdeauna pilele de combustie lucrează cu amestec sărac () pentru a reduce căderile de tensiune din cauza oxidantului.
În pilele de combustie drept oxidant se folosește aerul atmosferic, la care fracția masică a oxigenului este de 0,232. Pentru reactanții hidrogen/aer raportul stoechiometric devine:[24]
- .
Construcție și tipuri[modificare | modificare sursă]
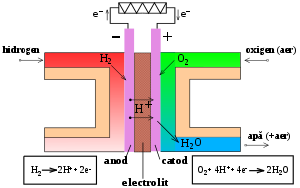
Există mai multe tipuri de pile de combustie, dar toate funcționează pe același principiu. Ele sunt alcătuite din trei componente adiacente: anodul, electrolitul și catodul. Două reacții chimice apar la interfețele dintre cele trei componente. Rezultatul net al celor două reacții este că se consumă combustibil, se creează apă sau/și dioxid de carbon și se generează curent electric care poate fi utilizat pentru alimentarea dispozitivelor electrice, care formează din punct de vedere electric sarcina.
La anod un catalizator oxidează combustibilul, de obicei hidrogen, transformând molecula de combustibil într-un ion încărcat pozitiv și un electron încărcat negativ. Electrolitul este o substanță specială prin care ionii pot trece, dar electronii nu. Electronii eliberați sunt culeși și vor ajunge la catod sub formă de curent electric prin circuitul extern. Ionii se deplasează la catod prin electrolit. La catod ionii se reunesc cu electronii și cei doi reacționează cu o a treia substanță chimică, de obicei oxigen, pentru a crea apă sau dioxid de carbon.
Elementele caracteristice unui anumit tip de pilă de combustie sunt:
- Electrolitul, care definește de obicei tipul pilei de combustie, și poate fi de exemplu hidroxid de potasiu, săruri (carbonați) și acidul fosforic.[25]
- Combustibilul folosit. Combustibilul obișnuit este hidrogenul.
- Catalizatorul anodic, de obicei pulbere fină de platină. Acesta descompune combustibilul în electroni și ioni.
- Catalizatorul catodic, de multe ori nichel. Acesta transformă ionii în produsele finale ale reacțiilor chimice, cel mai adesea apă.[26]
- Straturi de difuzie a gazelor, concepute pentru a rezista la oxidare.[26]
Pentru a funcționa, o pilă de combustibil are nevoie și de următoarele echipamente auxiliare:[27]
- compresorul de aer (ridică presiunea aerului la 2–5 bar),
- pompa de circulație a lichidului de răcire,
- ventilatorul sistemului de răcire,
- pompa de circulație a combustibilului,
- echipamentul electronic de coordonare și comandă.
Aceste echipamente consumă o parte din energia electrică produsă de pilă. Cel mai mare consumator este compresorul, al cărui consum este de circa 10 % din curentul produs de pilă. Celelalte echipamente consumă mult mai puțin — la proiectare, în primă aproximație, consumul lor poate fi neglijat.
O celulă tipică dintr-o pilă de combustibil produce o tensiune de 0,6–0,7 V la sarcină maximă. Pentru a furniza tensiunea și intensitatea de curent dorită celulele pot fi legate în serie pentru a se obține tensiunea necesară și în paralel pentru a se obține intensitatea de curent necesară. De asemenea, pentru a obține o intensitate mai mare se pot folosi pile cu suprafață de reacție a celulelor mai mare.
După modul de utilizare a combustibilului clasificarea pile de combustie este:[27]
- pile de combustie cu alimentare directă, alimentate cu combustibil din rezervor,
- pile de combustie cu alimentare indirectă, prevăzute suplimentar cu sistem de reformare catalitică, fiind alimentate cu metanol, etanol, gaz metan, benzină, hidrazină, amoniac etc., din care rezultă prin reformare hidrogenul.
După temperatura de funcționare există:[27]
- pile de combustie de temperaturi joase (< 200 °C),
- pile de combustie de temperaturi medii (200–600 °C),
- pile de combustie de temperaturi înalte (> 600 °C).
După electrolit și combustibil, cele mai cunoscute sunt:[27]
- pile de combustie cu membrană schimbătoare de protoni (engleză proton exchange membrane fuel cell — PEMFC),
- pile de combustie cu acid fosforic (engleză phosphoric acid fuel cell — PAFC),
- pile de combustie alcaline (engleză alkaline fuel cell — AFC),
- pile de combustie cu carbonat topit (engleză molten carbonate fuel cell — MCFC),
- pile de combustie cu oxizi solizi (engleză solid oxide fuel cell — SOFC),
- pile de combustie cu alimentare directă cu metanol (engleză direct methanol fuel cell — DMFC),
- pile de combustie cu alimentare indirectă cu metanol (engleză indirect methanol fuel cell — IMFC, engleză reformed methanol fuel cell — RMFC),
- pile de combustie cu alimentare directă cu etanol (engleză direct ethanol fuel cell — DEFC).
Pile de combustie cu membrană schimbătoare de protoni (PEMFC)[modificare | modificare sursă]

Pilele de combustie cu membrană schimbătoare de protoni (PEMFC, PEM) sunt formate dintr-un ansamblu de electrozi–membrană (MEA) care includ electrozii, electrolitul, catalizatorii și straturile de difuziune a gazelor.
Catalizatorii, carbonul și electrozii sunt conținuți într-o vopsea aplicată pe electrolitul solid, iar apoi pe ambele părți este presată la cald o hârtie cu carbon pentru a proteja interiorul celulei, îndeplinind și funcția de electrozi. Partea esențială a celulei sunt zonele de contact unde apare câte un strat triplu (TPB) în care electrolitul, catalizatorul și reactanții se amestecă și au loc efectiv reacțiile electrochimice.[28] Un aspect foarte important este că membrana nu trebuie să conducă curentul electric, astfel încât reacțiile de la catod și anod nu se amestecă.
Electrolitul este un copolimer solid din acid perfluorosulfonic (C9HF17O5S — PFSA, Nafion®) și politetrafluoroetilenă ( (C2F4)n — PTFE, Teflon®).[29] Denumirea copolimerului este tot Nafion, cele mai folosite fiind Nafion 112, 115 și 117. Catalizatorii sunt în special platina.
Aceste pile funcționează la temperaturi/presiuni relativ mici, (50–100 °C / 2–5 bar). Randamentul energetic maxim teoretic rezultă din energia liberă Gibbs kJ/mol și căldura de ardere a hidrogenului kJ/mol și este de 83 % la 298 K.[30]
Datorită căderilor interioare de tensiune randamentul practic al acestor pile este de c. 50–60 %.[31] Faptul că lucrează la temperaturi relativ mici — deci pornesc repede — și puterile convenabile le recomandă pentru a fi folosite la acționarea autovehiculelor.[32]
Pile de combustie cu acid fosforic (PAFC)[modificare | modificare sursă]
Pilele de combustie cu acid fosforic (PAFC) sunt similare cu pilele de combustie cu membrană schimbătoare de protoni. Au aceeași schemă de principiu și aceleași reacții chimice la anod și la catod. Electrolitul este format din acid fosforic (H3PO4) cu înaltă concentrație, într-un suport de carbură de siliciu (SiC, carborund), iar catalizatorul este tot platina.[33] Acidul creează probleme datorită coroziunii. Lucrează la temperaturi mai mari, de 160–220 °C.[33][34] Randamentul lor electric este în jur de 40 %, ceea ce le recomandă pentru instalații staționare cu producerea combinată a energiei electrice și căldurii (cogenerare), caz în care randamentul energetic poate ajunge la 80 %.[34] Electrolitul se solidifică sub 42 °C, astfel că ele trebuie încălzite înainte de pornire. Nu sunt potrivite pentru autovehicule.[33]
Pile de combustie alcaline (AFC)[modificare | modificare sursă]

Pilele de combustie alcaline consumă hidrogen și oxigen pur într-o reacție redox ca și pilele precedente. Contrar pilelor de combustie acide, apa se formează la anod.[35]
Cei doi electrozi sunt separați de un strat ceramic poros saturat cu o soluție apoasă alcalină, cum ar fi hidroxidul de potasiu (KOH), care formează electrolitul. Ionii care-l traversează sunt de hidroxil (OH–). Principala problemă a acestor pile este sensibilitatea electrolitului la acțiunea dioxidului de carbon, cu care formează carbonat de potasiu, care otrăvește pila. Din această cauză, pilele de combustie alcaline funcționează de obicei cu oxigen pur (cum este cazul la aplicațiile spațiale), sau cel puțin cu aer și combustibil (de exemplu hidrogen obținut prin reformarea alcoolilor) purificat, ceea ce necesită prezența în instalație a scruberelor care să curețe cât mai mult posibil dioxidul de carbon.[36][37] Datorită acestui efect de otrăvire, există două variante principale de AFC: cu electrolit static și cu electrolit care curge. Pentru maximizarea performanțelor aceste pile folosesc catalizatori de platină, însă se pot folosi și catalizatori mai ieftini ca argintul și nichelul.[38]
Pilele de combustie alcaline pot lucra în domenii largi de presiune și temperatură, de 2,2–45 bar și 80–220 °C. Au un randament mare, de c. 60 %.[39][40] În anii 1960 NASA a folosit acet tip de pile în Programul Apollo și pentru naveta spațială. Deși acest tip de pile de combustie a fost folosit pe larg în tehnica spațială,[36] datorită necesității de a folosi hidrogen și oxigen pur folosirea lor la autovehicule este sporadică.
Pile de combustie cu carbonat topit (MCFC)[modificare | modificare sursă]

Pilele de combustie cu carbonat topit (MCFC) lucrează la[temperatură înaltă, de 600 °C sau mai mult. Principalul lor avantaj este că pot fi alimentate direct cu diferiți combustibili care conțin carbon, ca gazul natural, biogazul și chiar praful de cărbune, deoarece folosesc un electrolit format din săruri topite (carbonați), plasate într-un suport ceramic inert din punct de vedere chimic, care nu sunt afectate de prezența dioxidului de carbon. Ionii pozitivi care trec prin electrolit sunt ionii de carbonat (CO32–), pentru formarea cărora este necesară la catod o sursă de CO2, care însă poate fi CO2 recirculat de la anod.[41] Temperatura necesară topirii sărurilor este de peste 600 °C. La această temperatură, dacă combustibilul este o hidrocarbură, extragerea hidrogenului necesar producției de curent se face printr-un proces de reformare direct în pilă, astfel că nu mai este nevoie de o unitate de reformare externă, pila făcînd parte din categoria pilelor cu alimentare directă cu hidrocarburi. Tot datorită temperaturilor înalte, la anod și catod se pot folosi catalizatori relativ ieftini, cum ar fi nichelul.[42][43]
Randamentul lor pe partea electrică este bun, de c. 50–60 %, iar dacă se folosește și căldura produsă, randamentul energetic poate atinge 85 %.[39][36] Puterile relativ mari, până la 3 MW, le fac potrivite pentru furnizarea de energie electrică și termică în cogenerare pentru obiective staționare, cum ar fi unități industriale, spitale, obiective izolate sau militare.[44][45] Deși teoretic pot fi alimentate cu benzină,[41][46] deoarece trebuie încălzite în prealabil pentru topirea electrolitului, durabilitatea lor este redusă, pornirea este lentă și răspund lent la variații de sarcină, motive pentru care nu sunt potrivite pentru autovehicule.[41]
Pile de combustiel cu oxizi solizi (SOFC)[modificare | modificare sursă]

Pilele de combustie cu oxizi solizi sunt caracterizate prin electrolitul lor format din oxizi în stare solidă care conduc ionii negativi de oxigen de la catod la anod similar cu modul de conducție al sarcinilor pozitive în materialele semiconductoare. Oxidarea electrochimică a hidrogenului, monoxidului de carbon sau a altor intermediari organici de către ionii de oxigen apare astfel pe partea anodului. Acestea funcționează la temperaturi foarte ridicate, de obicei 500–1000 °C.[41] La aceste temperaturi, SOFC nu necesită catalizatori scump, de exemplu platină, așa cum este necesar în prezent la pilele de combustie care funcționează la temperaturi reduse, cum ar fi pilele pilele cu membrană schimbătoare de protoni, și nu sunt vulnerabile la otrăvirea catalizatorului cu monoxid de carbon.[47] Însă aceste pile sunt vulnerabile la otrăvirea cu sulf, care trebuie îndepărtat, uzual prin utilizarea materialelor adsorbante, sau a altor mijloace.[48][49] Există și pile (PC-SOFC) ai căror electroliți conduc protoni în loc de ioni de oxigen, având avantajul că pot funcționa la temperaturi mai scăzute decât pilele cu oxizi solizi tradiționale.[41]

Spre deosebire de majoritatea celorlalte tipuri de pile de combustie, SOFC-urile pot avea două geometrii diferite. Geometria tipică a pilelor de combustie este cea planară, de tip sandwich, unde electrolitul este intercalat între electrozi. Cealaltă variantă este geometria tubulară unde aerul sau combustibilul sunt trecute prin interiorul tubului și celălalt gaz este trecut prin exteriorului tuburilor. Designul tubular este avantajos, deoarece etanșarea între gaze este mult mai ușor de realizat. Totuși, performanța pilelor cu electrolit plan este în prezent mai bună decât performanța pilelor cu electrolit tubular deoarece construcția plană are o rezistență hidrodinamică la curgerea gazelor mai mică.[47]
Avantajele acestor pile sunt că pot fi alimentate direct cu diferiți combustibili, inclusiv metanul, propanul și butanul, pot fi reformate intern la anod. SOFC-urile pot fi alimentate și cu hidrocarburi mai grele, reformate în exterior, cum ar fi benzina, motorina, petrolul pentru aviație (JP-8) sau diverși biocombustibili. Produsele reacțiilor de reformare sunt amestecuri de hidrogen, monoxid de carbon, dioxid de carbon, abur și metan, formate prin reacția combustibililor care conțin hidrocarburi cu aerul sau cu aburul într-un dispozitiv din amonte de anodul SOFC. Sistemele de alimentare SOFC pot crește eficiența utilizând căldura degajată de oxidarea electrochimică exotermă din pila de combustibil pentru procesul endoterm de reformare cu abur. În plus, combustibilii solizi, cum ar fi cărbunele și biomasa pot fi gazeificate pentru a forma gaz de cracare, care este bun la alimentarea SOFC.
Randamentul lor pe partea electrică este bun, de c. 60 %, iar dacă se folosește și căldura produsă, randamentul energetic poate atinge 85 %. Sunt folosite ca surse de curent electric și căldură în industrie și în domeniul militar.[39][44] Principalul dezavantaj este temperatura de funcționare ridicată, ceea ce duce la timpi mari de pornire și, datorită faptului că nu suportă șocurile termice, necesită un proces de încălzire uniform și bine reglat. Pachetele de electrolit ale SOFC cu geometrie plană necesită un timp de încălzire la temperatura de funcționare de ordinul unei ore. Geometriile cu electrolitul sub formă de microtuburi se încălzesc mult mai repede, pilele având timpi de pornire de ordinul minutelor.[50][51]
Pilele de combustie cu oxid solid sunt utilizate ca unități de alimentare auxiliare cu puteri de la 1 kW la 2 MW. Randamentul lor pe partea electrică este de c. 60 %, iar dacă se folosește și căldura produsă în cogenerare, randamentul energetic poate atinge 85 %.[36][39][44][52]
Vezi și[modificare | modificare sursă]
Note[modificare | modificare sursă]
- ^ en Saikia, Kaustav; Kakati, Biraj Kumar; Boro, Bibha; Verma, Anil (). „Current Advances and Applications of Fuel Cell Technologies”. Recent Advancements in Biofuels and Bioenergy Utilization. Singapore: Springer. pp. 303–337. doi:10.1007/978-981-13-1307-3_13. ISBN 978-981-13-1307-3.
- ^ en Khurmi, R. S. (). Material Science. S. Chand & Company.
- ^ en Schmidt-Rohr, K. (2018). "How Batteries Store and Release Energy: Explaining Basic Electrochemistry", J. Chem. Educ., 95: 1801–1810. https://doi.org/10.1021/acs.jchemed.8b00479
- ^ en "Types of Fuel Cells" Arhivat în , la Wayback Machine.. Department of Energy EERE website, accessed 4 August 2011
- ^ en „Mr. W. R. Grove on a new Voltaic Combination”. The London and Edinburgh Philosophical Magazine and Journal of Science. . doi:10.1080/14786443808649618. Accesat în .
- ^ en Grove, William Robert (). „On Voltaic Series and the Combination of Gases by Platinum”. Philosophical Magazine and Journal of Science. XIV (86–87): 127–130. doi:10.1080/14786443908649684.
- ^ en „On the Voltaic Polarization of Certain Solid and Fluid Substances” (PDF). The London and Edinburgh Philosophical Magazine and Journal of Science. . Arhivat din original (PDF) la . Accesat în .
- ^ en Grove, William Robert (). „On a Gaseous Voltaic Battery”. Philosophical Magazine and Journal of Science. XXI (140): 417–420. doi:10.1080/14786444208621600.
- ^ a b en Larminie, James (). Fuel Cell Systems Explained, Second Edition. Society of Automotive Engineers. ISBN 978-0-7680-1259-0.
- ^ en „The Brits who bolstered the Moon landings”. BBC. Accesat în .
- ^ en „Apollo 11 mission 50 years on: The Cambridge scientist who helped put man on the moon”. Cambridge Independent. Accesat în .
- ^ en „Fuel Cell Project: PEM Fuel Cells photo #2”. americanhistory.si.edu.
- ^ en „Collecting the History of Proton Exchange Membrane Fuel Cells”. americanhistory.si.edu.
- ^ en „Roger Billings Biography”. International Association for Hydrogen Energy. Arhivat din original la . Accesat în .
- ^ „Spotlight on Dr. Roger Billings”. Computer Technology Review. Arhivat din original la . Accesat în .
- ^ en „The PureCell Model 400 – Product Overview”. UTC Power. Arhivat din original la . Accesat în .
- ^ Eshani ș.a., Modern…, p. 348
- ^ a b c Eshani ș.a., Modern…, p. 349
- ^ Eshani ș.a., Modern…, p. 350
- ^ Eshani ș.a., Modern…, p. 351
- ^ a b Eshani ș.a., Modern…, p. 352
- ^ a b Eshani ș.a., Modern…, p. 353
- ^ a b c Eshani ș.a., Modern…, p. 354
- ^ a b c Eshani ș.a., Modern…, p. 355
- ^ en „Fuel Cells”. EnergyGroove.net. Accesat în .
- ^ a b en „High-Performance Materials”. Tex Tech Industries. Accesat în .
- ^ a b c d Oana Oneț, Elena Breaz, Dumitru Pop, Daniela Bordencea, Radu Tîrnovan, Eficiența unei pile cu combustibil cu membrană schimbătoare de protoni, stiintasiinginerie.ro, A XI-a Conferință Națională „Dorin Pavel”, Sebeș, 2011, accesat 2021-04-21
- ^ en Millington, Ben; Du, Shangfeng; Pollet, Bruno G. (). „The Effect of Materials on Proton Exchange Membrane Fuel Cell Electrode Performance”. Journal of Power Sources. 196 (21): 9013–017. doi:10.1016/j.jpowsour.2010.12.043.
- ^ Eshani, ș.a., Modern…, p. 357
- ^ Eshani ș.a., Modern…, p. 348
- ^ Eshani ș.a., Modern…, p. 354, 358
- ^ Eshani ș.a., Modern…, p. 358
- ^ a b c Eshani ș.a., Modern…, p. 361
- ^ a b en „Collecting the History of Phosphoric Acid Fuel Cells”. americanhistory.si.edu.
- ^ Eshani ș.a., Modern…, p. 359
- ^ a b c d en Daniel K. Rickleff, Hydrogen Powered Military Vehicles: A Vision or Reality by 2040?, dtic.mil, 2004, accesat 2021-04-24
- ^ Eshani ș.a., Modern…, p. 360
- ^ en Reuters Editorial (). „Platinum-free fuel cell developed in Japan”. Reuters. Accesat în .
- ^ a b c d en Comparison of Fuel Cell Technologies, energy.gov, accesat 2021-04-23
- ^ en Daniel K. Rickleff, Hydrogen Powered Military Vehicles: A Vision or Reality by 2040?, dtic.mil, 2004, accesat 2021-04-24
- ^ a b c d e Eshani, Modern…, p. 362
- ^ en Bodén, Andreas (). „The anode and the electrolyte in the MCFC” (PDF). Diva Portal. Accesat în .
- ^ en Wijayasinghe, Athula (). „Development and Characterisation of Cathode Materials for the Molten Carbonate Fuel Cell” (PDF). Accesat în .
- ^ a b c en „Types of Fuel Cells”. Office of Energy Efficiency and Renewable Energy, United States Department of Energy. Accesat în .
- ^ en „NFCRC Tutorial: Molten Carbonate Fuel Cell (MCFC)”. www.nfcrc.uci.edu. Arhivat din original la . Accesat în .
- ^ en R.P. Siegel, Fuel Cell Energy: Pros and Cons, triplepundit.com, 10 mai 2012, accesat 2021-04-26
- ^ a b Eshani, Modern…, p. 363
- ^ en R. Kerr, Effect of Sulfur on SOFC Performance Using Diesel Reformate, energy.gov, Workshop on Gas Cleanup for Fuel Cell Applications, ANL, 6–7 March 2014, accesat 2021-04-28
- ^ en Fangfang Wang, Haruo Kishimoto, Tomohiro Ishiyama, Katherine Develos-Bagarinao, Katsuhiko Yamaji, Teruhisa Horita, HarumiYokokawa, A review of sulfur poisoning of solid oxide fuel cell cathode materials for solid oxide fuel cells, Journal of Power Sources, Volume 478, 1 December 2020, 228763
- ^ en Sammes, N.M.; et al. (). „Design and fabrication of a 100 W anode supported micro-tubular SOFC stack”. Journal of Power Sources. 145 (2): 428–434. Bibcode:2005JPS...145..428S. doi:10.1016/j.jpowsour.2005.01.079.
- ^ en Panthi, D.; et al. (). „Micro-tubular solid oxide fuel cell based on a porous yttria-stabilized zirconia support”. Scientific Reports. 4: 5754. Bibcode:2014NatSR...4E5754P. doi:10.1038/srep05754. PMC 4148670
 . PMID 25169166.
. PMID 25169166.
- ^ en Florian-Patrice Nagel, Electricity from wood through the combination of gasification and solid oxide fuel cells, Ph.D. Thesis, Swiss Federal Institute of Technology Zurich, 2008
Bibliografie[modificare | modificare sursă]
- en Mehrdad Eshani, Yimin Gao, Sebastien E. Gay, Ali Emadi, Modern Electric, Hybrid Electric, and Fuel Cell Vehicles: Fundamentals, Theory and Design, Boca Raton, London, New York, Washington DC: CRC Press LLC, 2005, ISBN: 0-8493-3154-4
Lectură suplimentară[modificare | modificare sursă]
- I. Ștefănescu ș.a. Pile de combustibil - între teorie și practică, Editura Conphys, Rm. Vâlcea, 2010
- Gabriel L. Pavel, Modelarea pilelor de combustie de tip PEMFC, 2009
- D. Constantinescu, D.I. Văireanu, Tehnologia proceselor electrochimice, Printech București, 2000
- S. Muscalu, V. Platon, Pile de combustie, Editura Tehnică, București 1989
- I. G. Murgulescu, O. M. Radovici Introducere în chimia fizică, vol IV, "Electrochimia" Editura Academiei, București, 1986, p. 54-55
- A. Rădoi, Electromobilul, Editura Tehnică, București, 1981
- L. Oniciu, Conversia electrochimică a energiei, Editura tehnică 1977
- L. Oniciu, Pile de combustie, Editura Dacia 1971







































