Niobiu
| Niobiu | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 Cristale de niobiu | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Informații generale | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Nume, Simbol, Număr | Niobiu, Nb, 41 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Serie chimică | metale de tranziție | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Grupă, Perioadă, Bloc | 5, 5, d | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Densitate | 8570 kg/m³ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Culoare | gri metalic, albăstrui când e oxidat | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Număr CAS | 7440-03-1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Proprietăți atomice | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masă atomică | 92.90637(2) u | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rază atomică | 146 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rază de covalență | 164±6 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Configurație electronică | [Kr] 4d4 5s1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Electroni pe nivelul de energie | 2, 8, 18, 12, 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Număr de oxidare | 5, 4, 3, 2, -1 (un oxid ușor acid) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Structură cristalină | rețea cubică centrată intern | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Proprietăți fizice | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fază ordinară | solidă | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punct de topire | 2750 K (2477 °C, 4491 °F) K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punct de fierbere | 5017 K (4744 °C, 8571 °F) K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Energie de fuziune | 30 kJ kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Energie de evaporare | 689,9 kJ kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Temperatură critică | 9,2 K K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Volum molar | 10,83 m³/kmol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Viteza sunetului | 3480 m/s la 20 °C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Informații diverse | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Electronegativitate (Pauling) | 1,6 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Conductivitate termică | 53,7 W/(m·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Prima energie de ionizare | kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| A 2-a energie de ionizare | {{{potențial_de_ionizare_2}}} kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| A 3-a energie de ionizare | {{{potențial_de_ionizare_3}}} kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| A 4-a energie de ionizare | {{{potențial_de_ionizare_4}}} kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| A 5-a energie de ionizare | {{{potențial_de_ionizare_5}}} kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| A 6-a energie de ionizare | {{{potențial_de_ionizare_6}}} kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| A 7-a energie de ionizare | {{{potențial_de_ionizare_7}}} kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| A 8-a energie de ionizare | {{{potențial_de_ionizare_8}}} kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| A 9-a energie de ionizare | {{{potențial_de_ionizare_9}}} kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| A 10-a energie de ionizare | kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cei mai stabili izotopi | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Unitățile SI și condiții de temperatură și presiune normale dacă nu s-a specificat altfel. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Modifică text |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Niobiul (cunoscut și sub precedenta denumire de columbiu) este un element chimic notat cu simbolul Nb și numărul atomic 41. Este un metal de tranziție moale, de culoare gri, ductil, fiind găsit des în mineralele piroclor și în columbit, de unde și fosta denumire de „columbiu”. Numele metalului provine din mitologia greacă, fiind numit după Niobe, fiica lui Tantal. Numele reflectă similaritatea ridicată ale caracteristicilor fizice și chimice ale celor două elemente, fapt ce le face greu de distins.
În anul 1801, chimistul englez Charles Hatchett a descoperit un nou element similar cu tantalul și l-a numit columbiu (notat cu Cb); în 1808, chimistul englez William Hyde Wollaston a concluzionat greșit că tantalul și columbiul sunt identici. Chimistul german Heinrich Rose a determinat în 1846 că minereurile de tantal conțineau un al doilea element, pe care l-a numit niobiu. În 1864 și 1865, o serie de descoperiri științifice au clarificat că niobiul și columbiul erau același element (diferite de tantal), iar pentru un secol ambele nume au fost folosite alternativ. „Niobiu” a fost adoptat ca numele oficial al elementului în 1949, dar numele de columbiu rămâne în utilizarea curentă în metalurgie în Statele Unite.
Niobiul a fost folosit comercial abia la începutul secolului 20. Brazilia este producătorul principal al niobiului și al feroniobiului, (un aliaj al niobiului cu fier ce conține 60-70% niobiu). Niobiul este folosit în special în aliaje, de obicei în oțeluri precum cele utilizate în fabricarea conductelor de gaz. Deși aceste aliaje conțin maxim de 0,1% niobiu, acest procentaj este suficient pentru a crește duritatea oțelului. Stabilitatea termică a superaliajelor ce conțin niobiu justifică utilizarea sa în motoarele cu reacție și cele ale rachetelor.
Niobiul este folosit în diverse materiale supraconductibile. Aceste aliaje supraconductibile (care mai conțin și titan și staniu) sunt folosite pe scară largă în magneți supraconductori pentru scannerele IRM. Printre alte utilizări ale niobiului se numără folosirea sa în sudură, industria nucleară, electronică, optică, numismatică și fabricarea de bijuterii. Toxicitatea mică și irizația căpătată prin anodizare a niobiului sunt avantaje particulare daca se face referire la ultimele două utilizări.
Istoric[modificare | modificare sursă]

Descoperirea metalului a fost făcută de către chimistul englez Charles Hatchett în anul 1801,[1] depistând un nou element în interiorul unei probe de mineral ce a fost trimisă în Anglia din Connecticut, Statele Unite în 1734 de către John Whintrop F.R.S. (nepotul lui John Whintrop Jr.); mineralul a fost numit columbită și elementul columbiu, după Columbia, numele poetic pentru Statele Unite.[2][3][4] Columbiul descoperit de Hatchett era probabil un amestec al noului element cu tantalul.[2]
Ulterior, a existat o confuzie considerabilă[5] în ceea ce privește columbiul (niobiul) și asemănătorul tantal. În 1809, chimistul englez William Hyde Wollaston a comparat oxizii derivați și din columbiu—columbită, având o densitate de 5,918 g/cm3 și pe cei de tantal—tantalită, care aveau peste 8 g/cm3, concluzionând că cei doi oxizi, în ciuda diferențelor de densitate, erau identici; astfel el a păstrat numele de tantal.[5] Concluzia a fost disputată în 1846 de către chimistul german Heinrich Rose, care susținea că erau 2 elemente diferite în proba de tantalită, numindu-i după copii lui Tantal: niobiu (de la Niobe) și pelopiu (de la Pelops).[6][7] Această confuzie s-a iscat din cauza diferențelor minime între tantal și niobiu. Noile elemente chimice pelopiu, ilmeniu și dianiu[8] erau de fapt identice cu niobiul sau amestecuri ale acestuia cu tantalul.[9]
Diferențele între tantal și niobiu au fost demonstrate irevocabil în 1864 de către Christian Wilhelm Blomstrand,[9] Henri Etienne Sainte-Claire Deville, și Louis J. Troost, care au determinat formulele unora dintre compuși în 1865[9][10] și în final de chimistul elvețian Jean Charles Galissar de Marignac[11] în 1866, cu toții demonstrând că existau doar 2 elemente. Articole despre ilmeniu au continuat să apară până în 1871.[12]
De Marignac a fost primul care a preparat metalul în 1864, când a redus clorura de niobiu încălzind-o într-o atmosferă de hidrogen.[13] Deși Marignac putea produce niobiu care nu conținea tantal pe scară largă în 1866, abia la începutul secolului 20 niobiul a început să fie folosit comercial, în filamentele lămpilor incandescente - prima aplicație comercială.[10] Aceasta a devenit rapid nefolositoare odată cu înlocuirea niobiului cu tungstenul, care are o temperatură de topire mai ridicată, fiind astfel preferabil pentru folosirea în lămpile incandescente. În 1920 s-a descoperit că niobiul crește duritatea oțelului, astăzi aceasta rămânând utilizarea principală.[10] În 1961 fizicianul american Eugene Kunzler și colegii săi de la Bell Labs au descoperit că aliajul de niobiu-staniu continuă să fie supraconductibil în prezența curenților electrici puternici și a câmpurilor magnetice,[14] făcându-l primul material descoperit care suportă intensitățile ridicate și câmpurile necesare pentru magneți de mare putere și utilaje electrice. Această descoperire va permite - 2 decenii mai târziu - producția de bobine alcătuite din cabluri multifilare pentru a crea electromagneți mari și puternici pentru uzul în aparatura rotativă, acceleratoarele de particule și detectoarele de particule.[15][16]
Nomenclatură[modificare | modificare sursă]

Columbiu (simbol Cb[17]) a fost numele original dat acestui element de către Hatchett, el rămânând în uz în publicațiile americane - ultimul articol publicat de Societatea Americană de Chimie având columbiu în cuprinsul său datează din 1953[18] - în timp ce niobiu era folosit în Europa. Pentru a pune capăt acestei confuzii, numele niobiu a fost ales pentru elementul cu numărul 41 la a 15-a Conferință a Uniunii Chimiei în Amsterdam în 1949.[19] Un an mai târziu, acest nume a fost oficial adoptat de Uniunea Internațională de Chimie Pură și Aplicată (IUPAC) după 100 de ani de controverse, în ciuda precedenței cronologice a numelui columbiu.[19] Ultimul nume este încă folosit, uneori, în industria SUA.[20] Acesta a fost un fel de compromis;[19] IUPAC a acceptat tungsten în loc de wolfram, numele folosit în America de Nord; și niobiu în loc de columbiu, numele folosit de europeni. În timp ce multe societăți chimice americane și organizații guvernamentale folosesc, de obicei, numele oficial IUPAC, unii metalurgiști și societăți metalurgice încă folosesc numele original al elementului, columbiu.[21][22]
Structură atomică[modificare | modificare sursă]

Structura atomului de niobiu este determinată de numărul nucleonilor din nucleul atomic, astfel că pentru izotopul său natural, 93Nb, niobiul are 41 de protoni și 52 de neutroni. Numărul neutronilor poate varia în funcție de izotop. Raza atomică medie este de 1.47Å,[23], raza ionică e de 0.07Å,[24] iar volumul molar al niobiului este de 10.84.3/mol[25] Raza covalentă este de 1.34Å.[26]
Configurația electronică a niobiului este 4d35s2, iar cea mai comună și importantă stare de oxidare este +5.[26]
Niobiul este un element monoizotopic, cu toate ca acțiunile de cercetare ale radionuclizilor originati de la formarea Sistemului Solar au condus spre izotopii 92Nb, 94Nb si 95Nb; abundenta relativa ale acestor izotopi este foarte mica [27]; singurul său izotop stabil este 93Nb.[28]
Din 2003, cel puțin 32 de radioizotopi au fost sintetizați, masa lor atomică variind între 81 și 113. Cel mai stabil dintre aceștia este 92Nb , având un timp de înjumătățire de 34,7 milioane de ani. Unul dintre cei mai puțin stabili este 113Nb cu un timp de înjumătățire estimat la 30 de milisecunde. Izotopii care sunt mai ușori decât 93Nb tind să se dezintegreze prin dezintegrare beta (β+), iar cei care sunt mai grei tind să se dezintegreze prin β-, cu unele excepții. 81Nb, 82Nb, și 84Nb au căi de dezintegrare prin emisie de protoni întârziate de β+, 91Nb se dezintegrează prin captura de electroni și emisia de pozitroni, iar 92Nb se dezintegrează și prin dezintegrare β+ și β-.[28]
Cel puțin 25 de izomeri nucleari au fost descriși, masa lor atomică variind între 84 și 104. În acest interval, doar 96Nb, 101Nb, și 103Nb nu au izomeri. Cel mai stabil izomer al niobiului este 93mNb, cu un timp de înjumătățire de 16,13 ani. Cel mai puțin stabil izomer este 84mNb, cu un timp de înjumătățire de doar 103 ns. Toți izomerii niobiului se dezintegrează prin tranziție izomerică sau dezintegrare beta, excepție făcând 92m1Nb, care are un lanț de dezintegrare prin captură de electroni minor.[28]
Proprietăți[modificare | modificare sursă]
Proprietăți fizice[modificare | modificare sursă]
Niobiul este un metal lucios, gri, ductil, paramagnetic din grupa 5 a tabelului periodic (vezi tabelul), deși are o configurație atipică în ultimul său nivel energetic în comparație cu restul membrilor grupei. Acest lucru poate fi observat în vecinătatea ruteniului (44), rodiului (45) și a paladiului (46).
| Z | Element | Nr. de electroni/nivel |
|---|---|---|
| 23 | vanadiu | 2, 8, 11, 2 |
| 41 | niobiu | 2, 8, 18, 12, 1 |
| 73 | tantal | 2, 8, 18, 32, 11, 2 |
| 105 | dubniu | 2, 8, 18, 32, 32, 11, 2 (prezis) |
Prezintă un punct înalt de topire (2468 °C), care este depășit doar de 6 elemente: carbon, tungsten, reniu, tantal, osmiu și molibden,[29] iar punctul de fierbere este de 5127 °C.[30]
Deși se crede că are o structură cristalină cubică centrată intern de la zero absolut până la punctul de topire, măsurători cu rezoluție înaltă a expansiunii termale de-a lungul celor trei axe cristalografice arată prezența unor anizotropi inconsistenți cu structura cubică. De aceea, probabil vor exista studii suplimentare în această arie.
Niobiul devine un supraconductor la temperaturi criogenice. La presiunea atmosferică, are cea mai ridicată temperatură critică dintre supraconductorii elementari: 9,2 K.[31] Niobiul are cea mai mare adâncime de penetrație magnetică a oricărui element.[31] În plus, este unul din cei trei supraconductori elementari de tip II, împreună cu vanadiul și technețiul. Proprietățile supraconductive depind mult de puritatea niobiului.[32] Când e foarte pur, e moale și ductil, impuritățile făcând-ul mai rigid.[33]
Metalul are o secțiune eficace pentru neutronii termali mică;[34] de aceea e folosit în industria nucleară.[35]
Proprietăți chimice[modificare | modificare sursă]
Niobiul prezintă un caracter chimic extrem de complex: elementul în sine prezintă proprietăți metalice, pentoxidul sau este acid, în timp ce alți compuși de valență mai scăzută prezintă, de regulă, un caracter bazic[36].
Metalul prinde o nuanță albăstruie când e expus la aer la temperatura camerei pentru perioade extinse;[37] pe măsură ce temperatura niobiului creste, acesta suferă anumite schimbări ale culorii în absenta oxigenului, trecând de la luciul metalic la galben, violet, albastru, verde și în final spre alb (sub forma pentoxidului de niobiu la 390 grade).[38]
La temperatura camerei, niobiul nu este atacat de HCl diluat, în timp ce HCl concentrat îi conferă un aspect ușor corodat. La 100 grade, reacția cu HCl concentrat este mult mai pronunțată, cauzând metalul să fie mult mai fragil. Aqua regia și acidul azotic concentrat nu atacă metalul. Acidul fluorhidric reacționează moderat cu niobiul, iar prin adiția acidului azotic, metalul se poate dizolva complet. Acidul sulfuric diluat nu atacă niobiul, însă cel concentrat reacționează cu metalul direct proporțional cu temperatura (cu cât crește aceasta, viteza reacției crește de asemenea). Metalul devine fragil la 100 de grade folosind acid ortofosforic de concentrație 85%.[38]
Niobiul e mai puțin electropozitiv și mai compact decât predecesorul său în tabelul periodic, zirconiul, însă e relativ identic cu atomii mai grei de tantal, din cauza contracției lantanidelor.[33] Rezultatul este că proprietățile chimice ale niobiului sunt foarte similare cu cele ale tantalului, care apare direct sub niobiu în tabelul periodic.[10] Deși rezistența sa la coroziune nu e la fel de excepțională ca cea a tantalului, prețul său mai scăzut și disponibilitatea crescută fac niobiul mai atractiv pentru utilizările mai puțin pretențioase, cum ar fi căptușirea interioarelor instalațiilor chimice.[33]
Răspândire[modificare | modificare sursă]
Niobiul este estimat a fi al 33-lea cel mai comun element în scoarța Pământului, cu 20 de părți pe milion,[39] similar cu cobaltul și litiul.[40] Unii cred că abundența sa pe Pământ e mult mai mare, densitatea sa ridicată concentrându-l în nucleul Pământului.[21] Elementul liber nu e găsit în natură, însă niobiul apare în combinație cu alte elemente în minerale.[33] Mineralele care conțin niobiu de obicei conțin și tantal. Exemplele includ columbita ((Fe,Mn)(Nb,Ta)2O6) și columbita-tantalita (sau coltan, (Fe,Mn)(Ta,Nb)2O6).[41] Mineralele de columbită-tantalită sunt de obicei găsite în cantități infime în intruziile de pegmatită, și în rocile intruzive alcaline. Niobații de calciu, uraniu, thoriu și cei ai pământurilor rare sunt mai puțin comuni. Exemple a acestor niobați sunt piroclorul ((Na,Ca)2Nb2O6(OH,F)) (acum un nume de grupă, un nume destul de comun fiind, de exemplu, fluorcalciopiroclor) și euxenita (corect denumită euxenită-(Y)) ((Y,Ca,Ce,U,Th)(Nb,Ta,Ti)2O6). Aceste mari depozite de niobiu au fost descoperite asociate cu carbonatitele (roci magmatice de tip carbonat-silicat) și ca un constituent al piroclorului.[42]
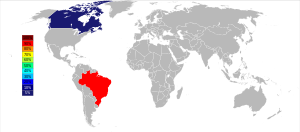
Dintre cele mai mari trei depozite de piroclor, două au fost găsite în anii 1950 în Brazilia și Canada, ambele țări fiind încă principalii producători de concentrați de mineral de niobiu.[10] Cel mai mare depozit se află într-o intruzie de carbonatită la Araxá, Minas Gerais în Brazilia, deținut de CBMM (Companhia Brasileira de Metalurgia e Mineração), celălalt depozit în exploatare e localizat în apropiere de Catalão, Goiás și e deținut de China Molybdenum, de-asemenea aflat într-o intruzie de carbonatită.[43] Puse la un loc, aceste 2 mine braziliene produc circa 88% din rezerva globală.[44] Brazilia mai deține un depozit mare, însă neexploatat, lângă São Gabriel da Cachoeira, unitatea federativă Amazonas, precum și mai multe depozite mai mici, în principal în unitatea federativă Roraima.
Al treilea cel mai mare producător de niobiu este mina Niobec, aflată tot într-o intruzie de carbonatită, din Saint-Honoré, lângă Chicoutimi, Quebec, deținută de Magris Resources, care produce în jur de 7-10% din rezerva globală.[43] Depozitele Kenyei găsite în Kwale sunt printe primele 6 din lume.[45] De curând, NioCorp consideră deschiderea unei mine în Elk Creek, Nebraska pentru a începe producția în Statele Unite.[46] Niobiul mai poate fi întâlnit ca reziduu în urma extragerii de staniu.[47]
Compuși[modificare | modificare sursă]
Niobiul e similar cu tantalul și zirconiul în multe feluri. Reacționează cu majoritatea nemetalelor la temperaturi ridicate: niobiul reacționează cu fluorul la temperatura camerei, cu clorul și hidrogenul la 200 °C, și cu azotul la 400 °C, rezultând compuși ce sunt frecvent interstițiali și nonstoichiometrici.[33] Metalul începe să oxideze în aer la 200 °C,[48] fiind rezistent la coroziunea amestecurilor de metale alcaline și a acizilor, incluzând aqua regia și acizii clorhidrici, sulfurici, nitrici și fosforici.[33] Niobiul e atacat de către acidul fluorhidric și amestecurile de acizi fluorhidrici/nitrici.
Deși niobiul are toate numerele de oxidare formale de la +5 la -1, în majoritatea compușilor, e găsit având numărul de oxidare +5.[33] Caracteristic, compușii ce au numere de oxidare mai mici de +5 arată legătura Nb–Nb.
Oxizi și sulfuri[modificare | modificare sursă]
Niobiul formează oxizi cu numărul de oxidare +5 (Nb2O5), +4 (NbO2) și +3 (Nb2O3),[48], și de asemenea și cu numărul de oxidare mai rar +2 (NbO).[49] Cel mai des întâlnit este pentoxidul, precursor al aproape tuturor compușilor și aliajelor niobiului.[48][50] Niobații sunt generați prin dizolvarea pentoxidului în soluții bazice de hidroxizi sau prin topirea sa în oxizi ai metalelor alcaline. Exemple sunt niobatul de litiu (LiNbO3) și niobatul de lantan (LaNbO4). În niobatul de litiu există o structură distorsionată asemănătoare cu perovskita, pe când niobatul de lantan conține ioni NbO3−
4.[48] Sulfidul stratificat de niobiu (NbS2) e de asemenea cunoscut.[33]
Materialele cu un înveliș subțire de oxid de niobiu (V) pot fi produse prin procesele de depoziție de vapori chimici sau de depoziție de straturi atomice, în fiecare caz prin descompunerea termală a etoxidului de niobiu (V) la peste 350 °C.[51][52]
Halogenuri[modificare | modificare sursă]

Niobiul formează halogenuri cu numerele de oxidare +5 și +4, precum și diverși compuși substoichiometrici.[48][53] Pentahalogenurile (NbX
5) au centri de Nb octaedrici. Pentafluorura de niobiu (NbF5) e un solid alb cu o temperatură de topire de 79.0 °C iar pentaclorura de niobiu (NbCl5) e galbenă (vezi imaginea din stânga), având o temperatură de topire de 203.4 °C. Ambele sunt hidrolizate pentru a da oxizi și oxihalogenuri, cum ar fi NbOCl3. Pentaclorura e un reactiv versatil, fiind folosită la generarea de compuși organometalici, cum ar fi diclorura de niobocen ((C
5H
5)
2NbCl
2).[54] Tetrahalogenurile (NbX
4) sunt polimeri închiși la culoare cu legături Nb-Nb, cum ar fi tetraflorura neagră, higroscopică de niobiu (NbF4) și tetraclorura maro de niobiu (NbCl4).

Compușii halogenurilor anionice sunt binecunoscute, acest fapt datorându-se acidității Lewis a penthalogenurilor. Cel mai important e [NbF7]2-, care e un intermediar în separarea Nb și Ta din minereuri.[41] Această heptafluorură tinde să formeze oxopentafluorura mai ușor decât o face compusul tantalului. Alți compuși halogenici includ octaedrica [NbCl6]−:
- Nb2Cl10 + 2 Cl− → 2 [NbCl6]−
Pentru metalele timpurii, o varietate de grupuri de halogenuri sunt cunoscute, un prim exemplu fiind [Nb6Cl18]4−.[55]
Nitruri și carburi[modificare | modificare sursă]
Ați compuși binari ai niobiului includ nitrura de niobiu (NbN), care devine un supraconductor la temperaturi joase și e folosită la detectorii de lumină infraroșie.[56] Principalul carbid de niobiu este NbC, un metal extrem de tare, refractar și ceramic, fiind folosit comercial la uneltele de tăiat.
Producere[modificare | modificare sursă]
Niobiul este obținut prin reducție electrochimica ale topiturilor de fluoruri complexe K2[NbOF5] și K2[TaF7], prin reducția fluorurilor cu sodiul la 800 de grade, reducția Nb2O5 sau Ta2O5 cu carbon la 2300 de grade[57].
După separarea de celelalte minerale, oxizii amestecați ai tantalului Ta2O5 și ai niobiului Nb2O5 sunt obținuți. Primul pas al procesului e reacția oxizilor cu acidul fluorhidric:[41]
- Ta2O5 + 14 HF → 2 H2[TaF7] + 5 H2O
- Nb2O5 + 10 HF → 2 H2[NbOF5] + 3 H2O
Prima separație la scală industrială, dezvoltată de de Marignac, exploatează solubilitățile diferite ale fluorurilor complexe de niobiu și tantal, monohidrat oxipentafluoriniobat de dipotasiu (K2[NbOF5]·H2O) și heptafluorotantalat de dipotasiu (K2[TaF7]) în apă. Procesele mai noi folosesc extracția lichidă a fluorurilor din soluții apoase prin solvenți organici, cum ar fi ciclohexanona.[41] Fluorurile complexe de niobiu și tantal sunt extrase separat din solventul organic cu apă și ori precipitate prin adăugarea de fluorură de potasiu pentru a produce un compus de fluorură de potasiu, ori cu amoniac ca pentoxid:[48]
- H2[NbOF5] + 2 KF → K2[NbOF5]↓ + 2 HF
Urmat de:
- 2 H2[NbOF5] + 10 NH4OH → Nb2O5↓ + 10 NH4F + 7 H2O
Mai multe metode sunt folosite pentru reducerea în forma de metal a niobiului. Electroliza unui amestec topit de K2[NbOF5] și clorură de sodiu este unul; celălalt este reducere fluorurii cu sodiu. Niobiul, având o puritate relativ foarte mare, este obținut astfel. În producția pe scară largă este folosită reducerea Nb2O5 cu hidrogen sau carbon.[48] În procesul ce include reacția aluminotermică, un amestec de oxid de fier și oxid de niobiu e pus într-o reacție cu aluminiul:
- 3 Nb2O5 + Fe2O3 + 12 Al → 6 Nb + 2 Fe + 6 Al2O3
Pentru a intensifica reacția, sunt adăugate cantități mici de oxidanți cum ar fi nitratul de sodiu. Rezultă oxidul de aluminiu și feroniobiul, un aliaj al fierului cu niobiului folosit în producerea oțelului.[58][59] Feroniobiul conține între 60% și 70% niobiu.[43] Fără adăugarea de oxid de fier, pentru producția niobiului e folosit procesul aluminotermic. Pentru a atinge marja aliajelor supraconductoare, este necesară purificarea ulterioară. Topirea cu fascicul de electroni în vid e metoda folosită de către cei doi principali distribuitori de niobiu.[53][60]
În 2013, compania braziliană Cia. Brasileira de Metalurgia & Mineracao „controla 85% din producția mondială de niobiu.”[61] Serviciul de prospectare geologică al Statelor Unite estimează că producția a crescut de la 38.700 tone în 2005 la 44.500 tone în 2006.[62][63] Resursele globale sunt estimate la 4.400.000 tone.[63] În timpul perioadei de 10 ani dintre 1995 și 2005, producția mai mult decât s-a dublat, începând de la 17.800 tone în 1995.[64] Din 2009, producția rămâne în jurul a 63.000 tone pe an.[65]
| Țara | 2000 | 2001 | 2002 | 2003 | 2004 | 2005 | 2006 | 2007 | 2008 | 2009 | 2010 | 2011 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 160 | 230 | 290 | 230 | 200 | 200 | 200 | ? | ? | ? | ? | ? | |
| 30.000 | 22.000 | 26.000 | 29.000 | 29.900 | 35.000 | 40.000 | 57.300 | 58.000 | 58.000 | 58.000 | 58.000 | |
| 2.290 | 3.200 | 3.410 | 3.280 | 3.400 | 3.310 | 4.167 | 3.020 | 4.380 | 4.330 | 4.420 | 4.400 | |
| ? | 50 | 50 | 13 | 52 | 25 | ? | ? | ? | ? | ? | ? | |
| ? | ? | 5 | 34 | 130 | 34 | 29 | ? | ? | ? | ? | ? | |
| 35 | 30 | 30 | 190 | 170 | 40 | 35 | ? | ? | ? | ? | ? | |
| 28 | 120 | 76 | 22 | 63 | 63 | 80 | ? | ? | ? | ? | ? | |
| Lume | 32.600 | 25.600 | 29.900 | 32.800 | 34.000 | 38.700 | 44.500 | 60.400 | 62.900 | 62.900 | 62.900 | 63.000 |
Cantități mai mici sunt găsite în Depozitul Kanyika din Malawi (mina Kanyika).
Utilizare[modificare | modificare sursă]

Este estimat că din 44.500 tone de niobiu minate în 2006, 90% au fost folosite în producerea de oțel, urmat de utilizarea lor în fabricarea superaliajelor.[67] Folosirea aliajelor niobiului în supraconductori și componentele electrice reprezintă doar o mică parte din producție.[67]
Producerea de oțel[modificare | modificare sursă]
Niobiul e un foarte bun element microaliator pentru oțel. Adăugarea niobiului în oțel cauzează formarea carbidului și nitrurii de niobiu în structura oțelului.[21] Acești compuși îmbunătățesc rafinarea cristalitelor, încetinirea recristalizării, și întărirea prin precipitare a oțelului. Aceste efecte în schimb cresc tăria, puterea, formabilitatea, și sudabilitatea oțelului microaliat.[21] Oțelurile inoxidabile microaliate conțin sub 0,1% niobiu.[68] E o importantă adiție pentru oțelurile microaliate care sunt larg folosite ca și componente structurale în automobilele moderne.[21] Aceste aliaje ce conțin niobiu sunt puternice, fiind des folosite în construcția conductelor.[69][70]
Component al otelului inoxidabil pentru aeronave, ustensile de bucătărie[71]
Aliaje bazate pe niobiu[modificare | modificare sursă]
Aliajul C-103 a fost dezvoltat în prima parte a anilor 1960 în același timp de către Wah Chang Corporation și Boeing Co. DuPont, Union Carbide Corp., General Electric Co. și mai multe alte companii, ce cercetau aliaje pe bază de niobiu simultan, conduse în mare parte de Războiul Rece și de Cursa Spațială. Senzitivitatea niobiului la oxigen necesită procesarea sa în vid sau într-o atmosferă inertă, care crește exponențial costul și dificultatea producției. Retopirea prin arc în vid (RAV) și topirea cu jet de electroni (TJE), tehnologii noi la acel timp, au permis dezvoltarea de metale reactive, cum ar fi niobiul. Proiectul aliajului C-103 a început în 1959 cu nu mai puțin de 256 de aliaje de niobiu experimentale în „seria C” (posibil de la columbiu) care puteau fi topite ca butoane și făcute în foițe. Wah Chang avea un inventar de hafniu, rafinat din aliaje de zirconiu de grad nuclear, pe care voia să le pună în uz comercial. Cea de a 103-a compoziție experimentală a aliajelor din seria C, Nb-10Hf-1Ti, avea cea mai bună combinație a formabilității și a proprietăților pentru temperaturi mari. Wah Chang a fabricat primele 250 kg de C-103 în 1961, lingouri sau foițe, folosind RAV și TJE. Aplicațiile intenționate erau componentele motoarelor cu turbină și ale schimbătoarelor de căldură din metale lichide. Aliajele de niobiu concurente din acea eră includeau FS85 (Nb-10W-28Ta-1Zr) de la Fansteel Metallurgical Corp., Cb129Y (Nb-10W-10H-0,2Y) de la Wah Chang și Boeing, Cb752 (Nb-10W-2,52Zr) de la Union Carbide, și Nb1Zr de la Superior Tube Co.[72]
Superaliaje[modificare | modificare sursă]

Cantități apreciabile ale elementului, ori în forma sa pură sau în cea de feroniobiu și niobiu-nichel, e folosit în superaliajele bazate pe nichel, cobalt și fier pentru diverse aplicații, cum ar fi componentele motoarelor cu reacție, turbinele cu gaze, subansamblurile de rachete, sistemele de turbo-încărcare, și echipamentele de combustie și rezistență la căldură. Niobiul precipită o fază de întărire γ'' în structura cristalitelor superaliajului.[73] Aliajele conțin până la 6,5% niobiu.[68] Un exemplu de superaliaj pe bază de nichel ce conține niobiu e Inconel 718, ce constă în aproximativ 50% nichel, 18,6% crom, 18,5% fier, 5% niobiu, 3,1% molibden, 0,9% titan, și 0,4% aluminiu.[74][75] Aceste superaliaje sunt folosite, spre exemplu, în fuzelajele avansate, cum ar fi cele folosite în programul Gemini.
Un aliaj folosit pentru duzele de propulsie ale rachetelor cu combustibil lichid, cum ar fi motorul principal al Modulelor Lunare Apollo, e aliajul de niobiu C-103, care constă în 89% niobiu, 10% hafniu și 1% titan.[72] Alt aliaj de niobiu a fost folosit pentru duza Modulului de Serviciu Apollo. Precum niobiul e oxidat la temperaturi de peste 400 °C, un înveliș de protecție e necesar pentru ca aceste aplicații să împiedice aliajul să devină sfărâmicios.[72]
Magneți supraconductori[modificare | modificare sursă]

Aliajele de niobiu-germaniu (Nb
3Ge), niobiu-staniu (Nb
3Sn) precum și cele de niobiu-titan sunt folosite ca fire supraconductoare de tip II pentru magneții supraconductori.[76][77] Acești magneți supraconductori sunt folosiți în aparatele de imagistică cu rezonanță magnetică și rezonanță magnetică nucleară precum și în acceleratoarele de particule.[78] De exemplu, acceleratorul Large Hadron Collider folosește 550 de tone de fire supraconductoare, în timp ce Reactorul Experimental Termonuclear Internațional folosește circa 600 de tone de fire de Nb3Sn și 250 de tine de fire de NbTi.[79] Doar în 1992, firele de niobiu-titan au fost folosite pentru a construi aparate de imagistică cu rezonanță magnetică clinice în valoare cumulată de peste 1 miliard de dolari.[15]
Supraconductibilitatea și altele[modificare | modificare sursă]
Cavitățile frecvențelor radio supraconductoare folosite în laserele cu electroni liberi FLASH (rezultat al proiectului anulat aș acceleratorului linear TESLA) și XFEL sunt făcute din niobiu pur.[80]
Superconductori feroviari[modificare | modificare sursă]
Sensibilitatea ridicată a bolometrilor nitrurii de niobiu supraconductori îi fac detectori ideali pentru radiația electromagnetică în banda de frecvență THz. Acești detectori au fost testați la Telescopul Submilimetru Heinrich Hertz, la Telescopul Polului Sud, la Telescopul Receiver Lab, și la APEX, fiind curent utilizați în instrumentul HIFI de la Observatorul Spațial Herschel.[81]
Alte utilizări[modificare | modificare sursă]
Criminalistică[modificare | modificare sursă]
În 2004, cercetătorii URFJ au dezvoltat luminolul brazilian, fabricat din niobiu. Luminolul este o substanță folosită de medicina criminalistă pentru a descoperi pete de sânge pe orice suprafețe, chiar și cele care au fost spălate. Luminolul importat din SUA este supus unor presiuni și temperaturi înalte, în timp ce luminolul brazilian este fabricat artizanal și este cu 90% mai ieftin decât cel importat.[82] O altă diferență este faptul că produsul importat necesită expunerea la radiație ultravioletă pentru localizarea urmelor de sânge, în timp ce substanța artizanală nu necesită această procedură, camera întunecată fiind mediul propice pentru depistarea acestor urme[82]
Electroceramica[modificare | modificare sursă]
Niobatul de litiu, care e feroelectric, e folosit pe scară largă în telefoanele mobile și modulatorii optici, și pentru fabricarea aparatelor de valuri acustice de suprafață. Are structura feroelectrică ABO3 ca tantalatul de litiu și titanatul de bariu.[83] Niobiul a fost evaluat ca fiind o alternativă mai ieftina a tantalului în condensatori,[84] dar condensatorii de tantal încă predomină. Niobiul e adăugat sticlei pentru a avea un indice de refracție mai mare, o proprietate folositoare pentru industria optică pentru a fabrica lentile de corecție mai subțiri.
Aplicații hipoalergenice: medicina și bijuteriile[modificare | modificare sursă]
Niobiul și unele aliaje ale acestuia sunt inerte fiziologic, și deci hipoalergenice. Din această cauza, niobiul e găsit în multe aparate medicale cum ar fi pacemaker-urile.[85] Niobiul tratat cu hidroxid de sodiu formează un strat poros care facilitează osteointegrația.[86]
Scannere medicale
Împreună cu titanul, tantalul, și aluminiul, niobiul poate fi încălzit electric și anodizat, rezultând într-o diversitate de culori folosind un proces cunoscut ca anodizarea metalelor reactive, care e folositor în fabricarea bijuteriilor.[87][88] Faptul că niobiul e hipoalergenic e benefic pentru utilizarea sa în bijuterii.[89]
Poate fi conținut în anumite componente ale ceasurilor[90]
Numismatică[modificare | modificare sursă]

Niobiul e folosit ca metal prețios în monedele comemorative, de obicei împreună cu argintul sau aurul. Austria a introdus în 2003 o moneda bimetalica de 10 euro, care conținea un miez de niobiu colorat în albastru-intens, fiind emisă în momentul celei de-a 700-a aniversare al celui mai vechi oraș; alte emisii ulterioare conțineau miezuri de niobiu violet și verde[91];culoarea acestor monede era dată de difracția luminii de către un strat de oxizi subțire produs de anodizare.[92]. Si alte tari au adoptat acest tip de monede, precum Mongolia si Sierra Leone[93].
În 2012, zece monede erau disponibile, având o varietate de culori în centrul lor: albastru, verde, maro, mov, violet sau galben. Alte două exemple sunt monedele comemorative ale Aniversării a 150 de ani ai Căii Ferate Alpine Semmering de 25 € din Austria,[94] și monedele comemorative ale Navigării prin Satelit Europene de 25 €.[95] Fabrica de bani austriacă a produs pentru Letonia o serie de monede similară începând din 2004,[96] cu alta urmând în 2007.[97]
În 2011, Fabrica de Bani Regală a Canadei a început producția unei monede de 5 $ din argint și niobiu numită Luna Vânătorului, (en „Hunter's Moon)[98] în care niobiul a fost oxidat selectiv, astfel creându-se monede unice, nici una fiind identică cu alta.
Altele[modificare | modificare sursă]
Sigiliile arc-tub ale lămpilor cu vapori de sodiu cu presiune ridicată sunt făcute din niobiu, sau niobiu cu 1% zirconiu, deoarece niobiul are un coeficient al expansiunii termale similar cu ceramicii arc-tub sinterizată de oxid de aluminiu, un material translucid ce rezistă la agenții chimici sau la reducere prin vaporii de sodiu lichid și fierbinte, conținut de lampa respectivă.[99][100][101] Metalul e de asemenea folosit în baghetele de sudură cu arc electric pentru unele grade stabilizate de oțel inoxidabil.[102] E folosit și ca un material în anozi pentru sistemele de protecție catodice ale unor rezervoare de apă, care sunt de obicei placate cu platină.[103][104] Construcția reactoarelor nucleare[105] Aliaj din niobiu și tantal este conținut în vârful pixurilor, datorită proprietății sale de rezistență împotriva coroziunii[90]
Rolul elementului în biologie[modificare | modificare sursă]
Niobiul nu are niciun rol biologic cunoscut. În timp ce praful de niobiu e un iritant al ochilor și pielii și un potențial pericol de incendiu, niobiul elemental pe scară largă e fiziologic inert (și deci hipoalergenic) și inofensiv. E des folosit în bijuterii și a fost testat pentru utilizarea în unele implanturi medicale.[106][107]
Niobiul este destul de prezent în organismul uman încât să poată fi depistat. Niobiul și compușii săi pot fi toxici, însă nu au existat raporturi privind intoxicații în rândul populației, cu toate că în Rusia există o limită de 10 ppb de niobiu în apa potabilă.[108]
Autorii Schroeder și Balassa au considerat niobiul ca fiind un element neglijat din punct de vedere biologic, afirmând acest lucru pe baza analizei nivelului de niobiu din țesuturile umane, precum și din cele animale (din sălbăticie și mediul domestic, precum și cele de laborator)[109]. Analizele au arătat urme de niobiu comparabile cu nivelul de cupru din țesuturi, fiind depășite de fier, zinc și rubidiu. Cantitatea de niobiu întâlnită în țesut proaspăt a fost de 0.5-3.0 micrograme/g țesut. Astfel, s-a sugerat un aport zilnic mai mare de 600 micrograme, dintre care aproximativ jumătate e absorbit și excretat prin urină[109].
Raporturi ulterioare au determinat valori opuse (microgram per gram de țesut): sânge 0.004±0.0005; rinichi 0.01±0.004; ficat 0.004±0.009; plămâni 0.02±0.0001; ganglioni limfatici 0.06±0.007; mușchi 0.03±0.008; testicule 0.009±0.04. Oasele conțineau mai puțin de 0.07 micrograme per gram de cenușă. [109] Cu toate că s-a arătat că aceste niveluri nu sunt periculoase pentru om, studiile pe șobolani au indicat faptul cp niobiul tinde sp se acumuleze în gonade, rinichi, plămâni, ficat și splină; aceasta a condus la scăderea duratei medii de viață, stoparea creșterii și incidența degenerării hepatice[109].
Deși niobiul în sine nu prezintă un rol biologic, compușii săi organici afectează organismele; aceștia au arătat activitate antitumorală și anti-retrovirală (HIV) in vitro și în urma experimentelor pe șoareci[110] Efectul niobiului a fost studiat asupra limfocitelor de tip CD+4T. Rezultatele obținute au demonstrat ca ionii metalului nu produc daune ADN-ului înaintea altor forme toxice (precum apoptiza și/sau necroza).[111]
Măsuri de protecție chimică[modificare | modificare sursă]
Cu toate că nu se cunoaște modul în care niobiul ar afecta sau nu organismul biologic, efectele niobiului au fost studiate asupra viabilității celulare și fosfatazei-alcaline, efectul fiind studiat in vitro utilizând 2 tipuri de celule osteoblaste, MG-63 și celule HOS. În prezenta niobiului, viabilitatea celulelor era scăzuta, fosfataza-alcalină a rămas constantă, iar celulele HOS au fost cu mult mai sensibile la acțiunea niobiului decât celulele MG-63.[111]
Compușii niobiului sunt rar întâlniți de majoritatea oamenilor, dar unii sunt toxici și trebuie tratați cu grijă. Expunerea pe termen lung și scurt la niobați și la clorura de niobiu, două chimicale care sunt solubile în apă, au fost testate pe șoareci. Șoarecii tratați cu o singură injecție cu pentaclorură de niobiu au arătat o doză mediană letală (LD50) între 10 și 100 mg/kg.[112][113][114] Pentru administrarea orală toxicitatea e mai scăzută; un studiu pe șoareci a avut LD50 după 7 zile de 940 mg/kg.[112]
O mare parte despre comportamentul niobiului in interiorul organismului este bazat pe studii asupra perechii radioizotopice 95Zr-95Nb, un produs comun al fisiunii nucleare. Un studiu a investigat incidenta cazurilor de cancer în rândul minerilor expuși la radon, găsind o asociere între cancerul pulmonar și radiația alfa cumulativa. Injectarea intravenoasă și intraperitoneală a niobiului (radioactiv) și a compușilor săi arătaseră o distribuire ușor uniformă, cu tendința de acumulare în ficat, rinichi, splină și măduva spinării.[115] Administrarea orala a pentaclorurii de niobiu cauzează iritarea acuta a stomacului și cauzează schimbări la nivelul ficatului; expunerea cronică timp de 4 luni de zile poate conduce la alterarea temporară a sângelui (leucocitoza, deficiență de protrombin).[115]
Niobiul inhalat este reținut în plămân, iar o doză zilnică de nitrit de niobiu inhalat, într-o concentrație de 40 mg/m3 poate conduce în câteva luni la semne de pneumoconioza; septul interalveolar este îngustat, fibre colagenoase se dezvoltă în țesutul peribronhial și perivascular și are loc descuamarea țesutului bronhial.[115] Schimbări similare intervin și în cazul în care praful pătrunde în organism pe cale intratraheală, fiind întâlnit în nodulii limfatici.[115]
Niobiul cationic este cu mult mai toxic decât niobații administrați parenteral, deoarece sărurile de niobiu cationic hidrolizează și formează compuși coloidali. Blocajul hepatic și renal reprezintă efectul toxic major al acestui metal.[116] Administrarea parenterala a pentaclorurii de niobiu conduce la respirație încetinită, letargie și, în cele din urmă, la deces.[110]
Deoarece niobiul este aproape inert în interiorul țesutului uman și fluidelor umane, practicele standard de igiena ar trebui respectate pentru a limita expunerea. În cazul contactului cu ochii, persoana intoxicată trebuie să se spele cu apă din abundență. Nici un protocol medical specific nu a fost realizat pentru această substanță.[117]
Note[modificare | modificare sursă]
- ^ See:
- Charles Hatchett (1802) "An analysis of a mineral substance from North America, containing a metal hitherto unknown", Philosophical Transactions of the Royal Society of London, 92 : 49–66.
- Hatchett, Charles (). „Eigenschaften und chemisches Verhalten des von Charles Hatchett entdeckten neuen Metalls, Columbium” [Properties and chemical behavior of the new metal, columbium, (that was) discovered by Charles Hatchett]. Annalen der Physik (în German). 11 (5): 120–122. Bibcode:1802AnP....11..120H. doi:10.1002/andp.18020110507.
- ^ a b Noyes, William Albert (). A Textbook of Chemistry. H. Holt & Co. p. 523.
- ^ Percival, James (ianuarie 1853). „Middletown Silver and Lead Mines”. Journal of Silver and Lead Mining Operations. 1: 186. Accesat în .
- ^ Griffith, William P.; Morris, Peter J. T. (). „Charles Hatchett FRS (1765–1847), Chemist and Discoverer of Niobium”. Notes and Records of the Royal Society of London. 57 (3): 299. doi:10.1098/rsnr.2003.0216. JSTOR 3557720.
- ^ a b Wollaston, William Hyde (). „On the Identity of Columbium and Tantalum”. Philosophical Transactions of the Royal Society. 99: 246–252. doi:10.1098/rstl.1809.0017. JSTOR 107264.
- ^ Rose, Heinrich (). „Ueber die Zusammensetzung der Tantalite und ein im Tantalite von Baiern enthaltenes neues Metall”. Annalen der Physik (în German). 139 (10): 317–341. Bibcode:1844AnP...139..317R. doi:10.1002/andp.18441391006.
- ^ Rose, Heinrich (). „Ueber die Säure im Columbit von Nordamérika”. Annalen der Physik (în German). 146 (4): 572–577. Bibcode:1847AnP...146..572R. doi:10.1002/andp.18471460410.
- ^ Kobell, V. (). „Ueber eine eigenthümliche Säure, Diansäure, in der Gruppe der Tantal- und Niob- verbindungen”. Journal für Praktische Chemie. 79 (1): 291–303. doi:10.1002/prac.18600790145.
- ^ a b c Marignac, Blomstrand, H. Deville, L. Troost und R. Hermann (). „Tantalsäure, Niobsäure, (Ilmensäure) und Titansäure”. Fresenius' Journal of Analytical Chemistry. 5 (1): 384–389. doi:10.1007/BF01302537.
- ^ a b c d e Gupta, C. K.; Suri, A. K. (). Extractive Metallurgy of Niobium. CRC Press. pp. 1–16. ISBN 0-8493-6071-4.
- ^ Marignac, M. C. (). „Recherches sur les combinaisons du niobium”. Annales de chimie et de physique (în French). 4 (8): 7–75.
- ^ Hermann, R. (). „Fortgesetzte Untersuchungen über die Verbindungen von Ilmenium und Niobium, sowie über die Zusammensetzung der Niobmineralien (Further research about the compounds of ilmenium and niobium, as well as the composition of niobium minerals)”. Journal für Praktische Chemie (în German). 3 (1): 373–427. doi:10.1002/prac.18710030137.
- ^ „Niobium”. Universidade de Coimbra. Arhivat din original la . Accesat în .
- ^ Geballe et al. (1993) raportează punctul critic al curenților ca fiind la 150 kiloamperi și cel al câmpurilor magnetice la 8.8 tesla.
- ^ a b Geballe, Theodore H. (octombrie 1993). „supraconductivity: From Physics to Technology”. Physics Today. 46 (10): 52–56. Bibcode:1993PhT....46j..52G. doi:10.1063/1.881384.
- ^ Matthias, B. T. (). „supraconductivity of Nb3Sn”. Physical Review. 95 (6): 1435–1435. Bibcode:1954PhRv...95.1435M. doi:10.1103/PhysRev.95.1435.
- ^ Kòrösy, F. (). „Reaction of Tantalum, Columbium and Vanadium with Iodine”. Journal of the American Chemical Society. 61 (4): 838–843. doi:10.1021/ja01873a018.
- ^ Ikenberry, Luther (). „Photometric Determination of Columbium, Tungsten, and Tantalum in Stainless Steels”. Analytical Chemistry. 25 (9): 1340–1344. doi:10.1021/ac60081a011.
- ^ a b c Rayner-Canham, Geoff; Zheng, Zheng (). „Naming elements after scientists: an account of a controversy”. Foundations of Chemistry. 10 (1): 13–18. doi:10.1007/s10698-007-9042-1.
- ^ Clarke, F. W. (). „Columbium Versus Niobium”. Science. 39 (995): 139–140. Bibcode:1914Sci....39..139C. doi:10.1126/science.39.995.139. JSTOR 1640945. PMID 17780662.
- ^ a b c d e Patel, Zh.; Khul'ka K. (). „Niobium for Steelmaking”. Metallurgist. 45 (11–12): 477–480. doi:10.1023/A:1014897029026.
- ^ Norman N., Greenwood (). „Vanadium to dubnium: from confusion through clarity to complexity”. Catalysis Today. 78 (1–4): 5–11. doi:10.1016/S0920-5861(02)00318-8.
- ^ Extractive Metallurgy of Niobium De C. K. Gupta,A. K. Suri, pagina 5
- ^ Oxide Semiconductors for Solar Energy Conversion: Titanium Dioxide De Janusz Nowotny, pagina 308
- ^ Encyclopedia of the Elements: Technical Data - History - Processing ..., de Per Enghag, pagina 551
- ^ a b Rajni Garg, Randhir Singh, Inorganic Chemistry, Cuprins
- ^ Extractive Metallurgy of Niobium De C. K. Gupta,A. K. Suri, pagina 4
- ^ a b c Georges, Audi; Bersillon, O.; Blachot, J.; Wapstra, A.H. (). „The NUBASE Evaluation of Nuclear and Decay Properties”. Nuclear Physics A. Atomic Mass Data Center. 729: 3–128. Bibcode:2003NuPhA.729....3A. doi:10.1016/j.nuclphysa.2003.11.001.
- ^ C. K. Gupta, A. K. Suri. Extractive Metallurgy of Niobium. Pag 4.
- ^ Ross W. Moshier. Analytical Chemistry of Niobium and Tantalum: International Series of .... Pag. 11.
- ^ a b Peiniger, M.; Piel, H. (). „A supraconducting Nb3Sn Coated Multicell Accelerating Cavity”. Nuclear Science. 32 (5): 3610. Bibcode:1985ITNS...32.3610P. doi:10.1109/TNS.1985.4334443.
- ^ Salles Moura, Hernane R. (). „Melting And Purification Of Niobium”. AIP Conference Proceedings. American Institute of Physics (927(Single Crystal – Large Grain Niobium Technology)): 165–178. ISSN 0094-243X. Arhivat din original la . Accesat în .
- ^ a b c d e f g h Nowak, Izabela; Ziolek, Maria (). „Niobium Compounds: Preparation, Characterization, and Application in Heterogeneous Catalysis”. Chemical Reviews. 99 (12): 3603–3624. doi:10.1021/cr9800208. PMID 11849031.
- ^ Jahnke, L.P. (). „Columbium Alloys Today”. Metal Progr. 77 (6): 69–74. OSTI 4183692.
- ^ Nikulina, A. V. (). „Zirconium-Niobium Alloys for Core Elements of Pressurized Water Reactors”. Metal Science and Heat Treatment. 45 (7–8): 287–292. doi:10.1023/A:1027388503837.
- ^ Extractive Metallurgy of Niobium, de C. K. Gupta,A. K. Suri, pagina 5
- ^ Lide, David R. (). „The Elements”. CRC Handbook of Chemistry and Physics (ed. 85). CRC Press. pp. 4–21. ISBN 978-0-8493-0485-9.
- ^ a b Ross W. Moshier. Analytical Chemistry of Niobium and Tantalum: International Series of ... . Pag. 12.
- ^ Emsley, John (). „Niobium”. Nature's Building Blocks: An A-Z Guide to the Elements. Oxford, England, UK: Oxford University Press. pp. 283–286. ISBN 0-19-850340-7.
- ^ Materials Handbook: A Concise Desktop Reference, De François Cardarelli, pagina 158
- ^ a b c d Soisson, Donald J. (). „Staff-Industry Collaborative Report: Tantalum and Niobium”. Industrial and Engineering Chemistry. 53 (11): 861–868. doi:10.1021/ie50623a016.
- ^ Lumpkin, Gregory R.; Ewing, Rodney C. (). „Geochemical alteration of pyrochlore group minerals: Pyrochlore subgroup” (PDF). American Mineralogist. 80: 732–743.
- ^ a b c Kouptsidis, J; Peters, F.; Proch, D.; Singer, W. „Niob für TESLA” (PDF) (în German). Deutsches Elektronen-Synchrotron DESY. Arhivat din original (PDF) la . Accesat în .
- ^ Materials Handbook: A Concise Desktop Reference, de François Cardarelli, pagina 158
- ^ Mining firm to build Sh12.8bn factory - Money Markets
- ^ Area residents dig the prospect of niobium mine
- ^ John Patrick Albers, Gus Hossein Goudarzi. Demand and supply of nonfuel minerals and materials for the United States ... . Pag. B-24
- ^ a b c d e f g Holleman, Arnold F. (). „Niob”. Lehrbuch der Anorganischen Chemie (în German) (ed. 91–100). Walter de Gruyter. pp. 1075–1079. ISBN 3-11-007511-3.
- ^ Greenwood, Norman N.; Earnshaw, Alan (). Chemistry of the Elements (ed. 2nd). Oxford: Butterworth-Heinemann. ISBN 0080379419.
- ^ Cardarelli, Francois (). Materials Handbook. Springer London. ISBN 978-1-84628-668-1.
- ^ Rahtu, Antti (). Atomic Layer Deposition of High Permittivity Oxides: Film Growth and In Situ Studies (Teză). University of Helsinki. ISBN 952-10-0646-3.
- ^ Maruyama, Toshiro (). „Electrochromic Properties of Niobium Oxide Thin Films Prepared by Chemical Vapor Deposition”. Journal of the Electrochemical Society. 141 (10): 2868. doi:10.1149/1.2059247.
- ^ a b Agulyansky, Anatoly (). The Chemistry of Tantalum and Niobium Fluoride Compounds. Elsevier. pp. 1–11. ISBN 978-0-444-51604-6.
- ^ C. R. Lucas, J. A. Labinger, J. Schwartz (). Robert J. Angelici, ed. „Dichlorobis(η5-Cyclopentadienyl)Niobium(IV)”. Inorganic Syntheses. Inorganic Syntheses. New York: J. Wiley & Sons. 28: 267–270. doi:10.1002/9780470132593.ch68. ISBN 0-471-52619-3.
- ^ Greenwood, Norman N.; Earnshaw, Alan (). Chemistry of the Elements (ed. 2nd). Oxford: Butterworth-Heinemann. ISBN 0080379419.
- ^ Verevkin, A. (). „Ultrafast supraconducting single-photon detectors for near-infrared-wavelength quantum communications”. Journal of Modern Optics. 51 (12): 1447–1458. doi:10.1080/09500340410001670866.
- ^ Inorganic Chemistry, de Egon Wiberg,Nils Wiber, pagina 1355
- ^ Tither, Geoffrey (). Minerals, Metals and Materials Society, Metals and Materials Society Minerals, ed. „Progress in Niobium Markets and Technology 1981–2001” (PDF). Niobium Science & Technology: Proceedings of the International Symposium Niobium 2001 (Orlando, Florida, USA). Niobium 2001 Ltd, 2002. ISBN 978-0-9712068-0-9. Arhivat din original (PDF) la . Accesat în .
- ^ Dufresne, Claude; Goyette, Ghislain (). Minerals, Metals and Materials Society, Metals and Materials Society Minerals, ed. „The Production of Ferroniobium at the Niobec mine 1981–2001” (PDF). Niobium Science & Technology: Proceedings of the International Symposium Niobium 2001 (Orlando, Florida, USA). Niobium 2001 Ltd, 2002. ISBN 978-0-9712068-0-9. Arhivat din original (PDF) la .
- ^ Choudhury, Alok; Hengsberger, Eckart (). „Electron Beam Melting and Refining of Metals and Alloys”. The Iron and Steel Institute of Japan International. 32 (5): 673–681. doi:10.2355/isijinternational.32.673.
- ^ Lucchesi, Cristane; Cuadros, Alex (aprilie 2013), „Mineral Wealth”, Bloomberg Markets (paper), p. 14
- ^ Papp, John F. „Niobium (Columbium)” (PDF). USGS 2006 Commodity Summary. Accesat în .
- ^ a b Papp, John F. „Niobium (Columbium)” (PDF). USGS 2007 Commodity Summary. Accesat în .
- ^ Papp, John F. „Niobium (Columbium)” (PDF). USGS 1997 Commodity Summary. Accesat în .
- ^ Niobium (Colombium) U.S. Geological Survey, Mineral Commodity Summaries, January 2011
- ^ Larry D. Cunningham (). „USGS Minerals Information: Niobium (Columbium) and Tantalum”. Minerals.usgs.gov. Accesat în .
- ^ a b Papp, John F. „Niobium (Columbium ) and Tantalum” (PDF). USGS 2006 Minerals Yearbook. Accesat în .
- ^ a b Heisterkamp, Friedrich; Tadeu Carneiro (). Minerals, Metals and Materials Society, Metals and Materials Society Minerals, ed. „Niobium: Future Possibilities – Technology and the Market Place” (PDF). Niobium Science & Technology: Proceedings of the International Symposium Niobium 2001 (Orlando, Florida, USA). Niobium 2001 Ltd, 2002. ISBN 978-0-9712068-0-9. Arhivat din original (PDF) la .
- ^ Eggert, Peter (). „Niobium: a steel additive with a future”. Economic Bulletin. 19 (9): 8–11. doi:10.1007/BF02227064.
- ^ Hillenbrand, Hans–Georg (). „Development and Production of High Strength Pipeline Steels” (PDF). Niobium Science & Technology: Proceedings of the International Symposium Niobium 2001 (Orlando, Florida, USA). Europipe. Arhivat din original (PDF) la .
- ^ Elements and the Periodic Table, Grades 5 - 8, de Theodore S. Abbgy, pagina 37
- ^ a b c Hebda, John (). „Niobium alloys and high Temperature Applications” (PDF). Niobium Science & Technology: Proceedings of the International Symposium Niobium 2001 (Orlando, Florida, USA). Companhia Brasileira de Metalurgia e Mineração. Arhivat din original (PDF) la .
- ^ Donachie, Matthew J. (). Superalloys: A Technical Guide. ASM International. pp. 29–30. ISBN 978-0-87170-749-9.
- ^ Bhadeshia, H. k. d. h. „Nickel Based Superalloys”. University of Cambridge. Accesat în .
- ^ Pottlacher, G. (). „Thermophysikalische Eigenschaften von festem und flüssigem Inconel 718”. Thermochimica Acta (în German). 382 (1––2): 55–267. doi:10.1016/S0040-6031(01)00751-1.
- ^ Lindenhovius, J.L.H.; Hornsveld, E.M.; Den Ouden, A.; Wessel, W.A.J.; Ten Kate, H.H.J. (). „Powder-in-tube (PIT) Nb/sub 3/Sn conductors for high-field magnets”. IEEE Transactions on Applied supraconductivity. 10: 975–978. doi:10.1109/77.828394.
- ^ Nave, Carl R. „supraconducting Magnets”. Georgia State University, Department of Physics and Astronomy. Accesat în .
- ^ Glowacki, B. A.; Yan, X. -Y.; Fray, D.; Chen, G.; Majoros, M.; Shi, Y. (). „Niobium based intermetallics as a source of high-current/high magnetic field supraconductors”. Physica C: supraconductivity. 372–376 (3): 1315–1320. arXiv:cond-mat/0109088
 . Bibcode:2002PhyC..372.1315G. doi:10.1016/S0921-4534(02)01018-3.
. Bibcode:2002PhyC..372.1315G. doi:10.1016/S0921-4534(02)01018-3.
- ^ Grunblatt, G. (). „A success story: LHC cable production at ALSTOM-MSA”. Fusion Engineering and Design (Proceedings of the 23rd Symposium of Fusion Technology). 75–79: 1–5. doi:10.1016/j.fusengdes.2005.06.216.
- ^ Lilje, L. (). „Achievement of 35 MV/m in the supraconducting nine-cell cavities for TESLA”. Nuclear Instruments and Methods in Physics Research Section A: Accelerators, Spectrometers, Detectors and Associated Equipment. 524 (1–3): 1–12. arXiv:physics/0401141
 . Bibcode:2004NIMPA.524....1L. doi:10.1016/j.nima.2004.01.045.
. Bibcode:2004NIMPA.524....1L. doi:10.1016/j.nima.2004.01.045.
- ^ Cherednichenko, Sergey (). „A Hot-electron bolometer terahertz mixers for the Herschel Space Observatory”. Review of Scientific Instruments. 79 (3): 0345011–03451010. Bibcode:2008RScI...79c4501C. doi:10.1063/1.2890099. PMID 18377032.
- ^ a b Brazil Mineral & Mining Sector Investment and Business Guide, de USA International Business Publications, pagina 157
- ^ Volk, Tatyana; Wohlecke, Manfred (). Lithium Niobate: Defects, Photorefraction and Ferroelectric Switching. Springer. pp. 1–9. ISBN 978-3-540-70765-3.
- ^ Pozdeev, Y. (). „Reliability comparison of tantalum and niobium solid electrolytic capacitors”. Quality and Reliability Engineering International. 14 (2): 79–82. doi:10.1002/(SICI)1099-1638(199803/04)14:2<79::AID-QRE163>3.0.CO;2-Y.
- ^ Mallela, Venkateswara Sarma (). „Trends in Cardiac Pacemaker Batteries”. Indian Pacing Electrophysiol J. 4 (4): 201–212. PMC 1502062
 . PMID 16943934.
. PMID 16943934.
- ^ Godley, Reut (). „Bonelike apatite formation on niobium metal treated in aqueous NaOH” (PDF). Journal of Materials Science: Materials in Medicine. 15 (10): 1073–1077. doi:10.1023/B:JMSM.0000046388.07961.81. PMID 15516867.[nefuncțională]
- ^ Biason Gomes, M. A. (). „Anodization of niobium in sulphuric acid media”. Journal of Applied Electrochemistry. 21 (11): 1023–1026. doi:10.1007/BF01077589.
- ^ Chiou, Y. L. (). „A note on the thicknesses of anodized niobium oxide films”. Thin Solid Films. 8 (4): R37–R39. Bibcode:1971TSF.....8R..37C. doi:10.1016/0040-6090(71)90027-7.
- ^ Azevedo, C. R. F. (). „Characterization of metallic piercings that caused adverse reactions during use”. Journal of Failure Analysis and Prevention. 2 (4): 47–53. doi:10.1361/152981502770351860. Arhivat din original la . Accesat în .
- ^ a b Analytical Chemistry of Niobium and Tantalum: International Series of ..., de Ross W. Moshier, pagina 7
- ^ One Coin is Never Enough: Why and How We Collect; De Michael S. Shutty Jr. Ph.D, pagina 175
- ^ Grill, Robert; Gnadenberge, Alfred (). „Niobium as mint metal: Production–properties–processing”. International Journal of Refractory Metals and Hard Materials. 24 (4): 275–282. doi:10.1016/j.ijrmhm.2005.10.008.
- ^ One Coin is Never Enough: Why and How We Collect De Michael S. Shutty Jr. Ph.D, pagina 175
- ^ „25 Euro – 150 Years Semmering Alpine Railway (2004)”. Austrian Mint. Arhivat din originalul de la . Accesat în .
- ^ „150 Jahre Semmeringbahn” (în German). Austrian Mint. Arhivat din originalul de la . Accesat în .
- ^ „Neraža – mēs nevarējām atrast meklēto lapu!” (în Latvian). Bank of Latvia. Arhivat din original la . Accesat în .
- ^ „Neraža – mēs nevarējām atrast meklēto lapu!” (în Latvian). Bank of Latvia. Arhivat din original la . Accesat în .
- ^ „$5 Sterling Silver and Niobium Coin – Hunter's Moon (2011)”. Royal Canadian Mint. Arhivat din original la . Accesat în .
- ^ Henderson, Stanley Thomas (). Lamps and Lighting. Edward Arnold Press. pp. 244–245. ISBN 0-7131-3267-1.
- ^ Eichelbrönner, G. (). „Refractory metals: crucial components for light sources”. International Journal of Refractory Metals and Hard Materials. 16 (1): 5–11. doi:10.1016/S0263-4368(98)00009-2.
- ^ Michaluk, Christopher A. (). Minerals, Metals and Materials Society, Metals and Materials Society Minerals, ed. „Niobium and Niobium 1% Zirconium for High Pressure Sodium (HPS) Discharge Lamps”. Niobium Science & Technology: Proceedings of the International Symposium Niobium 2001 (Orlando, Florida, USA). Niobium 2001 Ltd, 2002. ISBN 978-0-9712068-0-9.
- ^ US patent 5254836, Okada, Yuuji; Kobayashi, Toshihiko; Sasabe, Hiroshi; Aoki, Yoshimitsu; Nishizawa, Makoto; Endo, Shunji, "Method of arc welding with a ferrite stainless steel welding rod", issued 1993-10-19
- ^ Moavenzadeh, Fred (). Concise Encyclopedia of Building and Construction Materials. MIT Press. pp. 157–. ISBN 978-0-262-13248-0. Accesat în .
- ^ Cardarelli, François (). Materials handbook: a concise desktop reference. Springer. pp. 352–. ISBN 978-1-84628-668-1. Accesat în .
- ^ Analytical Chemistry of Niobium and Tantalum: International Series of ...,de Ross W. Moshier, pagina 7
- ^ Vilaplana, J. (). „New trends in the use of metals in jewellery”. Contact Dermatitis. 25 (3): 145–148. doi:10.1111/j.1600-0536.1991.tb01819.x. PMID 1782765.
- ^ Vilaplana, J.; Romaguera, C. (). „New developments in jewellery and dental materials”. Contact Dermatitis. 39 (2): 55–57. doi:10.1111/j.1600-0536.1998.tb05832.x. PMID 9746182.
- ^ Nature's Building Blocks: An A-Z Guide to the Elements, de John Emsley, pagina 283
- ^ a b c d Trace Elements in Human and Animal Nutrition, Volumul 2, pagina 451
- ^ a b Principles and Methods of Toxicology, Fifth Edition, editat de A. Wallace Hayes, pagina 873
- ^ a b Metalloproteomics, de Eugene Permyakov, pagina 580
- ^ a b Haley, Thomas J. (). „Pharmacology and toxicology of niobium chloride”. Toxicology and Applied Pharmacology. 4 (3): 385–392. doi:10.1016/0041-008X(62)90048-0. PMID 13903824.
- ^ Downs, William L. (). „The Toxicity of Niobium Salts”. American Industrial Hygiene Association Journal. 26 (4): 337–346. doi:10.1080/00028896509342740. PMID 5854670.
- ^ Schroeder, Henry A. (). „Zirconium, Niobium, Antimony, Vanadium and Lead in Rats: Life term studies”. Journal of Nutrition. 100 (1): 59–68. PMID 5412131.
- ^ a b c d Encyclopaedia of Occupational Health and Safety: Chemical, industries and ..., editat de Jeanne Mager Stellman, pagina 63,34
- ^ Physiologic and Chemical Basis for Metal Toxicity De B. Venugopal, pagina 181
- ^ Hamilton and Hardy's Industrial Toxicology De Raymond D. Harbison,Marie M. Bourgeois,Giffe T. Johnson, pagina 185
Bibliografie[modificare | modificare sursă]
- D. Marian, Metale de înaltă puritate, Editura Tehnică, 1988
- Galia Gruder, Metale neobișnuite, Editura Științifică, 1964
Legături externe[modificare | modificare sursă]
- Los Alamos National Laboratory – Niobium
- Tantalum-Niobium International Study Center
- Niobium for particle accelerators eg ILC. 2005 Arhivat în , la Wayback Machine.
 „Columbium”. Encyclopædia Britannica (ed. 11). .
„Columbium”. Encyclopædia Britannica (ed. 11). . „Columbium”. New International Encyclopedia. .
„Columbium”. New International Encyclopedia. .- Niobium at The Periodic Table of Videos (University of Nottingham)
- Spectroscopical, monoclorura (NbCl) a fost observată la temperaturi ridicate: vezi Ram, R.S. (). „Fourier transform emission spectroscopy and ab initio calculations on NbCl” (PDF). Journal of Molecular Spectroscopy. 228 (2): 544–553. Bibcode:2004JMoSp.228..544R. doi:10.1016/j.jms.2004.02.001. Arhivat din original (PDF) la .
| |||||||||||||||||||||||||||||||||||||


