Acid tartric
Acest articol sau secțiune are mai multe probleme. Puteți să contribuiți la rezolvarea lor sau să le comentați pe pagina de discuție. Pentru ajutor, consultați pagina de îndrumări.
Nu ștergeți etichetele înainte de rezolvarea problemelor. |
| Acid tartric | |
 | |
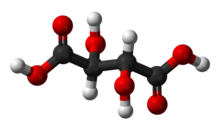 | |
| Nume IUPAC | Acid 2,3-dihidroxibutandioic |
|---|---|
| Alte denumiri | Acid tartric Acid 2,3-dihidroxisuccinic Acid racemic Acid uvic |
| Identificare | |
| Număr CAS | [526-83-0] |
| ChEMBL | CHEMBL333714 |
| PubChem CID | 875 |
| Informații generale | |
| Formulă chimică | HOOC-CHOH-CHOH-COOH |
| Aspect | Pulbere albă |
| Masă molară | 150,087 g/mol |
| Proprietăți | |
| Densitate | 1,790 g/cm3 |
| Starea de agregare | solidă |
| Punct de topire | 171–174 °C (L-tartaric) 206 °C (DL, racemic) 146–148 °C (meso) ) |
| Aciditate (pKa) | 3,04 4,37 |
| Sunt folosite unitățile SI și condițiile de temperatură și presiune normale dacă nu s-a specificat altfel. | |
| Modifică date / text | |
Acidul tartric (acidul 2,3-dihidroxibutandioic) este un acid organic, diprotic, cu formula HOOC-CHOH-CHOH-COOH. Acesta este un dihidroxi-derivat al acidului succinic. Acidul tartric poate fi găsit în numeroase plante, și în numeroase fructe, precum strugurii și bananele. Acidul tartric este unul din acizii importanți ce se găsesc în vin (în forma L(+)). Este un reducător destul de puternic.
Tartratul mixt de potasiu și de sodiu este folosit în prepararea soluției Fehling. Acidul tartric a fost izolat prima dată de chimistul suedez Carl Wilhelm Scheele în 1769. Chiralitatea acidului tartric a fost descoperită în 1832 de Jean Baptiste Biot, care a descoperit că acesta putea roti planul luminii polarizate. Louis Pasteur a continuat cercetările asupra chiralității acidului tartric, cercetând în 1847 forma cristalelor tartratului de sodiu și amoniu. Pasteur a produs primul acid levotartric pur.
Acidul tartric este folosit precum aditiv alimentar (E334), antioxidant, regulator de pH și sechestrant.
În gravimetrie este folosită o soluție de acid tartric pentru a precipita ionii de calciu, potasiu, magneziu, stronțiu, scandiu și tantal. Cei doi enantiomeri ai acidului tartric (L-(+) și D-(–)), pot de asemenea fi folosiți la separarea unui amestec de enantiomeri.
Acidul tartric natural este chiral, în sensul că moleculele sale sunt asimetrice, non-superpozabile pe imaginea lor în oglindă. Este o materie primă utilă în chimia organică pentru sinteza altor molecule chirale. Apare, în mod natural, sub o singură formă: acid L-(+)-tartric (dextrotartaric). Enantiomerul său, acidul levotartaric sau D-(-)-tartric, și forma achirală, acidul mezotartaric, se pot sintetiza în mod artificial. Formele dextro și levo nu sunt identice cu configurația D / L (care este derivată convențional din D-sau L-glicerinaldehida). Acestea sunt abrevierile dextro- și levo-, iar astăzi acestea nu ar trebui să fie utilizate. Acizii levotartaric și dextrotartaric sunt enantiomeri între ei, iar acidul mezotartaric este un diastereoizomer pentru ambele.
O formă rară optic inactivă a acidului tartric, acid DL-tartric, este un amestec 1:1 de acizi levo- și dextrotartric. Acesta este diferit de acid mezotartaric, și a fost denumit și acid racemic (de la racemus din latină - "un ciorchine de struguri"). Cuvânt racemic și-a modificat mai târziu sensul, devenind un termen general pentru toate amestecurile enantiomerice 1:1 - racemații.
Acidul tartric este utilizat pentru a preveni ionii de cupru (II) să reacționeze cu ionii de hidroxid (HO-), prezenți în prepararea soluției de oxid de cupru (I). Oxidul cupros este un precipitat de culoare brun-roșcată, și rezultă din reducerea sării cuprice cu o aldehidă într-o soluție alcalină.
Vezi și[modificare | modificare sursă]
Bibliografie[modificare | modificare sursă]
- C. D. Nenițescu, Chimie generală
- Constantin D. Albu, Maria Brezeanu, Mică enciclopedie de chimie, Editura Enciclopedică Română, 1974, p 26
Referințe[modificare | modificare sursă]
- ^ „Acid tartric”, 2,3-Dihydroxybutanedioic acid (în engleză), PubChem, accesat în
| ||||||||

